Sử dụng thuốc kháng sinh trong điều trị viêm nội tâm mạc nhiễm khuẩn
PHẦN I. CÁC VẤN ĐỀ CHUNG
1. DỊCH TỄ HỌC
Ngày nay, mặc dù đã có rất nhiều tiến bộ về bệnh nguyên, chẩn đoán, tiên lượng và điều trị viêm nội tâm mạc nhiễm khuẩn (VNTMNK), nhưng hiểu biết của chúng ta về VNTMNK rõ ràng còn nhiều thiếu sót. Tỷ lệ mắc hằng năm gần như không thay đổi, dao động từ 3 đến 9 ca trong 100.000 người ở các nước công nghiệp phát triển. Tỷ lệ tử vong trong viện dao động từ 15% đến 20%, tỷ lệ tử vong sau 1 năm từ 30% đến 40% tùy thuộc vào chủng vi sinh, vị trí van tổn thương, loại van, các bệnh lý kèm theo, chỉ thay đổi rất ít trong vòng 20 năm qua.
Đa số bệnh nhân có tổn thương tim cấu trúc trước đó (bệnh van tim, van tim nhân tạo, bệnh tim bẩm sinh có tím…), trừ trường hợp bệnh nhân nghiện chích ma túy hoặc chủng vi khuẩn có độc lực cao, bệnh nhân cũng có thể mắc VNTMNK mà không có tổn thương cấu trúc tim rõ ràng trước đó.
2. SINH LÝ BỆNH

Hình 21.1: Bệnh sinh của viêm nội tâm mạc nhiễm khuẩn
AO: Động mạch chủ, LA: nhĩ trái, LV: thất trái, PA: động mạch phổi; RA: nhĩ phải, RV: thất phải. (Nguồn: Bashore TM, et al. Update on infective endocarditis. Curr Probl Cardiol. 2006 Apr;31(4):274-352).
A, Sùi do viêm nội tâm mạc nhiễm khuẩn thường ở nơi dòng máu có tốc độ cao đi qua
gây tổn thương nội mạc. Cần chú ý rằng sùi nằm ở phía mặt nhĩ của van nhĩ – thất và ở mặt thất của van bán nguyệt. Ngoài ra, dòng phụt ngược từ các van bán nguyệt (van tổ chim) có thể làm tổn thương dây chằng. Dấu hoa thị đánh dấu các khu vực tổn thương do dòng máu gây ra (mảng McCallum) trên nội tâm mạc trong thông liên thất (trên lá vách van ba lá) hoặc ở nhĩ trái do dòng phụt ngược qua van hai lá.
B, Các giai đoạn phát triển tổn thương của viêm nội tâm mạc trên van động mạch chủ.
(1) Lá van động mạch chủ bình thường có một phần dày lên ở dưới đường mép là vùng các lá van áp với nhau và là nơi hay xảy ra tổn thương. Lớp nội mạc phủ lên lá van là một phần mở rộng của nội mạc động mạch chủ và tâm thất. Lớp sợi là cấu trúc nâng đỡ chính cho lá van. Lớp thất nằm dưới bờ tự do của lá van và lớp xốp nằm ở phần trung tâm, giữa lớp sợi và lớp thất.
(2) Các tổn thương ban đầu ở nội mạc và làm bộc lộ collagen của van.
(3) Sự lắng đọng tiểu cầu và tơ huyết với sự hình thành của tổn thương nội mạc dạng huyết khối vô khuẩn.
(4) Các vi sinh vật bám vào và xâm nhập vào tổn thương nội mạc, sau đó nhân lên. Các tế bào viêm thâm nhập, phá hủy elastin và collagen, gây tổn hại đến van tim.
Bình thường lớp nội mạc đóng vai trò như một hàng rào tự nhiên bảo vệ chống lại các vi khuẩn gây bệnh. Khi lớp nội mạc bị tổn thương, theo sau đó là sự lắng đọng tiểu cầu – fibrin, tạo điều kiện thuận lợi cho vi khuẩn có thể bám dính lại, phát triển và hình thành tổn thương sùi. Hầu hết các vị trí hình thành sùi đều tương ứng với lớp nội mạc bị dòng máu gây tổn thương, ví dụ: ở mặt thất của các van tổ chim, ở mặt nhĩ của các van nhĩ thất.
Khoảng 30% bệnh nhân không có bằng chứng của tổn thương cấu trúc tim trước đó. Một số vi khuẩn có động lực cao có khả năng gây tổn thương trên cả van bình thường gồm: S. aureus, một số Streptococcus, Salmonella, Rickettsia, Borrelia…
3. MỘT SỐ KHÁI NIỆM CƠ BẢN VỀ VI KHUẨN HỌC
3.1. Nhuộm Gram
Do vi khuẩn không có màu và thường vô hình dưới kính hiển vi, do đó các phương pháp nhuộm đã được phát triển để có thể quan sát được hình thái vi khuẩn. Phương pháp hữu dụng nhất là nhuộm Gram, được phát minh bởi nhà vi sinh học người Đan Mạch Hans Christian Gram năm 1884. Phương pháp này giúp chia vi khuẩn thành hai nhóm: Gram âm và Gram dương.
Sự khác biệt về kết quả khi nhuộm Gram là do sự khác biệt về cấu trúc thành tế bào của vi khuẩn Gram âm và Gram dương.
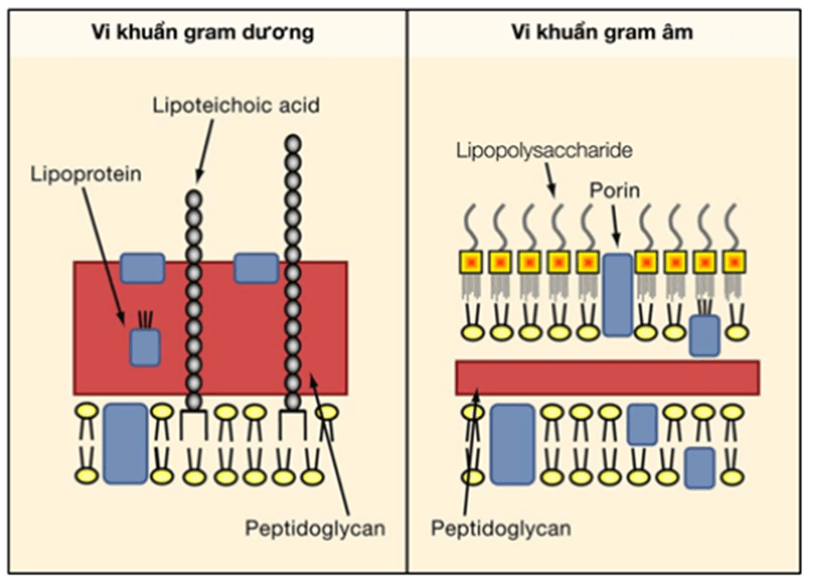
Hình 21.2: Cấu trúc thành tế bào của vi khuẩn Gram dương và Gram âm. (Nguồn: Shizuo Akira, et al. Pathogen Recognition and Innate Immunity. Cell. 2006 Feb; 124, 783–801)
Vi khuẩn Gram dương có lớp vách tế bào được tạo bởi lớp peptidoglycan dày, liên kết chặt chẽ. Mặt trong vách tế bào tiếp xúc với màng tế bào, được cấu tạo bởi một lớp phospholipid kép. Khác với màng tế bào của các loài động vật, màng tế bào vi khuẩn không có cholesterol hay các loại sterol khác.
Vi khuẩn Gram âm có lớp vách peptidoglycan mỏng hơn, liên kết ít và lỏng lẻo hơn. Mặt trong là lớp màng tế bào phospholipid kép. Ngoài ra, khác với vi khuẩn Gram dương, vi khuẩn Gram âm có thêm một lớp áo ngoài (lipopolysaccharide) có chứa lipid A. Lipid A là một chất độc đối với con người, đây là nội độc tố của vi khuẩn Gram âm. Khi tế bào vi khuẩn bị ly giải do hoạt động của hệ miễn dịch, do thuốc kháng sinh… lipid A được giải phóng vào hệ tuần hoàn, có thể gây tình trạng sốc nhiễm độc.
Sự khác biệt về kết quả khi nhuộm Gram là do sự khác biệt về cấu trúc vách tế bào vi khuẩn. Vi khuẩn Gram dương có lớp peptidoglycan dày, dạng lưới, có khả năng giữ phức hợp iod sử dụng khi nhuộm Gram. Trong khi đó, lớp peptidoglycan của các vi khuẩn Gram âm mỏng hơn và thường có thêm lớp màng lipopolysaccharide bên ngoài, do đó phức hợp tím iod sẽ bị rửa trôi.
Ý nghĩa lâm sàng: Lớp vách peptidoglycan đơn thuần của vi khuẩn Gram dương không ngăn cản được các chất có trọng lượng phân tử thấp, do đó các chất như kháng sinh, thuốc nhuộm, thuốc tẩy rửa có thể đi qua được. Ngược lại, lớp lipopolysaccharide của vi khuẩn Gram âm ngăn chặn các chất trên đi qua, do đó, kháng sinh, hóa chất tấn công lớp peptidoglycan bị vô hiệu hóa tác dụng.
3.2. Hình dạng vi khuẩn
Bảng 21.1: Phân loại hình dạng vi khuẩn
|
Hình dạng |
Gram dương |
Gram âm |
|
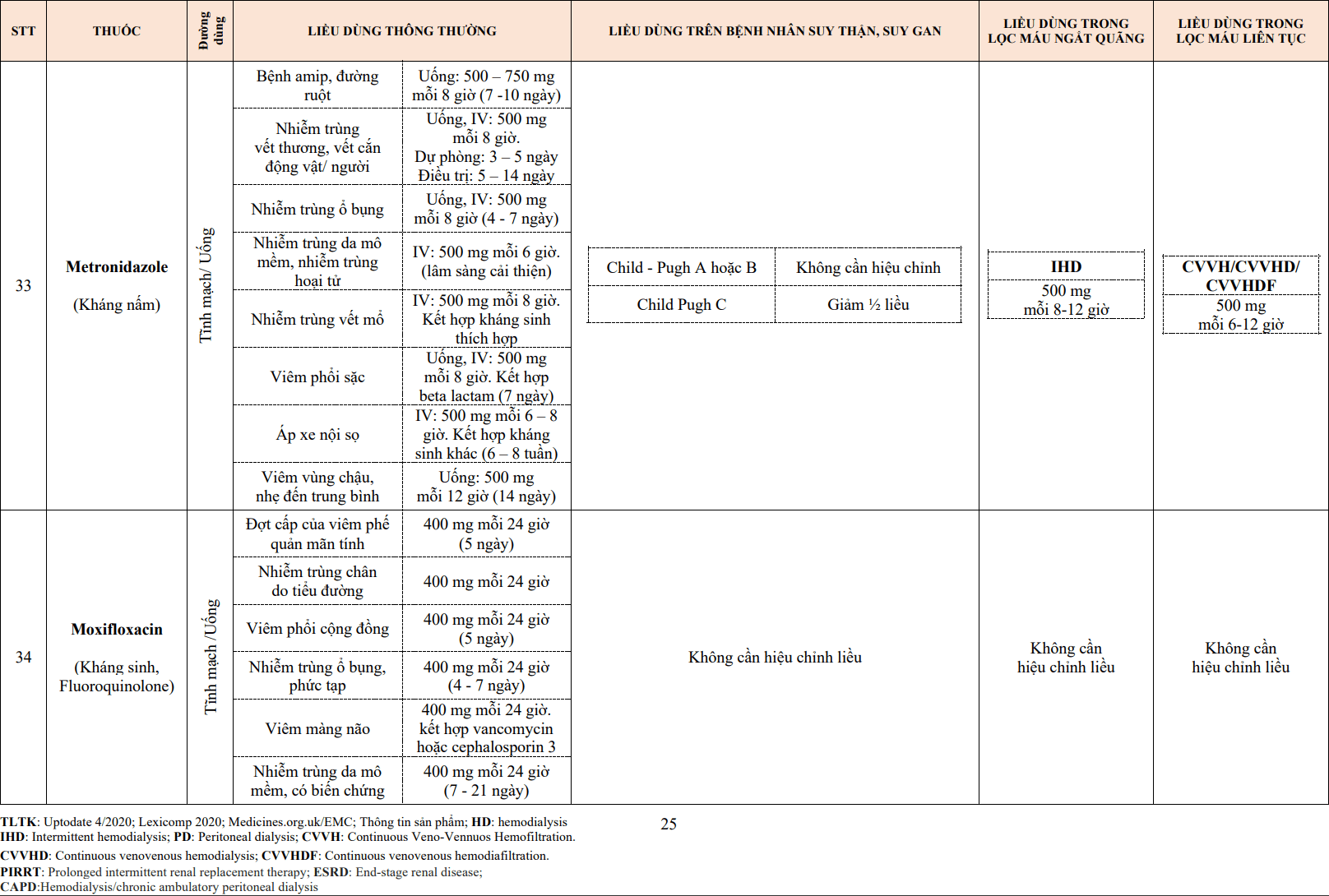
Cầu khuẩn |
Streptococcus Staphylococcus |
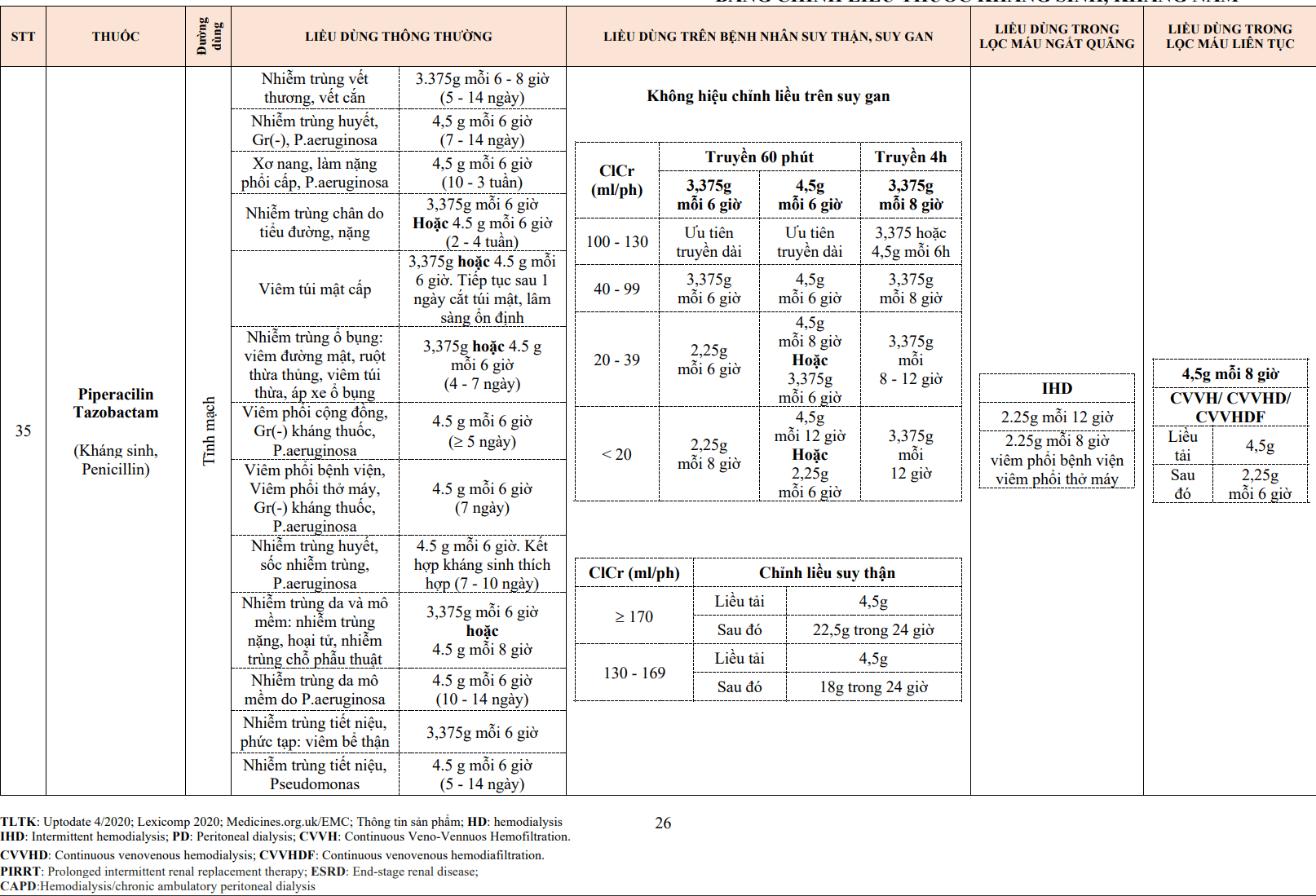
Neisseria |
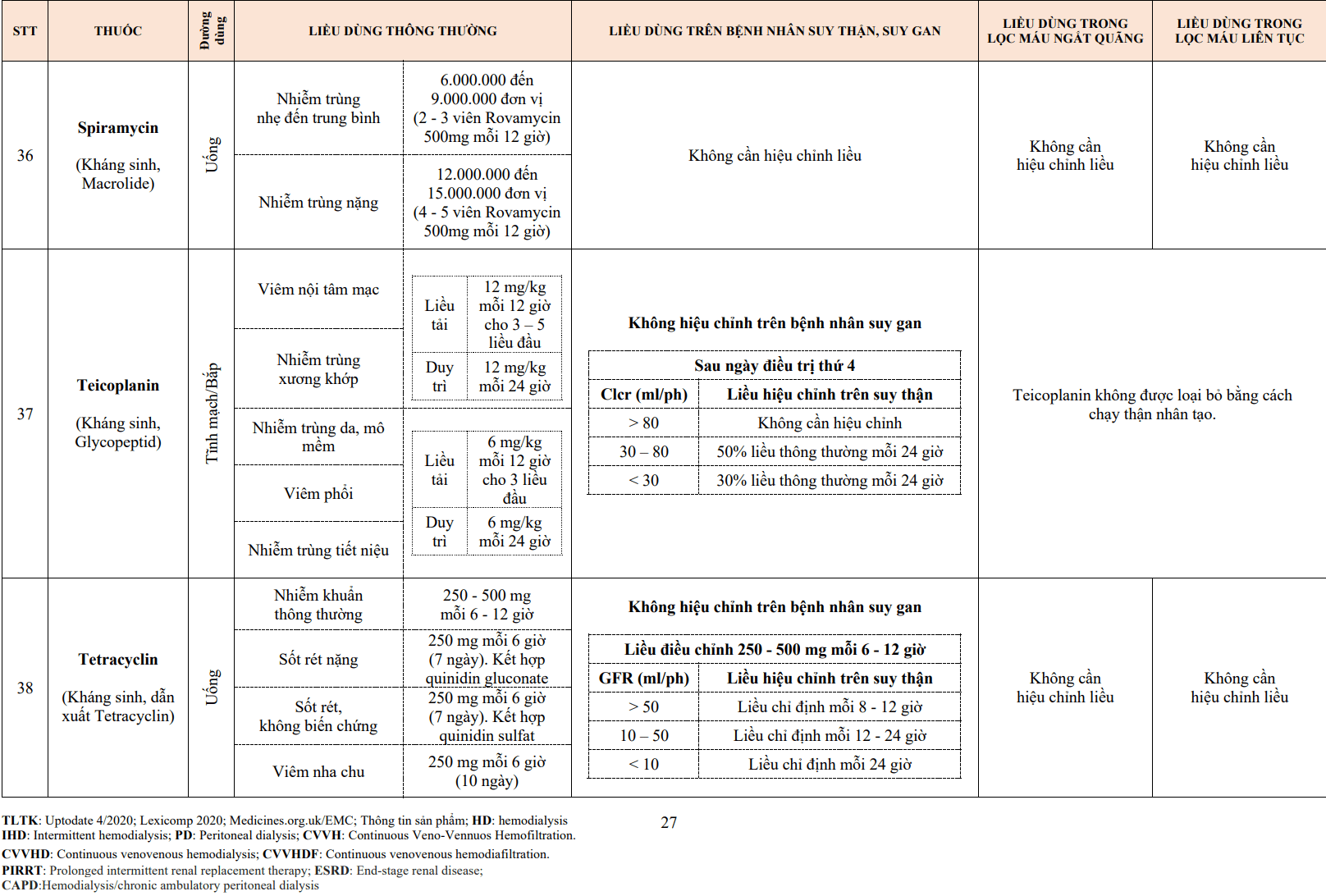
|
Trực khuẩn |
Corynebacterium Listeria Bacillus Clostridium Mycobacterium |
Enterics Escherichia coli Shigella Salmonella Yersinia Klebsiella Proteus Enterobacter Vibrio Campylobacter Helicobacter Pseudomonas Haemophilus Bordetella Legionella Francisella Brucella Pasteurella Gardnerella |
|
Xoắn khuẩn |
Treponema Borrelia Leptospira |
|
|
Dạng sợi phân nhánh |
Actinomyces Nocardia |
|
|
Đa hình thái |
Chlamydia Rickettsiae |
|
|
Không có vách tế bào |
Mycoplasma |
|
3.2. Hiếu khí và kỵ khí
Cách vi khuẩn đáp ứng với oxy là một trong các yếu tố chính để phân loại vi khuẩn. Phân tử oxy có hoạt tính rất cao, hình thành nên các phân tử có hoạt tính cao hydro peroxide (oxy già – H2O2), các gốc tự do (O2– , OH–). Đây đều là những chất độc với tế bào.
Vi khuẩn hiếu khí là các vi khuẩn có các enzym bảo vệ để phân hủy các sản phẩm chuyển hóa của oxy (catalase, peroxidase, superoxide dismutase).
Vi khuẩn kỵ khí là những vi khuẩn không có các enzym trên và sẽ chết khi có mặt của oxy.
- Vi khuẩn hiếu khí bắt buộc: Các vi khuẩn này sử dụng glycoside, chu trình Krebs, sử dụng oxy làm chất nhận electron cuối cùng. Chúng có tất cả các loại enzym nói trên.
- Vi khuẩn kỵ khí tùy ý: Sử dụng oxy như chất nhận electron cuối cùng trong chuỗi chuyển hóa. Chúng có hai enzym là catalase và superoxide dismutase. Tuy nhiên, điểm khác biệt là những chủng vi khuẩn này có thể phát triển khi không có mặt oxy, bằng cách sử dụng quá trình hô hấp yếm khí (lên men) để lấy năng lượng.
- Vi khuẩn vi hiếu khí: lấy năng lượng nhờ quá trình lên hô hấp yếm khí và không có hệ thống vận chuyển electron. Tuy nhiên, chúng có thể dung nạp với một lượng nhỏ oxy do có một enzyme là superoxide dismutase.
- Vi khuẩn kỵ khí bắt buộc: Các vi khuẩn này không có cả ba loại enzyme nói trên.
Bảng 21.2: Phân loại các vi khuẩn hiếu, kỵ khí
|
Hiếu khí bắt buộc |
Kỵ khí tùy ý |
Vi hiếu khí |
Kỵ khí bắt buộc |
|
|
Gram dương |
Nocardia Bacillus cereus |
Staphylococcus Bacillus anthracis Corynebacterium Listeria Actinomyces |
Streptococcus |
Clostridium |
|
Gram âm |
Neisseria Pseudomonas Bordetella Legionella Brucella |
Spirochetes Treponema Borrelia Leptospira Campylobacter |
Bacteroides |
|
|
Kháng toan |
Mycobacterium Nocardia |
|||
|
Không có vách tế bào |
Mycoplasma |
Trên lâm sàng, khi cấy máu cho bệnh nhân, cần lấy hai mẫu máu, một cho vào môi trường nuôi cấy hiếu khí và một cho vào môi trường nuôi cấy kỵ khí.
3.4. Độc tố vi khuẩn
- Ngoại độc tố: là những protein được giải phóng bởi cả vi khuẩn Gram âm và Gram dương, chúng có thể gây nhiều biểu hiện bệnh lý khác nhau.
- Nội độc tố: là lipid A – một thành phần trong cấu tạo lớp vỏ ngoài lipopolysaccharide của vi khuẩn Gram âm. Lipid A cực độc và được giải phóng khi tế bào vi khuẩn bị phá hủy. Nội độc tố chỉ có ở vi khuẩn Gram âm, một ngoại lệ duy nhất là Listeria monocytogenes là vi khuẩn Gram dương có nội độc tố.
Trên lâm sàng, khi điều trị cho một bệnh nhân nhiễm khuẩn Gram âm bằng kháng sinh, có thể khiến cho tình trạng bệnh nhân nặng lên do vi khuẩn bị ly giải đồng loạt, giải phóng một lượng lớn nội độc tố.
4. MỘT SỐ KHÁI NIỆM VỀ DƯỢC ĐỘNG HỌC VÀ DƯỢC LỰC HỌC (PK/PD)
4.1. Dược động học (Pharmacokinetics – PK)
Dược động học mô tả quá trình hấp thu, phân bố, chuyển hóa, thải trừ của một thuốc. Các thông số cơ bản đánh giá dược động học của thuốc được mô tả trong bảng dưới đây.
Bảng 21.3: Các thông số dược động học của thuốc
|
Các thông số |
Định nghĩa |
|
Sinh khả dụng |
Là thông số biểu thị lượng thuốc vào được vòng tuần hoàn chung ở dạng còn hoạt tính so với liều đã dùng. Thuốc dùng đường tĩnh mạch có sinh khả dụng 100%, các đường dùng khác có sinh khả dụng thấp hơn. |
|
Cpeak Cmax |
The maximum concentration Nồng độ thuốc tối đa trong máu sau khi dùng một liều đơn độc. |
|
Cmin |
The minimum concentration Nồng độ thuốc tối thiểu trong máu. |
|
Tmax |
Time to Maximum Plasma Concentration Thời gian để đạt nồng độ thuốc tối đa trong máu. |
|
AUC |
Area under the curve Là diện tích dưới đường cong của đồ thị biểu diễn sự biến thiên của nồng độ thuốc trong máu theo thời gian. |
|
t1/2 |
Half – life Là thời gian cần thiết để nồng độ thuốc trong máu giảm đi một nửa. |
|
T > MIC |
Thời gian thuốc có nồng độ lớn hơn MIC trong vòng 24h. |
4.2. Dược lực học (Pharmacodynamics)
Dược lực học (PD) thể hiện mối quan hệ giữa nồng độ và hiệu quả điều trị, trong trường hợp đối với kháng sinh, PD là mối quan hệ giữa nồng độ và hiệu quả diệt khuẩn/kìm khuẩn.
Bảng 21.4: Các thông số dược lực học của thuốc
|
Các thông số |
Định nghĩa |
|
MIC |
Minimum inhibitory concentration Nồng độ tối thiểu của kháng sinh có tác dụng ức chế sự phát triển của vi khuẩn. |
|
PEA |
Post antibiotic effect Tác dụng hậu kháng sinh là khả năng diệt khuẩn kéo dài của một kháng sinh sau khi thuốc đã được loại ra khỏi môi trường in vitro. |
|
PEA – SME |
Post antibiotic effect and postantibiotic sub-MIC effect Tác dụng hậu kháng sinh dưới MIC là khả năng diệt khuẩn kéo dài khi nồng độ thuốc giảm xuống dưới MIC |
4.3. Phân loại kháng sinh
Dựa vào đặc điểm PK/PD, các kháng sinh được chia thành: kháng sinh diệt khuẩn phụ thuộc nồng độ fluoroquinolone, aminoglycoside, kháng sinh diệt khuẩn phụ thuộc thời gian không có hoặc có tác dụng kéo dài ngắn (hầu hết các β-lactam), kháng sinh diệt khuẩn phụ thuộc thời gian có tác dụng kéo dài trung bình hoặc dài như azithromycin.
a. Kháng sinh diệt khuẩn phụ thuộc nồng độ
Với kháng sinh phụ thuộc nồng độ, tổng lượng thuốc được dùng là yếu tố xác định hiệu quả điều trị. Khi một kháng sinh phụ thuộc nồng độ có khả năng đạt tỷ số Cpeak/MIC tối ưu (ví dụ 10:1), thì yếu tố thời gian lúc này không có ý nghĩa, chỉ số Cpeak/MIC chính là yếu tố đánh giá hiệu quả điều trị. Nếu kháng sinh đó không thể đạt được Cpeak/MIC tối ưu, lúc này cần phải xem xét đến cả yếu tố về thời gian, và tỷ số AUC/MIC là yếu tố đánh giá hiệu quả điều trị trong trường hợp này, vì AUC = nồng độ × thời gian. Vì vậy, đối với nhiều kháng sinh không có khả năng đạt Cpeak/MIC tối ưu, AUC/MIC là chỉ số tốt nhất để đánh giá hiệu quả điều trị. Các loại kháng sinh phụ thuộc nồng độ thường dùng gồm: fluoroquinolone, aminoglycoside.
b. Kháng sinh diệt khuẩn phụ thuộc thời gian
Với kháng sinh phụ thuộc thời gian (nhóm kháng sinh β-lactam bao gồm penicillin, cephalosporine, và carbapenem, macrolide), yếu tố xác định hiệu quả là thời gian duy trì nồng độ trên MIC. Một số kháng sinh phụ thuộc thời gian như β-lactam không có hoặc có PAE rất ngắn, trong khi một số kháng sinh phụ thuộc thời gian khác lại có PAE trung bình hoặc dài. Các β-lactam có hoạt phổ rộng trên cả vi khuẩn Gram âm và Gram dương, đạt hiệu quả điều trị cao nhất khi đạt nồng độ khoảng trên 4 lần MIC. Nồng độ cao hơn giá trị này sẽ không làm tăng khả năng diệt khuẩn. Vì vậy, T > MIC là chỉ số tối ưu để đánh giá hiệu quả điều trị của nhóm này.
Với hầu hết các β-lactam, T > MIC đạt ≥ 40 – 50% so với khoảng đưa liều được xem là đạt hiệu quả điều trị. Carbapenem là một phân nhóm của β-lactam (ertapenem, imipenem, meropenem) có một số điểm khác với các β-lactam khác. Với các kháng sinh này, giá trị T > MIC có thể thấp hơn đối với vi khuẩn Gram âm, T > MIC đạt 20% được báo cáo là có tác dụng kìm khuẩn, đạt 40% được báo cáo là có tác dụng diệt khuẩn.
Để đạt T > MIC đạt hiệu quả điều trị có thể tăng liều dùng, rút ngắn khoảng đưa liều, dùng công thức giải phóng thuốc kéo dài hoặc truyền liên tục. Đặc biệt, truyền liên tục có tác dụng tối ưu hóa thời gian điều trị, giảm thiểu sự dao động nồng độ thuốc trong huyết tương.
Với những kháng sinh có PAE dài, thường gặp ở các thuốc có khả năng diệt khuẩn bằng cách ức chế ADN hoặc ức chế tổng hợp protein như fluoroquinolone và clindamycin, số lần đưa thuốc sẽ ít hơn so với số lần được ước tính dựa trên thời gian bán thải.
5. TÁC NHÂN THƯỜNG GẶP GÂY VIÊM NỘI TÂM MẠC NHIỄM KHUẨN
Có rất nhiều loại vi khuẩn có thể gây VNTMNK, tỷ lệ thay đổi theo các quần thể khác nhau.
Ba nguyên nhân gây VNTMNK phổ biến nhất là staphylococcus, streptococcus và enterococcus. Streptococcus là nguyên nhân phổ biến nhất ở nhóm bệnh nhân cao tuổi và VNTMNK mắc phải ở cộng đồng, trong khi staphylococcus là nguyên nhân phổ biến nhất gây VNTMNK ở các nước phát triển và VNTMNK liên quan đến chăm sóc y tế.
Bảng 21.5: Các nguyên nhân gây viêm nội tâm mạc nhiễm khuẩn
|
Tác nhân vi khuẩn |
Tổng (%) |
VNTMNK van tự nhiên (%) |
VNTMNK ở bệnh nhân có các thiết bị cấy ghép (%) |
||
|
Nghiện chích ma túy |
Không nghiện chích ma túy |
Van tim nhân tạo |
ICD, CRT, máy tạo nhịp vĩnh viễn |
||
|
Staphylococcus aureus |
31 |
68 |
28 |
23 |
35 |
|
Staphylococcus có coagulase âm tính |
11 |
3 |
9 |
17 |
26 |
|
Streptococci nhóm viridans |
17 |
10 |
21 |
12 |
8 |
|
Streptococcus bovis |
6 |
1 |
7 |
5 |
3 |
|
Streptococci khác |
6 |
2 |
7 |
5 |
4 |
|
Các chủng Enterococcus |
10 |
5 |
11 |
12 |
6 |
|
HACEK |
2 |
0 |
2 |
2 |
0.5 |
|
Nấm |
2 |
1 |
1 |
4 |
1 |
|
Cấy máu âm tính |
10 |
5 |
9 |
12 |
11 |
|
Nhiều chủng vi khuẩn |
1 |
2 |
1 |
1 |
0 |
|
Khác |
4 |
3 |
4 |
7 |
6 |
(Nguồn: Clinical presentation, etiology, and outcome of infective endocarditis in the 21st century: The International Collaboration on Endocarditis-Prospective Cohort Study)
Các trường hợp VNTMNK cấy máu âm tính chiếm khoảng 10%, bao gồm hai trường hợp: VNTMNK ở bệnh nhân đã sử dụng kháng sinh trước khi chẩn đoán hoặc VNTMNK do chủng vi khuẩn khó nuôi cấy.
Trong trường hợp thứ 2, xét nghiệm huyết thanh học, PCR tổ chức van hoặc máu… có thể giúp xác định căn nguyên trong 60% trường hợp, phần lớn là do các chủng Bartonella, các chủng Brucella, Coxiella burnetii (sốt Q), nhóm HACEK và Tropheryma whipplei.
Bảng 21.6: Các căn nguyên gây viêm nội tâm mạc nhiễm khuẩn thường gặp trên các nhóm bệnh nhân riêng biệt (AHA 2015)
|
Đặc điểm bệnh nhân |
Nguyên nhân thường gặp |
|
Nghiện chích ma túy |
S. aureus Các streptococcus tan máu β Nấm Trực khuẩn Gram âm hiếu khí, bao gồm cả Pseudomonas aeruginosa Nhiễm nhiều chủng vi khuẩn |
|
Có các thiết bị tim mạch cấy ghép |
S. aureus Các tụ cầu coagulase âm tính staphylococcus Nấm Trực khuẩn Gram âm hiếu khí Corynebacterium sp |
|
Bệnh lý đường sinh dục (nhiễm trùng, có thai, đẻ, nạo phá thai) |
Enterococcus sp Các streptococcus nhóm B Listeria monocytogenes Trực khuẩn Gram âm hiếu khí Neisseria gonorrhoeae |
|
Bệnh lý da mạn tính, nhiễm trùng da tái phát nhiều lần |
S. aureus Các streptococcus tan máu β |
|
Bệnh lý răng miệng, tiền sử thực hiện các thủ thuật răng miệng |
Các streptococcus viridan Streptococci khác Abiotrophia defectiva Granulicatella sp Gemella sp HACEK |
|
Nghiện rượu, xơ gan |
Bartonella sp Aeromonas sp Listeria sp S. pneumoniae |
|
Bỏng |
S. aureus Trực khuẩn Gram âm hiếu khí, bao gồm Pseudomonas aeruginosa Nấm |
|
Đái tháo đường |
S. aureus Pseudomonas aeruginosa S. pneumonia |
|
Thay van tim nhân tạo ≤ 1 năm |
Các staphylococcus coagulase âm tính S. aureus Trực khuẩn Gram âm hiếu khí Nấm Corynebacterium sp Legionella sp |
|
Thay van tim nhân tạo > 1 năm |
Coagulase – negative staphylococci S. aureus Viridans group streptococci Enterococcus sp Nấm Corynebacterium sp |
|
Thường tiếp xúc với chó, mèo |
Bartonella sp Pasteurella sp Capnocytophaga sp |
|
Tiếp xúc với sữa bị ô nhiễm hoặc động vật bị nhiễm trùng ở trang trại |
Brucella sp Coxiella burnetii Erysipelothrix sp |
|
Người vô gia cư, có chấy, AIDS |
Bartonella sp Salmonella sp S. pneumoniae S. aureus |
|
Viêm phổi, viêm màng não |
S. pneumoniae |
|
Ghép tạng |
S. aureus Aspergillus fumigatus Enterococcus sp Candida sp |
|
Tổn thương đường tiêu hóa |
S. gallolyticus (bovis) Enterococcus sp Clostridium septicum |
5.1. Streptococcus
- Vi khuẩn Gram dương, xếp chuỗi, kỵ khí tùy ý.
- Phân loại:
- Theo khả năng tan máu: gồm ba nhóm alpha (tan máu một phần), beta (tan máu hoàn toàn), gama (không gây tan máu).
- Theo kháng nguyên Lancefield ở vách tế bào: từ A, B, C, D, E, tới S.
- Ngày nay việc phân loại liên cầu theo kháng nguyên Lancefield ít được áp dụng hơn, mà chủ yếu dựa vào tính chất tan máu, các thành phần kháng nguyên, đặc điểm phát triển, gen.
- Có trên 30 chủng liên cầu, tuy nhiên 5 chủng chính gây bệnh ở người gồm: 3 chủng thuộc nhóm A, B và D; 2 chủng còn lại không có kháng nguyên Lancefield là Streptococcus pneumoniae và các streptococcus nhóm viridan.
- Các streptococcus nhóm viridan, streptococcus bovis là hai nguyên nhân thường gặp nhất trong nhóm liên cầu gây VNTMNK.
- Viridans group streptococci: thực chất là một nhóm gồm nhiều chủng liên cầu, đại đa số thuộc nhóm tan máu alpha.
- Gồm: S. salivarius, S. sanguis, S. mitis, S. intermedius, S. mutans…
- Đây là các chủng vi khuẩn bình thường trong hệ vi khuẩn chí của người ở đường tiêu hóa, vùng hầu họng và khoang miệng.
- Các tổn thương trong khoang miệng có thể khiến các vi khuẩn này đi vào trong máu, bám trên bề mặt nội tâm mạc đặc biệt những vị trí nội mạc đã có tổn thương trước đó.
- Lâm sàng thường biểu hiện diễn biến bán cấp, sốt nhẹ, mệt mỏi, thiếu máu, tiếng thổi mới ở tim.
- Streptococcus bovis:
- Thuộc nhóm liên cầu nhóm D, tan máu alpha. Bao gồm: S. equinus, S. gallolyticus, S. infantarius…
- Sinh sống trong đường tiêu hóa của người thường gây nhiễm khuẩn tiết niệu, nhiễm trùng đường mật và VNTMNK diễn biến bán cấp.
- Lưu ý 50% bệnh nhân nhiễm S. bovis có tổn thương đại tràng ác tính.
5.2. Staphylococcus
Gồm ba chủng chính: Staphylococcus aureus, Staphylococcus epidermidis, Staphylococcus saprophyticus. Staphylococci sinh sống trên da và vùng hầu họng ở 50% số người bình thường. Đây là nhóm cầu khuẩn Gram dương xếp chùm, kỵ khí tùy ý.
- Staphylococcus aureus:
- Có lớp vỏ bao ngoài thành peptidoglycan, có chứa protein gắn penicillin.
- S. aureus có nhiều protein làm vô hiệu hóa hệ miễn dịch của con người: Protein A (ngăn cản quá trình opsonin hóa và thực bào), coagulase (enzyme này giúp tạo lớp fibrin xung quanh vi khuẩn, bảo vệ S. aureus khỏi sự thực bào), hemolysins (phá hủy tế bào hồng cầu, bạch cầu đa nhân trung tính, đại thực bào, tiểu cầu), leukocidins (phá hủy bạch cầu), penicillinase (là một dạng của beta – lactamase, phá hủy vòng beta – lactam làm vô hiệu hóa penicillin.
- Các protein giúp S. aureus đâm xuyên mô: hyaluronidase (giáng hóa proteoglycan trong mô liên kết, staphylokinase (phân hủy fibrin), lipase (giáng hóa mỡ), protease (phân hủy protein mô).
- Các ngoại độc tố: exfoliatin (gây bong da), enterotoxin (gây ngộ độc thực phẩm: nôn, tiêu chảy), TSST – 1 (gây hội chứng sốc nhiễm độc, 20% S. aureus có độc tố này).
- S. aureus có thể gây bệnh ở hầu hết các cơ quan trong cơ thể:
- Bệnh do ngoại độc tố: ngộ độc thực phẩm, tổn thương da (nhọt kèm bong da), hội chứng sốc nhiễm độc.
- Bệnh do vi khuẩn xâm nhập trực tiếp: viêm phổi, viêm màng não, viêm xương khớp, VNTMNK, nhiễm khuẩn tiết niệu.
- MSSA (Methicillin – susceptible Staphylococcus aureus) và MRSA (Methicillin – resistant Staphylococcus aureus):
- Staphylococci tiết ra penicillinase do đó chúng kháng penicillin. Methicillin, nafcillin, oxacillin, cloxacillin, dicloxacillin là các penicillin kháng penicillinase, không bị giáng hóa bởi penicillinase, do đó chúng có khả năng diệt S. aureus.
- Những S. aureus nhạy cảm với các penicillin kháng penicillinase được gọi là MSSA, những S. aureus kháng với các penicillin kháng penicillinase gọi là MRSA.
- MRSA là chủng vi khuẩn đa kháng kháng sinh, là một trong những căn nguyên nhiễm khuẩn bệnh viện hàng đầu.
- VNTMNK do S. aureus: Khởi phát đột ngột, BN sốt cao, rét run, tổn thương van tim tiến triển nhanh, có thể ở những bệnh nhân không có bệnh van tim trước đó. Những bệnh nhân có tiền sử nghiện chích ma túy thường gặp tổn thương van tim bên phải.
- Staphylococcus epidermidis:
- Loại vi khuẩn này là một phần trong hệ vi khuẩn chí bình thường ở người và thường chung sống hòa bình trên da không gây bệnh. Tuy nhiên, ở những bệnh nhân được đặt ống thông tiểu, đường truyền tĩnh mạch … vi khuẩn có thể xâm nhập qua các đường vào trên và gây bệnh.
- Khác với S. aureus, S. epidermidis không có men coagulase.
- S. epidermidis là một trong các loại vi khuẩn đôi khi bị tạp nhiễm khi cấy máu. Do đó, nếu chỉ có một trong các mẫu máu cấy dương tính với S. epidermidis, cần nghi ngờ đây chỉ là tạp nhiễm trên da bệnh nhân. Nếu có từ hai mẫu máu trở lên dương tính, thì khả năng cao bệnh nhân có nhiễm khuẩn huyết do S. epidermidis.
- Trên thực tế, đây là chủng vi khuẩn gây nhiễm khuẩn trên thiết bị nhân tạo thường gặp nhất. Nguyên nhân là do S. epidermidis có lớp vỏ polysaccharide, cho phép vi khuẩn bám dính vào vật liệu nhân tạo.
- Staphylococcus saprophyticus:
- Thường gây nhiễm trùng tiết niệu ở nữ giới có quan hệ tình dục, trong cộng đồng.
- Không có men coagulase.
5.3. Enterococcus
- Trước đây, Enterococcus được xếp vào Streptococcus nhóm D, tan huyết alpha. Tuy nhiên, ngày nay Enterococcus được tách thành nhóm riêng do có quá nhiều điểm khác biệt với Streptococcus.
- Đây là nhóm cầu khuẩn, Gram dương, thường xếp đôi, kỵ khí tùy ý.
- Enterococcus là thành phần của hệ vi khuẩn chí trong đường tiêu hóa của người. Hai chủng phổ biến nhất ở người là E. faecalis và E. faecium.
- Thường gây viêm đường tiết niệu, đường mật, VNTMNK. Thực tế enterococcus là một trong những nguyên nhân hàng đầu gây nhiễm trùng bệnh viện ngày nay.
5.4. HACEK
- HACEK là nhóm trực khuẩn hoặc hình dạng lai giữa cầu khuẩn và trực khuẩn, gram âm, khó nuôi cấy, gồm các trực khuẩn:
- Haemophilus species (H. parainfluenzae, H. aphrophilus, H. paraphrophilus, H. influenzae)
- Actinobacillus actinomycetemcomitans
- Cardiobacterium hominis
- Eikenella corrodens
- Kingella species (K. kingae, K. denitrificans)
- HACEK là vi khuẩn sống hội sinh ở vùng hầu họng. Eikenella và Cardiobacterium được tìm thấy cả ở đường tiêu hóa và đường sinh dục nữ.
- VNTMNK do HACEK thường diễn biến bán cấp trong nhiều tuần. 60% các trường hợp có liên quan với bệnh lý răng miệng. Bên cạnh VNTMNK, những vi khuẩn này còn gây nhiễm trùng vết thương (đặc biệt là những vết thương do bị cắn), áp xe phần mềm, áp xe não, viêm quanh răng…
5.5. Nấm
VNTMNK do nấm rất hiếm chủ yếu ở nhóm bệnh nhân có các thiết bị cấy ghép nhân tạo và tiền sử dùng thuốc đường tĩnh mạch. Candida spp, Aspergillus spp là những nguyên nhân chủ yếu gây VNTMNK do nấm.
Cần nghĩ đến nhiễm nấm ở bệnh nhân có tổn thương sùi lớn.
6. NGUYÊN TẮC ĐIỀU TRỊ KHÁNG SINH
- Điều trị kháng sinh nhằm vào căn nguyên vi khuẩn gây bệnh và mức độ đề kháng của vi khuẩn tại từng cơ sở. Việc chẩn đoán chính xác vi khuẩn gây bệnh rất quan trọng, có ảnh hưởng rất lớn đến diễn biến quá trình điều trị. Yêu cầu lấy máu và/hoặc các bệnh phẩm vô trùng khác để phân lập vi khuẩn trước khi sử dụng kháng sinh. Cần lấy ít nhất 3 mẫu cấy máu tại các vị trí tĩnh mạch khác nhau, mỗi mẫu cách nhau 30 phút.
- Những trường hợp diễn biến bệnh không cấp tính có thể trì hoãn điều trị kháng sinh cho đến khi có kết quả cấy máu. Nếu diễn biến bệnh cấp tính thì cần điều trị kháng sinh ngay. Trong khi chưa có kết quả phân lập vi khuẩn từ máu và/hoặc từ các bệnh phẩm vô trùng khác thì cần phỏng đoán mầm bệnh để điều trị kháng sinh theo kinh nghiệm. Nhìn chung kháng sinh điều trị kinh nghiệm cần bao vây được tụ cầu (cả nhạy và kháng methicillin), phế cầu và các Enterococcus.
- Ưu tiên: Sử dụng kháng sinh diệt khuẩn hơn là kháng sinh kìm khuẩn, dùng đường tĩnh mạch hơn là đường uống và thời gian điều trị kéo dài.
- Thời gian điều trị kháng sinh: ít nhất 4 – 6 tuần đối với VNTMNK trên van tự nhiên và 6 tuần đối với van nhân tạo. Thời gian liệu trình kháng sinh nên được tính từ ngày liệu pháp kháng sinh có hiệu quả. Tức là nếu ban đầu bệnh nhân có kết quả cấy máu dương tính, thời gian liệu trình kháng sinh nên được tính từ ngày kết quả cấy máu chuyển sang âm tính. Sau phẫu thuật, một liệu trình kháng sinh mới đầy đủ chỉ nên áp dụng trong trường hợp bệnh phẩm nuôi cấy van dương tính.
- Theo dõi hiệu quả điều trị kháng sinh dựa trên sự biến đổi các biểu hiện lâm sàng và chỉ dấu sinh học chỉ điểm tình trạng phản ứng viêm. Cần định kỳ cấy máu theo dõi, cách 1 – 2 ngày lại cấy hai mẫu máu cho đến khi kết quả trở về âm tính.
PHẦN II. CÁC THUỐC KHÁNG SINH
1. BENZYLPENICILLIN (PENICILLIN G)
1.1. Lịch sử
- Penicillin được Fleming phân lập từ nấm Penicillium notatum năm 1928 và được Florey, Chain và đồng sự sử dụng trên lâm sàng từ năm 1941. Với đóng góp to lớn này cho y học, Fleming, Florey và Chain đã được trao giải thưởng Nobel năm 1945.
- Ban đầu việc sản xuất penicillin từ lên men nấm cho ra nhiều loại penicillin được đặt theo các chữ cái như F, G, X, K… trong đó penicillin G có hiệu lực cao nhất. Hiện nay penicillin G được sản xuất công nghiệp có độ tinh khiết rất cao. Ngoài dạng muối Na và K có độ hòa tan rất cao còn có procaine benzylpenicillin và benzathine penicillin G duy trì kéo dài nồng độ penicillin trong huyết thanh.
1.2. Dược lực học và dược động học
- Thuốc tác động đến sự tổng hợp vách tế bào vi khuẩn khi vi khuẩn nhân lên khiến cho vi khuẩn không tổng hợp được vách tế bào, dẫn đến chết tế bào vi khuẩn. Hiệu lực diệt khuẩn trên những vi khuẩn nhạy cảm bao gồm cả vi khuẩn Gram dương và Gram âm. Đây là lựa chọn cơ bản để điều trị liên cầu, phế cầu, tụ cầu vàng không sinh penicillinase, vi khuẩn kỵ khí Clostridium perfringens, vi khuẩn giang mai Treponema pallidum và những vi khuẩn ít gặp như Actinomyces sp., vi khuẩn bạch hầu, Enterococcus faecalis, Leptospira sp., P. acnes, P. multocida, Peptostreptococci. Tụ cầu vàng và nhiều vi khuẩn khác có thể sinh penicillinase làm bất hoạt penicillin G.
- Thuốc sử dụng đường tiêm (tiêm bắp sâu, tiêm/truyền tĩnh mạch), đạt nồng độ đỉnh huyết thanh ngay sau tiêm/truyền tĩnh mạch.
- Phân bố: Thuốc ngấm kém qua hàng rào máu não, kể cả trong trường hợp viêm màng não. Tỷ số nồng độ dịch não tủy: máu khi viêm màng não dao động từ 2% đến 6%.
- Thời gian bán thải ở trẻ sơ sinh dưới 6 ngày tuổi là 3,1h, ở trẻ sơ sinh trên 14 ngày tuổi là 1,4h, ở người lớn có chức năng thận bình thường là 31 đến 50 phút, còn ở bệnh thận giai đoạn cuối là từ 6 đến 20h.
- Thải trừ qua nước tiểu có tới 58-85% thuốc ở dạng không biến đổi.
1.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do Enterococcus nhạy penicillin: 18 đến 30 triệu đơn vị/24h truyền liên tục hoặc tiêm cách quãng mỗi 4h, phối hợp gentamicin hoặc streptomycin. Thời gian điều trị 4-6 tuần.
- VNTMNK do Erysipelothrix rhusiopathiae: 12 đến 20 triệu đơn vị/24h tiêm cách quãng mỗi 4-6h trong 4-6 tuần.
- VNTMNK do Listeria monocytogenes: 15 đến 20 triệu đơn vị/24h tiêm cách quãng mỗi 4-6h trong 4 tuần.
- VNTMNK do liên cầu viridans và S. bovis:
- Van tự nhiên: Nếu vi khuẩn nhạy cảm penicillin (MIC ≤ 0,12 μg/mL) dùng 12 đến 18 triệu đơn vị/24h truyền liên tục hoặc tiêm cách quãng mỗi 4-6h trong 4 tuần, hoặc dùng trong 2 tuần khi kết hợp với gentamicin. Nếu vi khuẩn tương đối kháng penicillin (MIC từ 0,12 đến dưới 0,5 μg/ml) dùng 24 triệu đơn vị/24h truyền liên tục hoặc tiêm cách quãng mỗi 4-6 giờ trong 4 tuần, trong đó 2 tuần đầu dùng kết hợp với gentamicin.
- Van nhân tạo: Nếu vi khuẩn nhạy cảm penicillin (MIC ≤ 0,12 μg/ml) dùng 24 triệu đơn vị/24h truyền liên tục hoặc tiêm cách quãng mỗi 4-6 giờ trong 6 tuần (có thể kết hợp với gentamicin trong 2 tuần đầu). Nếu vi khuẩn kháng penicillin (MIC > 0,12 μg/mL) dùng 24 triệu đơn vị/24h truyền liên tục hoặc tiêm cách quãng mỗi 4-6h trong 6 tuần, kết hợp với gentamicin trong 6 tuần.
1.4. Tác dụng phụ và xử trí
- Phản ứng dị ứng:
- Mặc dù có tới 10% người bệnh kể tiền sử dị ứng penicillin nhưng 85-90% số bệnh nhân này không xuất hiện dị ứng khi dùng penicillin. Khi người bệnh tăng bạch cầu đơn nhân nhiễm trùng do virus Epstein-Barr dùng penicillin thì có tới 90% xuất hiện phát ban, nhưng sau đợt bệnh đó dùng lại penicillin thì không xảy ra dị ứng. Khi sử dụng procaine penicillin thì dị ứng cũng có thể do procaine chứ không nhất thiết là do penicillin. Dị ứng chéo giữa penicillin với các cephalosporine và carbapenem vào khoảng 10%.
- Dị ứng nguy hiểm nhất là phản vệ qua trung gian IgE. Mặc dù phản vệ gặp chỉ 0,05% nhưng nguy cơ tử vong tới 5-10%. Các biểu hiện khác cũng qua trung gian IgE là mày đay, phù mạch, phù thanh quản, co thắt phế quản. Phát ban dạng sởi xuất hiện sau 72h không phải qua trung gian IgE và không nghiêm trọng. Những phản ứng dị ứng muộn nghiêm trọng bao gồm thiếu máu huyết tán, giảm bạch cầu trung tính, giảm tiểu cầu, bệnh huyết thanh, viêm thận kẽ, viêm gan, tăng bạch cầu ái toan, sốt do thuốc.
- Nếu người bệnh có tiền sử dị ứng penicillin hoặc thuốc kháng sinh beta-lactam hoặc có tiền sử phản vệ với nhiều dị nguyên khác nhau thì cần test da trước khi dùng penicillin. Giá trị tiên đoán âm tính của test da đối với dị ứng penicillin là 97-99%. Nguy cơ phản ứng toàn thân khi làm test da là dưới 1%.
- Nếu vẫn bắt buộc phải dùng penicillin khi test da dương tính thì cần tiến hành giải mẫn cảm. Pha loãng penicillin, tiêm bắt đầu từ liều 20 đơn vị/0,2 mL tăng dần qua 15 bước cho đến khi lên đến liều 800.000 đơn vị/0,8 mL mà không có phản ứng đáng kể thì giải mẫn cảm thành công. Lưu ý giải mẫn cảm phải tiến hành ở các đơn vị hồi sức cấp cứu có sẵn phương tiện xử trí cấp cứu nếu xuất hiện tình trạng phản vệ. Thận trọng khi dùng penicillin cho người bệnh hen phế quản.
- Nồng độ cao trong dịch não tủy có thể gây co giật. Cần chú ý giảm liều khi suy thận.
- Mức lọc cầu thận > 50 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 10-50 mL/phút: cho dùng 75% liều thông thường.
- Mức lọc cầu thận < 10 mL/phút: cho dùng 20-50% liều thông thường.
- Rối loạn điện giải: Dạng chế phẩm chứa muối Na, K khi dùng liều cao đường tĩnh mạch có thể gây thay đổi nồng độ các muối này trong huyết thanh. Khi liều dùng trên 10 triệu đơn vị cần truyền tĩnh mạch chậm trong hơn 30 phút.
- Penicillin có thể tăng tác dụng chống đông máu của các thuốc kháng vitamin K (ví dụ như acenocoumarol). Do đó khi điều trị penicillin cần lưu ý theo dõi INR để điều chỉnh liều thuốc kháng vitamin K nếu cần.
1.5. Ý nghĩa lâm sàng
- Trong bối cảnh sử dụng kháng sinh có xu hướng lạm dụng và leo thang như hiện nay thì việc chỉ định đúng đắn các kháng sinh cổ điển như penicillin có ý nghĩa hết sức quan trọng.
- Rào cản lớn hạn chế việc sử dụng penicillin chính là nhận thức về nguy cơ dị ứng penicillin. Khai thác chính xác tiền sử dị ứng cùng với việc thử test da penicillin sẽ giúp người thầy thuốc có thêm căn cứ xác đáng để chỉ định kháng sinh này.
- Việc thực hiện y lệnh truyền liên tục cũng như tiêm cách quãng penicillin đòi hỏi cơ sở y tế phải có sự chuẩn bị nhất định về trang thiết bị cũng như nhân lực.
2. GENTAMICIN
2.1. Lịch sử
- Gentamicin được nhóm nghiên cứu của Weinstein phát hiện khi lên men Micromonospora purpurea. Các vi khuẩn Micromonospora sống hoại sinh phổ biến trong đất và nước. Sau khi được tinh chế và sản xuất chế phẩm sử dụng đường tĩnh mạch vào năm 1971, gentamicin đã được sử dụng rộng rãi trên lâm sàng.
- Thực chất gentamicin là hỗn hợp với ba thành phần bao gồm gentamicin C1, gentamicin C2 và gentamicin C1a. Ba thành phần này có sự khác biệt nhỏ về cấu trúc với sự thay thế nguyên tử H và gốc CH3 ở một số vị trí nhưng đều có chung bộ khung giống nhau và khá nhất trí về hiệu lực diệt khuẩn.
2.2. Dược lực học và dược động học
- Gentamicin gắn vào tiểu phần 30S của ribosom gây sai lạc quá trình tổng hợp protein của vi khuẩn. Hiệu lực diệt khuẩn là kết quả của sự tích tụ các peptid vô nghĩa, sự gắn không hồi phục của thuốc với ribosom và quá trình tương tác với màng tế bào vi khuẩn.
- Phổ kháng khuẩn của gentamicin là các vi khuẩn hiếu khí, trong đó chủ yếu là trực khuẩn Gram âm. Thuốc có hiệu lực kém hơn với vi khuẩn Gram dương hiếu khí mặc dù có tác dụng hiệp đồng với kháng sinh tác động đến vách tế bào vi khuẩn. Vi khuẩn nhạy cảm thường là Bartonella sp., Francisella tularensis.
- Thuốc hấp thu nhanh và hoàn toàn sau tiêm bắp. Thời gian đạt đỉnh nồng độ trong huyết thanh là 30-90 phút sau tiêm bắp, 30 phút sau truyền tĩnh mạch.
- Phân bố chủ yếu ở dịch ngoại bào (rất ưa nước) với nồng độ cao ở vỏ thận. Tỷ lệ ngấm vào dịch não tủy và mô mắt rất thấp, kể cả khi dùng đường tĩnh mạch. Tỷ số nồng độ dịch não tủy: máu đối với màng não bình thường là < 10%, khi màng não viêm là ≤ 25%. Tỷ lệ gắn protein huyết thanh là < 30%.
- Thời gian bán thải dao động quanh khoảng 2h. Ở trẻ sơ sinh dưới 1 tuần tuổi thời gian bán thải là 3-11,5h, trên 1 tuần tuổi là 3-6h. Ở trẻ còn bú thời gian bán thải khoảng 4h. Khi suy thận thời gian bán thải kéo dài từ 6-127h.
- Thuốc thải trừ qua thận với > 70% ở dạng không biến đổi. Độ thanh thải giảm khi suy thận.
2.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- Trong VNTMNK, gentamicin được chỉ định sử dụng phối hợp với các kháng sinh khác, thường là với kháng sinh nhóm beta-lactam để tăng cường hiệu quả diệt khuẩn. Thuốc có thể tiêm bắp sâu hoặc pha truyền trong 30-120 phút.
- VNTMNK do Bartonella sp: 3 mg/kg/24h truyền tĩnh mạch 1 lần hoặc có thể chia 3 lần, kết hợp với doxycyclin trong 2 tuần, sau đó duy trì bằng đơn trị liệu doxycyclin.
- VNTMNK do Enterococcus sp: 1 mg/kg/8h tiêm bắp hoặc truyền tĩnh mạch trong phác đồ kết hợp. Thời gian điều trị 4-6 tuần.
- VNTMNK do Staphylococcus sp (van nhân tạo): 1 mg/kg/8h tiêm bắp hoặc truyền tĩnh mạch trong phác đồ kết hợp. Thời gian điều trị 2 tuần đầu, sau đó vẫn duy trì các thành phần kết hợp khác cho đến ít nhất 6 tuần.
- VNTMNK do liên cầu nhóm viridans và S. bovis: 3 mg/kg/24h tiêm bắp hoặc truyền tĩnh mạch 1 lần hoặc có thể chia 3 lần, kết hợp với một beta-lactam. Thời gian điều trị gentamicin là 2 tuần trong những trường hợp van tự nhiên và/hoặc vi khuẩn nhạy penicillin. Riêng trường hợp van nhân tạo với vi khuẩn kháng penicillin (MIC từ 0,12 μg/mL trở lên) thì thời gian điều trị gentamicin là 6 tuần.
- Điều trị theo kinh nghiệm VNTMNK: 1 mg/kg/8h truyền tĩnh mạch, kết hợp với vancomycin (van tự nhiên) hoặc vancomycin và rifampicin (van nhân tạo).
- Giảm liều khi suy thận:
- Mức lọc cầu thận > 50 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 10-50 mL/phút: giãn khoảng cách liều dùng mỗi 12-48h.
- Mức lọc cầu thận < 10 mL/phút: giãn khoảng cách liều dùng mỗi 48-72h.
2.4. Tác dụng phụ và xử trí
- Như các aminoglycosid khác, gentamicin có thể gây hoại tử ống thận và suy thận, điếc do độc thần kinh ốc tai, chóng mặt do tổn thương cơ quan tiền đình và hiếm gặp hơn là liệt do nghẽn dẫn truyền thần kinh cơ. Độc tính thận và ốc tai liên quan đến hiện tượng tích lũy liều nên nguyên tắc chung là tránh dùng liều cao kéo dài và phải giảm liều đối với bệnh nhân suy thận.
- Nguy cơ độc tính trên thận và tai tăng lên khi dùng gentamicin đồng thời với cyclosporine, vancomycin, amphotericin B, thuốc cản quang. Nguy cơ này giảm xuống khi dùng cùng penicillin chống Pseudomonas và sử dụng 1 lần/24h.
- Độc tính ốc tai ban đầu gây thương tổn tế bào lông truyền âm tần số cao nên người bệnh có thể không phát hiện thấy thay đổi gì. Bổ sung aspirin 3g/24h giúp giảm nguy cơ tổn thương ốc tai do gentamicin.
- Độc tính tiền đình có thể gặp nhiều hơn mất nghe nhưng không phát hiện ra do thường xuất hiện đối xứng hai bên. Nếu tổn thương một bên thì chóng mặt, còn nếu tổn thương hai bên thì mất thăng bằng và nhìn mọi thứ quay khi chuyển động đầu. Độc tính tiền đình không liên quan đến liều cũng như thời gian điều trị.
2.5. Ý nghĩa lâm sàng
- Nhiều vi khuẩn đã sinh đề kháng gentamicin ngay từ những năm 1970, cộng với các tác dụng phụ trên thận và tai đã khiến cho có thời gian dài gentamicin không còn được ưa chuộng. Tuy nhiên, việc xuất hiện lại các chủng vi khuẩn ưu thế nhạy cảm gentamicin, cộng với tác dụng hiệp đồng của gentamicin với kháng sinh nhóm beta-lactam đã duy trì vị trí của gentamicin trong các phác đồ điều trị VNTMNK.
- Một trong các căn nguyên vi khuẩn trong các trường hợp VNTMNK cấy máu âm tính có thể là Bartonella sp. Điều này có thể lý giải hiệu quả ngoạn mục của gentamicin khi điều trị những trường hợp VNTMNK cấy máu âm tính.
3. CEFTRIAXONE
3.1. Lịch sử
- Ceftriaxone được cấp bằng sáng chế năm 1978 và được công nhận sử dụng trong y khoa từ năm 1982. Hiện nay ceftriaxone vẫn là thuốc đầu tay trong điều trị theo kinh nghiệm VNTMNK.
- Ceftriaxone là một cephalosporine thế hệ 3, thuộc nhóm kháng sinh beta-lactam.
3.2. Dược lực học và dược động học
- Ceftriaxone có tác dụng với nhiều trực khuẩn Gram âm hiếu khí và liên cầu, phế cầu, não mô cầu cũng như tụ cầu nhạy cảm methicillin (MSSA). Tuy nhiên thuốc không có hiệu quả đối với Listeria sp., Enterococcus faecium, MRSA, trực khuẩn mủ xanh P. aeruginosa và B. fragilis. Tương tự như các thuốc khác trong nhóm beta-lactam, cơ chế tác dụng của ceftriaxone là gắn vào protein gắn penicillin (PBP) dẫn đến ức chế tổng hợp peptidoglycan của vách tế bào vi khuẩn, hậu quả là vi khuẩn không tổng hợp được vách sẽ bị ly giải. Ceftriaxone dễ dàng bị bất hoạt bởi các enzyme beta-lactamase phổ rộng (ESBL) và cephalosporinase nhiễm sắc thể.
- Thuốc hấp thu tốt sau tiêm bắp. Thời gian đạt nồng độ đỉnh trong huyết thanh sau tiêm bắp là 2-3h.
- Thuốc phân bố rộng rãi trong các mô cơ thể kể cả túi mật, dịch mật, phổi, xương, dịch não tủy. Tỉ lệ gắn protein cao tới 85-95%.
- Thời gian bán thải ở người lớn có chức năng gan thận bình thường là 5-9h, ở trẻ em là 4-6,6h còn ở trẻ sơ sinh 1-4 ngày là 16h, trẻ sơ sinh 9-30 ngày là 9h. Ở người lớn suy thận thời gian bán thải là 12-16h.
- Thuốc thải trừ qua nước tiểu (33-67% ở dạng không biến đổi) và phân (dưới dạng thuốc không còn hoạt tính).
3.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do liên cầu nhóm viridans và S. bovis: 2 g/24h, truyền tĩnh mạch hoặc tiêm bắp 1 lần/24h. Đối với các chủng nhạy cảm penicillin (MIC ≤ 0,125 μg/mL) thì dùng đơn trị liệu trong 4 tuần hoặc phối hợp với gentamicin hoặc neltimicin điều trị trong 2 tuần. Đối với các chủng đề kháng penicillin (MIC 0,25 – 2 μg/mL) thì điều trị 4 tuần, trong đó 2 tuần đầu phối hợp với gentamicin.
- VNTMNK do Granulicatella và Abiotrophia: 2 g/24h truyền tĩnh mạch hoặc tiêm bắp 1 lần/24h, điều trị trong 6 tuần, trong đó 2 tuần đầu kết hợp với gentamicin hoặc neltimicin.
- VNTMNK do Enterococcus faecalis còn nhạy cảm penicillin: 4 g/24h truyền tĩnh mạch hoặc tiêm bắp chia 2 lần, kết hợp với ampicillin, điều trị trong 6 tuần. Đây là kết hợp hiệp đồng hai thuốc ức chế tổng hợp vách vi khuẩn để điều trị những chủng còn nhạy cảm với beta-lactam.
- VNTMNK do các vi khuẩn HACEK (Haemophilus, Aggregatibacter/Actinobacillus, Cardiobacterium, Eikenella, Kingella): 2 g/24h truyền tĩnh mạch hoặc tiêm bắp 1 lần/24h trong 4 tuần (van tự nhiên) hoặc 6 tuần (van nhân tạo).
- Điều trị theo kinh nghiệm cho VNTMNK trên van tự nhiên: 2g/24h truyền tĩnh mạch, kết hợp với vancomycin.
- Lưu ý không dùng ceftriaxone cho trẻ sơ sinh tăng bilirubin do thuốc có tỷ lệ gắn protein cao sẽ làm trầm trọng thêm tình trạng tăng bilirubin.
- Thuốc không phải điều chỉnh liều khi suy thận. Tuy nhiên, khi dùng cho bệnh nhân đồng thời suy gan và suy thận thì liều dùng hằng ngày không nên vượt quá 2 g.
- Ceftriaxone không tương hợp với canxi gây kết tủa. Do có những báo cáo tổn thương phổi và thận gây tử vong liên quan kết tủa canxi-ceftriaxone ở trẻ sơ sinh, không được sử dụng các dung dịch có chứa canxi (ví dụ như Ringer lactat) để pha hoặc truyền cùng ceftriaxone.
3.4. Tác dụng phụ và xử trí
- Giả sỏi mật do bùn túi mật: chủ yếu phát hiện trên siêu âm mà ít có biểu hiện lâm sàng. Nguy cơ xuất hiện khi dùng ≥ 2 g/24h ở bệnh nhân không ăn, nuôi dưỡng tĩnh mạch.
- Dùng đồng thời lansoprazole gây kéo dài khoảng QTc.
3.5. Ý nghĩa lâm sàng
- Do đặc điểm phân bố tốt tới các mô, không phải điều chỉnh liều khi suy thận, chỉ phải dùng 1-2 lần/24h và phổ kháng khuẩn bao phủ được nhiều loại vi khuẩn thường gặp trong VNTMNK, ceftriaxone hay được lựa chọn để điều trị theo kinh nghiệm cũng như điều trị đặc hiệu sau khi phân lập được mầm bệnh.
4. AMPICILLIN
4.1. Lịch sử
- Ampicillin là kháng sinh penicillin bán tổng hợp được khám phá năm 1958 và đưa ra thị trường từ năm 1961. Đây là một trong các kháng sinh hiện vẫn còn sử dụng với giá thành điều trị rất thấp.
4.2. Dược lực học và dược động học
- Thuốc tác dụng chủ yếu trên các liên cầu, phần lớn các Enterococcus, Listeria, Clostridium và một số các vi khuẩn kỵ khí khác. Là một aminopenicillin, cơ chế tác dụng của ampicillin tương tự như của các kháng sinh khác thuộc nhóm beta-lactam là ức chế tổng hợp vách vi khuẩn.
- Sinh khả dụng đường uống chỉ khoảng 50% nên thuốc chủ yếu sử dụng đường tiêm tĩnh mạch.
- Phân bố được vào dịch mật. Trường hợp màng não viêm thuốc phân bố được vào dịch não tủy với tỷ số nồng độ dịch não tủy/máu 13-14%.
- Thời gian bán thải từ 1-1,8h. Ở bệnh nhân vô niệu thời gian này là 8-20h, còn ở trẻ sơ sinh 2-7 ngày tuổi thời gian bán thải là 4h, 8-14 ngày tuổi thời gian bán thải là 2,8h.
- Thuốc thải trừ qua nước tiểu (khoảng 90% dưới dạng không biến đổi trong vòng 24h) và phân.
4.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do Enterococcus faecalis còn nhạy cảm penicillin: 2g mỗi 4h tiêm tĩnh mạch, phối hợp với ceftriaxon hoặc gentamicin. Thời gian điều trị thường là 6 tuần. Nếu van tự nhiên và triệu chứng dưới 3 tháng thì điều trị kết hợp ampicillin và gentamicin có thể chỉ cần 4 tuần. Lựa chọn kết hợp ampicillin với ceftriaxon được ưu tiên hơn cho những bệnh nhân có nguy cơ suy thận.
- VNTMNK do các vi khuẩn HACEK (Haemophilus, Aggregatibacter/Actinobacillus, Cardiobacterium, Eikenella, Kingella): 2g mỗi 4h tiêm tĩnh mạch trong 4 tuần (van tự nhiên) hoặc 6 tuần (van nhân tạo).
- VNTMNK do liên cầu nhóm viridans và S. bovis: 2 g mỗi 4h tiêm tĩnh mạch. Đối với van tự nhiên, vi khuẩn rất nhạy penicillin (MIC ≤ 0,12 μg/ml) thì điều trị trong 4 tuần, còn vi khuẩn tương đối đề kháng penicillin (MIC từ 0,12-0,5 μg/mL) thì cũng điều trị trong 4 tuần nhưng kết hợp gentamicin trong 2 tuần đầu. Đối với van nhân tạo, vi khuẩn rất nhạy penicillin (MIC < 0,12 μg/mL) thì điều trị trong 6 tuần, còn khi vi khuẩn tương đối đề kháng penicillin (MIC từ 0,12-0,5 μg/mL) thì điều trị kết hợp với gentamicin trong 6 tuần.
- Điều chỉnh liều dùng khi suy thận:
- Mức lọc cầu thận > 50 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 30-50 mL/phút: giãn khoảng cách liều dùng mỗi 6h.
- Mức lọc cầu thận 10-30 mL/phút: giãn khoảng cách liều dùng mỗi 8h.
- Mức lọc cầu thận < 10 mL/phút: giãn khoảng cách liều dùng mỗi 12h.
4.4. Tác dụng phụ và xử trí
- Phát ban dát sẩn, tiêu chảy, tăng bạch cầu ái toan là những biểu hiện hay gặp khi điều trị ampicillin liều cao kéo dài. Đôi khi xuất hiện sốt kèm theo giảm bạch cầu trung tính mà trên lâm sàng rất khó phân biệt với triệu chứng của chính VNTMNK.
- Khi dùng đồng thời allopurinol thì tăng nguy cơ phát ban.
4.5. Ý nghĩa lâm sàng
- Cũng như penicillin G, điều trị ampicillin chi phí thấp nhưng đòi hỏi đầu tư nhân lực để đảm bảo yêu cầu tiêm thuốc nhiều lần trong ngày.
- Đối với những mầm bệnh đặc biệt như Actinomyces, Listeria, Enterococcus thì hiện nay kháng sinh cổ điển ampicillin vẫn là thuốc lựa chọn đầu tay.
5. OXACILLIN
5.1. Lịch sử
- Đây là kháng sinh thuộc nhóm isoxazolyl penicillin có đặc điểm đề kháng với beta-lactamase của tụ cầu. Thuốc được đăng ký bằng sáng chế từ năm 1960 và được sử dụng tập trung để điều trị tụ cầu từ năm 1962. Methicillin cũng là penicillin bán tổng hợp nhưng không còn dùng trên lâm sàng do độc tính mà chỉ dùng trong lĩnh vực xét nghiệm mức độ nhạy cảm của tụ cầu.
5.2. Dược lực học và dược động học
- Phổ kháng khuẩn của thuốc là tụ cầu vàng nhạy cảm với methicillin (MSSA), S. epidermidis, S. lugdunensis và các tụ cầu không sinh coagulase còn nhạy cảm. Ngoài ra thuốc cũng có tác dụng với phế cầu và liên cầu. Cơ chế tác dụng cũng là ức chế tổng hợp vách vi khuẩn như các thuốc beta-lactam khác.
- Nồng độ đỉnh huyết thanh đạt được sau tiêm bắp 30 phút, sau tiêm tĩnh mạch 5 phút.
- Phân bố được tới dịch mật, nước ối và dịch màng phổi, nhưng chỉ đạt được nồng độ không đáng kể trong dịch não tủy và thủy dịch của mắt. Gắn protein huyết thanh tới 94% (chủ yếu gắn albumin).
- Thời gian bán thải 20-30 phút, kéo dài khi suy thận. Ở trẻ sơ sinh 8-15 ngày, thời gian này là 1,6h còn ở trẻ nhỏ dưới 2 tuổi thời gian bán thải là 0,9-1,8h.
- Thuốc chuyển hóa qua gan và thải trừ qua nước tiểu và dịch mật (dưới dạng thuốc không biến đổi).
5.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do tụ cầu vàng nhạy methicillin (MSSA): 12 g/24h tiêm tĩnh mạch chậm hoặc truyền tĩnh mạch. Đối với van tự nhiên chia đều 4-6 lần/24h dùng trong 2 tuần nếu tổn thương tim phải không biến chứng, trong 6 tuần nếu tổn thương tim phải có biến chứng hoặc tổn thương tim trái. Đối với van nhân tạo chia đều 6 lần/24h điều trị kết hợp với rifampicin trong ít nhất 6 tuần, trong đó 2 tuần đầu kết hợp thêm với gentamicin.
- Không nên sử dụng oxacillin cho những trường hợp vi khuẩn nhạy cảm có thể điều trị được bằng penicillin G hoặc ampicillin.
5.4. Tác dụng phụ và xử trí
- Nên tiêm chậm (trong vòng 30 phút) trên đường truyền có sẵn để giảm thiểu nguy cơ viêm tĩnh mạch quanh vị trí tiêm truyền.
- Dùng liều cao có thể xuất hiện tổn thương gan. Men gan thường tăng sau điều trị vài ngày và giảm xuống sau khi ngừng điều trị.
5.5. Ý nghĩa lâm sàng
- Do methicillin gắn liền với tụ cầu như một chỉ điểm nhạy cảm kháng sinh, nhiều thầy thuốc ưa dùng oxacillin hơn các beta-lactam khác để điều trị tụ cầu. Tuy vậy trên lâm sàng còn nhiều lựa chọn beta-lactam thay thế khác cho oxacillin, ví dụ như các cephalosporine.
6. CEFAZOLIN
6.1. Lịch sử
- Cefazoline là kháng sinh cephalosporine thế hệ 1 đăng ký bằng sáng chế từ năm 1967 và lưu hành thị trường từ năm 1971.
6.2. Dược lực học và dược động học
- Phổ kháng khuẩn chủ yếu là các cầu khuẩn Gram dương như tụ cầu, liên cầu (không tác dụng với MRSA và các Enterococcus) nhưng thuốc cũng có tác dụng đối với một số trực khuẩn Gram âm như Escherichia coli, Proteus mirabilis và Klebsiella sp. Cơ chế tác dụng ngăn chặn quá trình tổng hợp vách của vi khuẩn khiến vi khuẩn ly giải.
- Thuốc dùng đường tiêm với thời gian đạt nồng độ đỉnh huyết thanh sau tiêm bắp 0,5-2h, sau tiêm tĩnh mạch 5 phút.
- Thuốc phân bố tốt đến nhiều mô cơ thể như túi mật, gan, thận, xương, đờm, dịch mật, dịch màng phổi và dịch khớp. Tuy nhiên ngấm dịch não tủy kém.
- Thời gian bán thải 1,8-2h, kéo dài khi suy thận. Ở trẻ sơ sinh thời gian này là 3 đến 5h.
- Thải trừ qua nước tiểu với 70-80% là ở dạng không biến đổi.
6.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do tụ cầu nhạy cảm methicillin: 2g mỗi 8h tiêm tĩnh mạch chậm hoặc truyền tĩnh mạch. Đối với van tự nhiên điều trị trong 6 tuần. Trường hợp van nhân tạo điều trị kết hợp rifampicin trong ít nhất 6 tuần, trong đó 2 tuần đầu kết hợp thêm gentamicin.
- Không nên dùng cefazoline khi đồng thời cũng có nhiễm trùng hệ thần kinh trung ương (ví dụ áp xe não).
- Điều chỉnh liều dùng khi suy thận:
- Mức lọc cầu thận > 50 mL/phút: không cần điều chỉnh liều
- Mức lọc cầu thận 10-50 mL/phút: giãn khoảng cách liều dùng mỗi 12h
- Mức lọc cầu thận < 10 mL/phút: giãn khoảng cách liều dùng mỗi 24h
6.4. Tác dụng phụ và xử trí
- Cefazoline không có cùng chuỗi nhánh với các kháng sinh beta-lactam khác nên nguy cơ dị ứng chéo với penicillin cũng như các beta-lactam khác là rất thấp.
6.5. Ý nghĩa lâm sàng
- Đối với VNTMNK do tụ cầu nhạy cảm methicillin không có di bệnh hệ thần kinh trung ương thì cefazoline là một lựa chọn hợp lý. Khả năng sẵn có cefazoline còn được tăng thêm khi thuốc được sử dụng rộng rãi trong điều trị dự phòng phẫu thuật. Khoảng cách 8h giữa các lần dùng thuốc giúp đảm bảo việc thực hiện thuốc dễ dàng hơn trong điều kiện nguồn lực hạn chế.
7. PIPERACILLIN/TAZOBACTAM
7.1. Lịch sử
- Piperacillin/tazobactam là kết hợp giữa beta-lactam và thuốc ức chế beta-lactamase với tỷ lệ 8:1. Kết hợp này lần đầu tiên được đăng ký vào năm 1993. Tuy nhiên, piperacillin là một aminobenzyl penicillin đã được đăng ký bằng sáng chế từ năm 1974 và sử dụng trong y khoa từ năm 1981. Hiện nay piperacillin hầu như không còn sử dụng đơn độc nữa mà chỉ có mặt trong dạng kết hợp với tazobactam.
- Cấu trúc mang chuỗi nhánh phân cực làm cho piperacillin dễ ngấm vào trong vi khuẩn Gram âm và giảm khả năng phá hủy bởi enzyme beta-lactamase của vi khuẩn Gram âm. Nhờ đặc điểm này mà thuốc có tác dụng mạnh đối với trực khuẩn mủ xanh Pseudomonas aeruginosa nên còn được gọi là “penicillin chống trực khuẩn mủ xanh”.
7.2. Dược lực học và dược động học
- Cũng như các beta-lactam khác, piperacillin ức chế tổng hợp vách vi khuẩn do gắn với PBP nhưng với ái lực cao nên hoạt phổ được mở rộng hơn. Hoạt phổ của piperacillin rất rộng với nhiều loại trực khuẩn Gram âm hiếu khí, trong đó có trực khuẩn mủ xanh. Tazobactam hình thành phức ổn định với các beta-lactamase nhóm A của Ambler giúp bảo vệ piperacillin khỏi sự tấn công của các beta-lactamases từ MSSA, H. influenzae, M. catarrhalis và B. fragilis.
- Sinh khả dụng sau tiêm bắp của piperacillin đạt 71% và của tazobactam đạt 84%. Nồng độ đỉnh huyết thanh đạt được 30 phút sau truyền tĩnh mạch.
- Thuốc phân bố tốt đến các mô phổi, niêm mạc ruột, tử cung, buồng trứng, vòi trứng, dịch kẽ, túi mật và dịch mật nhưng ngấm kém vào dịch não tủy. Tỷ lệ gắn protein thấp (30%).
- Thời gian bán thải của piperacillin là 0,7-1,2h, còn của tazobactam là 0,7-0,9h. Thời gian bán thải của piperacillin tăng 2 lần và của tazobactam tăng 4 lần ở bệnh nhân có mức lọc cầu thận < 20 mL/phút.
- Piperacillin thải trừ qua nước tiểu (68% dưới dạng thuốc không biến đổi) và phân (10-20%) còn tazobactam thải trừ qua nước tiểu (80% dưới dạng thuốc không biến đổi).
7.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do trực khuẩn Gram âm: 4,5 g piperacillin/tazobactam truyền tĩnh mạch cách 6h, phối hợp với tobramycin, thời gian điều trị ít nhất 6 tuần. Thông thường truyền tĩnh mạch trong 30 phút nhưng cũng có thể truyền kéo dài 4h để tăng cường tối ưu hiệu quả dược động học/dược lực học.
- Không nên dùng piperacillin/tazobactam cho những trường hợp trực khuẩn Gram âm hiếu khí sinh beta-lactamase phổ rộng (ESBL).
- Điều chỉnh liều khi suy thận:
- Mức lọc cầu thận > 40 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 20-40 mL/phút: giảm còn 3,375 g mỗi 6h.
- Mức lọc cầu thận < 20 mL/phút: giảm còn 2,25 g mỗi 6h.
Nếu truyền kéo dài thì khi mức lọc cầu thận < 20 mL/phút, cứ cách 12h lại truyền tĩnh mạch 3,375 g trong 4h.
7.4. Tác dụng phụ và xử trí
- Cũng như các kháng sinh beta-lactam, khi sử dụng penicillin/tazobactam có thể xuất hiện phản ứng dị ứng cũng như các tác dụng không mong muốn như sốt, phát ban, buồn nôn/nôn, tiêu chảy, đau đầu, giảm bạch cầu trung tính, tăng bạch cầu ái toan, giảm tiểu cầu, tăng men gan…
- Một số nghiên cứu quan sát cho thấy dường như nguy cơ tổn thương thận cấp tăng lên khi dùng piperacillin/tazobactam. Tuy nhiên, bằng chứng còn chưa chắc chắn và hiện còn chưa rõ cơ chế gì có thể làm tăng nguy cơ tổn thương thận.
- Khi dùng đồng thời methotrexat thì làm tăng nồng độ methotrexat.
7.5. Ý nghĩa lâm sàng
- Mặc dù tazobactam là thuốc ức chế beta-lactamase mạnh hơn sulbactam, nhưng việc bổ sung tazobactam không làm tăng hoạt tính chống trực khuẩn mủ xanh của piperacillin.
- Xu hướng sử dụng kháng sinh xuống thang và điều trị bao vây hiện nay đã làm lu mờ vị trí vốn có của piperacillin/tazobactam trong danh sách các kháng sinh nhằm vào trực khuẩn mủ xanh nói riêng cũng như trực khuẩn Gram âm nói chung.
8. CEFEPIME
8.1. Lịch sử
- Được coi là thuốc đại diện cho kháng sinh cephalosporine thế hệ 4, cefepime được đăng ký bằng sáng chế năm 1982 và được công nhận dùng trong lĩnh vực y học từ năm 1994.
8.2. Dược lực học và dược động học
- Cấu trúc phân tử oxyimino beta-lactam với chuỗi nhánh amino thiazolin cho phép cefepime xuyên thấm tốt và nhanh hơn qua thành tế bào trực khuẩn Gram âm hiếu khí. Hoạt phổ kháng khuẩn của cefepime rất rộng, bao gồm MSSA (mạnh hơn các cephalosporine thế hệ 3), Neisseria sp., H. influenzae và một loạt các trực khuẩn Gram âm, trong đó có trực khuẩn mủ xanh P. aeruginosa.
- Cefepime có thể có tác dụng với trực khuẩn Gram âm hiếu khí sinh ESBL nếu dùng liều cao (2g mỗi 8h). Tuy nhiên, đây không phải là kháng sinh lựa chọn cho trực khuẩn Gram âm sinh ESBL.
- Cefepime bền vững với phần lớn beta-lactamase, nhất là các enzyme AmpC nhiễm sắc thể và qua trung gian plasmid của vi khuẩn Gram âm.
- Thuốc hấp thu nhanh và hoàn toàn sau tiêm bắp. Thời gian đạt nồng độ đỉnh huyết thanh là 1-2h sau tiêm bắp, 0,5h sau truyền tĩnh mạch.
- Thuốc phân bố trong dịch viêm với nồng độ ~80% nồng độ huyết thanh, trong niêm mạc phế quản với nồng độ ~60% nồng độ huyết tương và qua được hàng rào máu não. Thuốc ít gắn protein (20%) và được chuyển hóa tối thiểu ở gan.
- Thời gian bán thải là 2h, ở trẻ sơ sinh thời gian này là 4-5h. Ở bệnh nhân chạy thận nhân tạo, thời gian bán thải là 13,5h.
- Thuốc thải trừ qua nước tiểu (85% ở dạng thuốc không biến đổi).
8.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do trực khuẩn Gram âm: 2g cách 8h truyền tĩnh mạch trong 30 phút, kết hợp với tobramycin. Thời gian điều trị ít nhất 6 tuần.
- Điều chỉnh liều khi suy thận:
- Mức lọc cầu thận > 60 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 30-60 mL/phút: giãn khoảng cách liều mỗi 12h.
- Mức lọc cầu thận 11-29 mL/phút: giãn khoảng cách liều mỗi 24h.
- Mức lọc cầu thận <11 mL/phút: giảm liều mỗi lần xuống 1g và giãn khoảng cách liều mỗi 24h.
8.4. Tác dụng phụ và xử trí
- Các tác dụng phụ thường gặp giống như các kháng sinh beta-lactam khác như phát ban, tiêu chảy, đau đầu, buồn nôn/nôn, giảm bạch cầu trung tính,tăng bạch cầu ái toan, giảm tiểu cầu, tăng men gan…
- Đã có báo cáo hội chứng người đỏ khi dùng cefepime.
- FDA cảnh báo nguy cơ trạng thái động kinh không có cơn giật (non-convulsive status epilepticus) khi dùng cefepime. Suy giảm chức năng thận là yếu tố nguy cơ. Cơ chế là do thuốc ức chế cạnh tranh hệ dẫn truyền GABA. Biểu hiện bao gồm lú lẫn, mất tập trung, rối loạn định hướng, bất thường hành vi, kích động, ảo giác, rung giật cơ, thất ngôn, suy giảm ý thức và hôn mê. Chẩn đoán tình trạng này dựa vào thay đổi trên điện não đồ.
8.5. Ý nghĩa lâm sàng
- Mặc dù có hiệu lực mạnh trên vi khuẩn Gram âm nhưng cefepime không phải là lựa chọn cho vi khuẩn Gram âm sinh ESBL. Điều này khiến cho vai trò của cefepime trong thực hành lâm sàng bị thu hẹp lại nhiều.
9. MEROPENEM
9.1. Lịch sử
- Meropenem là kháng sinh nhóm carbapenem được đăng ký bằng sáng chế năm 1983 và công nhận sử dụng trong lĩnh vực y từ năm 1996.
- Với hiệu quả vượt trội so với các kháng sinh khác về hoạt phổ diệt khuẩn, meropenem được sử dụng ngày càng rộng rãi, nhất là trong lĩnh vực hồi sức.
9.2. Dược lực học và dược động học
- Meropenem là kháng sinh diệt khuẩn nhanh và mạnh. So với imipenem là kháng sinh cùng nhóm carbapenem, meropenem có tác dụng mạnh hơn đối với trực khuẩn Gram âm nhưng lại kém hơn về cầu khuẩn Gram dương. Hoạt phổ của meropenem bao gồm trực khuẩn Gram âm cả hiếu khí và kỵ khí, trong đó có trực khuẩn Gram âm hiếu khí sinh beta-lactamase phổ rộng (ESBL). Cũng như các kháng sinh beta-lactam khác, cơ chế tác dụng của meropenem là gắn với protein, gắn penicillin gây ức chế tổng hợp vách vi khuẩn dẫn đến vi khuẩn bị ly giải.
- Thuốc phân bố tốt đến phần lớn các mô và dịch cơ thể bao gồm đường tiết niệu, dịch màng bụng, xương, dịch mật, phổi, niêm mạc phế quản, mô cơ, van tim và dịch não tủy. Ngoại trừ ở dịch mật, phổi và cơ, thuốc đạt nồng độ đỉnh tại mô khoảng 1h sau khi truyền tĩnh mạch. Trong trường hợp màng não viêm, thuốc đạt nồng độ đỉnh trong dịch não tủy 2-3 giờ sau truyền.
- Thuốc rất ít gắn protein (2%). Chuyển hóa tại gan thủy phân mở vòng beta-lactam để thuốc chuyển thành dạng không còn hoạt tính.
- Thời gian bán thải là 1h. Ở trẻ 3 tháng-2 tuổi thời gian này là 1,5h. Ở trẻ sơ sinh và trẻ ≤ 3 tháng tuổi, thời gian bán thải là 2,7h.
- Thuốc thải trừ qua nước tiểu (70% dưới dạng thuốc không biến đổi, 28% dưới dạng chất chuyển hóa không còn hoạt tính) và phân (2%). Độ thanh thải thuốc giảm tỷ lệ với mức lọc cầu thận ở bệnh nhân suy giảm chức năng thận.
9.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do trực khuẩn Gram âm: 1g cách 8h truyền tĩnh mạch trong 30 phút, kết hợp với tobramycin. Thời gian điều trị ít nhất 6 tuần.
- Điều chỉnh liều dùng khi suy thận:
- Mức lọc cầu thận > 50 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 26-50 mL/phút: giãn khoảng cách liều mỗi 12h.
- Mức lọc cầu thận 10-25 mL/phút: giảm nửa liều và giãn khoảng cách liều mỗi 12h.
- Mức lọc cầu thận < 10 ml/phút: giảm nửa liều và giãn khoảng cách liều mỗi 24h.
9.4. Tác dụng phụ và xử trí
- Nguy cơ co giật thấp hơn imipenem. Khi dùng cùng thuốc chống co giật, acid valproic, meropenem làm giảm nồng độ của acid valproic nên tránh dùng đồng thời hai thuốc này.
- Cũng như nhiều thuốc khác thuộc nhóm beta-lactam, meropenem có nguy cơ dị ứng chéo với penicillin.
- Các tác dụng phụ hay gặp bao gồm tiêu chảy, buồn nôn/nôn, tăng men gan, đau đầu, phản ứng quá mẫn, giảm bạch cầu trung tính, tăng bạch cầu ái toan, giảm tiểu cầu.
9.5. Ý nghĩa lâm sàng
- Với hoạt phổ rất rộng và cách dùng không quá phức tạp, meropenem đang được sử dụng hết sức rộng rãi trên lâm sàng, nhất là ở các đơn vị hồi sức. Tuy nhiên ở bệnh nhân nhiễm khuẩn nặng, thể tích phân bố thường tăng cao dẫn đến nguy cơ nồng độ thuốc giảm hơn so với đối tượng người tình nguyện khỏe mạnh.
- Cần sử dụng hợp lý meropenem để hạn chế nguy cơ đề kháng thuốc, giúp bảo tồn tính hiệu quả của thuốc trong tương lai. Bên cạnh việc chỉ định hợp lý, cần lưu ý tối ưu hóa liều dùng và cách dùng (ví dụ như truyền tĩnh mạch liên tục) nhằm đảm bảo duy trì thời gian nồng độ thuốc trong huyết tương trên nồng độ ức chế tối thiểu (t > MIC).
10. TOBRAMYCIN
10.1. Lịch sử
- Tobramycin là kháng sinh aminoglycosid bắt nguồn từ nấm Streptomyces tenebrarius. Thuốc được đăng ký bằng sáng chế năm 1965 và đưa vào sử dụng trong lĩnh vực y năm 1974.
- So với gentamicin, tobramycin có hoạt tính kháng trực khuẩn mủ xanh Pseudomonas aeruginosa mạnh hơn, tác dụng trên những chủng P. aeruginosa và Acinetobacter baumannii kháng gentamicin và ít độc tính hơn.
10.2. Dược lực học và dược động học
- Cơ chế tác dụng của tobramycin là gắn vào ribosome 30S và 50S của vi khuẩn, ngăn ngừa hình thành phức 70S khiến mARN không thể dịch mã thành protein và gây chết tế bào. Phổ kháng khuẩn của tobramycin chủ yếu là các trực khuẩn Gram âm hiếu khí, trong đó có trực khuẩn mủ xanh.
- Thuốc hấp thu nhanh và hoàn toàn sau tiêm bắp. Thời gian đạt nồng độ đỉnh huyết thanh sau tiêm bắp là 30-60 phút, sau truyền tĩnh mạch là 30 phút.
- Thuốc phân bố vào dịch ngoại bào, bao gồm huyết thanh, dịch áp xe, dịch cổ trướng, dịch màng ngoài tim, dịch màng phổi, dịch khớp, bạch huyết và dịch màng bụng. Ngấm kém vào dịch não tủy, mắt, xương, tuyến tiền liệt. Tỷ lệ gắn protein dưới 30%.
- Thời gian bán thải phụ thuộc trực tiếp mức lọc cầu thận. Thông thường là 2-3h nhưng khi suy thận kéo dài tới 5-70 giờ. Ở trẻ sơ sinh thời gian bán thải 2-9h, còn ở trẻ nhỏ thời gian này là 1-5h.
- Thuốc thải trừ qua nước tiểu (90-95%). Độ thanh thải giảm khi suy thận.
10.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do trực khuẩn Gram âm: Liều tải đầu tiên 5-7 mg/kg truyền tĩnh mạch (60 phút), sau đó 1,5-2 mg/kg truyền tĩnh mạch (20-60 phút) cách 8h, phối hợp với một beta-lactam như cefepim, meropenem hoặc piperacillin/tazobactam. Thời gian điều trị ít nhất 6 tuần.
- Nếu theo dõi được nồng độ tobramycin huyết thanh thì điều chỉnh để nồng độ đỉnh 4-10 μg/mL, nồng độ đáy 1-2 μg/mL.
- Điều chỉnh liều dùng khi suy thận:
- Mức lọc cầu thận > 60 mL/phút: không cần điều chỉnh liều.
- Mức lọc cầu thận 40-60 mL/phút: giãn khoảng cách liều mỗi 12h.
- Mức lọc cầu thận 20-39 mL/phút: giãn khoảng cách liều mỗi 24h.
- Mức lọc cầu thận < 20 mL/phút: cho liều tải, sau đó theo dõi nồng độ huyết thanh để điều chỉnh liều tiếp theo.
10.4. Tác dụng phụ và xử trí
- Nguy cơ độc tính trên thận, ốc tai và cơ quan tiền đình như đối với các aminoglycosid. Hiện tại chưa có biện pháp nào giúp loại bỏ nguy cơ độc với thận và tai của aminoglycosid. Chỉ định điều trị đúng đắn, tính toán liều dùng nghiêm túc và theo dõi chức năng thận trong quá trình điều trị giúp giảm được nguy cơ này. Nếu có điều kiện thì theo dõi nồng độ thuốc trong huyết thanh giúp điều chỉnh liều sát hợp hơn.
- Nguy cơ độc với thận tăng lên khi dùng cùng các thuốc: amphotericin B, cis platinum, cyclosporin, thuốc chống viêm không steroid, thuốc cản quang, vancomycin.
- Nguy cơ độc với tai tăng lên khi dùng cùng: cis-platinum, lợi tiểu quai.
10.5. Ý nghĩa lâm sàng
- Mặc dù tiềm ẩn nguy cơ độc tính thận, tai và tiền đình, tobramycin vẫn còn được sử dụng trên lâm sàng bởi tính hiệu quả của nó.
11. VANCOMYCIN
11.1. Lịch sử
- Vancomycin được phân lập lần đầu tiên năm 1953 từ vi khuẩn Amycolatopsis orientalis (danh pháp cũ là Streptomyces orientalis và Nocardia orientalis) trong đất thuộc đảo Borneo ở Đông Nam Á. Chính bởi khả năng khống chế tụ cầu qua nhiều lần cấy chuyển mà vẫn không phát sinh đề kháng nên thuốc được gọi tên là vancomycin dựa theo từ “vanquish” (chinh phục).
- Ban đầu dạng chế phẩm thuốc chưa tinh khiết có màu nâu được gọi là “bùn Mississippi” sử dụng gây độc cho tai trong và thận nên chỉ được dùng đến như giải pháp cuối cùng. Tuy nhiên dạng chế phẩm vancomycin hydrochloride hiện nay có độ tinh khiết trên 92% sử dụng an toàn hơn.
- Với thành phần carbohydrate và peptid, vancomycin được xếp vào nhóm kháng sinh glycopeptid. Bên cạnh tác dụng vượt trội khống chế tụ cầu kháng methicillin, vancomycin còn được sử dụng đường uống để điều trị viêm đại tràng do Clostridium difficile.
11.2. Dược lực học và dược động học
- Ngoại trừ một số vi khuẩn Neisseria, nhìn chung vancomycin không có tác dụng với vi khuẩn Gram âm mà chỉ tiêu diệt được vi khuẩn Gram dương. Phổ tác dụng của vancomycin chủ yếu là các loại tụ cầu, liên cầu, Enterococcus faecalis và Clostridium sp. Cơ chế tác dụng của vancomycin là gắn vào D-alanyl-D-alanine của peptid tham gia tổng hợp vách vi khuẩn, qua đó ức chế tổng hợp vách vi khuẩn.
- Thuốc hấp thu kém qua đường uống nên khi dùng đường uống chỉ nhằm mục đích tiêu diệt vi khuẩn trong lòng ống tiêu hóa. Nồng độ đỉnh huyết thanh đạt được ngay sau khi truyền tĩnh mạch xong.
- Thuốc phân bố rộng rãi trong các mô và dịch cơ thể, ngoại trừ dịch não tủy. Khi màng não viêm, tỷ số khuếch tán từ máu vào dịch não tủy tương đối tốt, nồng độ trong dịch não tủy khi đó thường cao hơn nồng độ ức chế tối thiểu (MIC). Thuốc gắn protein ở mức độ trung bình (55%).
- Thời gian bán thải là 4-6h, kéo dài đáng kể khi suy giảm chức năng thận. Ở suy thận giai đoạn cuối, thời gian này là 7,5 ngày. Ở trẻ sơ sinh, thời gian bán thải là 6-10h còn ở trẻ nhỏ thời gian này là 2-4h.
- Thuốc thải trừ chủ yếu qua lọc cầu thận, trong nước tiểu có tới 75% thuốc ở dạng chưa biến đổi trong 24h đầu. Ở người cao tuổi, độ thanh thải thuốc giảm.
11.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- Cần kiểm tra nồng độ ức chế tối thiểu (MIC) của vancomycin đối với chủng tụ cầu phân lập được. Nếu MIC ≥ 4 μg/mL thì cần chuyển sang lựa chọn điều trị khác. Xem xét lựa chọn điều trị thay thế khi MIC > 1 μg/mL. Nếu kết quả cấy máu sau 2-3 ngày điều trị vẫn dương tính kèm theo bằng chứng lâm sàng của nhiễm trùng tiến triển, cho dù MIC là bao nhiêu thì cũng vẫn phải coi như thất bại điều trị vancomycin.
- Liều tải ban đầu được tính theo cân nặng thực tế của bệnh nhân. Liều dùng tiếp theo cần điều chỉnh để đảm bảo nồng độ đáy trong huyết thanh 10-15 μg/mL (đối với liên cầu) hoặc 15-20 μg/mL (trường hợp tụ cầu). Nếu liều dùng trên 1g thì thời gian truyền tĩnh mạch từ 1,5-2h.
- VNTMNK do Enterococcus (chủng kháng penicillin hoặc bệnh nhân không thể dùng được beta-lactam): 15 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 12h kết hợp với gentamicin trong 6 tuần. Cần điều chỉnh để nồng độ đáy 15-20 μg/mL.
- VNTMNK do tụ cầu vàng kháng methicillin hoặc nhạy methicillin nhưng không sử dụng được beta-lactam: 15 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 12h, hoặc 15-20 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 8-12h, điều trị trong 6 tuần. Cần điều chỉnh để nồng độ đáy 15-20 μg/mL. Trường hợp van nhân tạo cần kết hợp với rifampicin và điều trị ít nhất 6 tuần, bên cạnh đó đó kết hợp với gentamicin trong 2 tuần đầu.
- VNTMNK do liên cầu nhóm viridans và S. bovis không dung nạp với penicillin hoặc ceftriaxon: 15 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 12h. Thời gian điều trị là 4 tuần đối với van tự nhiên hoặc 6 tuần đối với van nhân tạo. Cần điều chỉnh để nồng độ đáy 15-20 μg/mL.
- Điều trị theo kinh nghiệm VNTMNK trên van tự nhiên: 15-20 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 8-12h, kết hợp với ceftriaxon hoặc gentamicin. Cần điều chỉnh để nồng độ đáy 15-20 μg/mL.
- Điều trị theo kinh nghiệm VNTMNK trên van nhân tạo: 15-20 mg/kg (liều tối đa 2 g) truyền tĩnh mạch cách 8-12h, kết hợp với gentamicin và rifampicin. Cần điều chỉnh để nồng độ đáy 15-20 μg/mL.
- Điều chỉnh liều dùng khi suy thận:
- Mức lọc cầu thận > 90 mL/phút: không cần điều chỉnh liều
- Mức lọc cầu thận 50-90 mL/phút: giãn khoảng cách liều mỗi 12h.
- Mức lọc cầu thận 15-49 mL/phút: giãn khoảng cách liều mỗi 24h.
- Mức lọc cầu thận < 15 mL/phút: cho liều tải, sau đó theo dõi nồng độ huyết thanh để điều chỉnh liều tiếp theo. Nếu nồng độ ≤ 20 μg/mL thì dùng liều kế tiếp, nếu đã vượt 20 μg/mL thì tạm ngừng liều kế tiếp và tiếp tục theo dõi nồng độ huyết thanh sau 12h.
11.4. Tác dụng phụ và xử trí
- Tốt nhất nên tránh dùng cùng các thuốc độc với thận. Nếu bắt buộc phải sử dụng đồng thời các thuốc độc với thận thì cần lưu ý thường xuyên theo dõi chức năng thận. Trong các kết hợp kháng sinh lưu ý kết hợp với piperacillin/tazobactam có nguy cơ tổn thương thận cấp tính cao hơn.
- Hội chứng đỏ người thường xuất hiện khi truyền vancomycin quá nhanh. Nếu liều dùng trên 1g thì thời gian truyền tĩnh mạch từ 1,5-2h.
- Hội chứng DRESS (drug reaction with eosinophilia and systemic signs/symptoms) có biểu hiện tương tự hội chứng Stevens-Johnson nhưng không tổn thương niêm mạc. So với các kháng sinh khác cũng gây tăng bạch cầu ái toan, riêng vancomycin có nguy cơ cao gây thêm tổn thương da, thận và gan. Những người có HLA-A*32:01 tăng nguy cơ bị hội chứng DRESS sau dùng vancomycin trên 2 tuần.
- Các tác dụng phụ hay gặp khác bao gồm sốt, viêm da bọng nước IgA, giảm bạch cầu trung tính, giảm tiểu cầu, giảm thính lực. Nguy cơ giảm tiểu cầu và giảm thính lực có lẽ liên quan đến nồng độ đáy cao kéo dài.
11.5. Ý nghĩa lâm sàng
- Vancomycin vẫn là thuốc chủ lực để điều trị VNTMNK do tụ cầu kháng methicillin hiện nay nhưng việc dùng thuốc đòi hỏi phải rất tỉ mỉ từ xác định MIC, nồng độ huyết thanh cho đến đảm bảo thời gian truyền tĩnh mạch và theo dõi các tác dụng phụ.
- Một số thuốc kháng sinh điều trị MRSA mới hơn đã khắc phục được nhiều mặt trái của vancomycin, tuy nhiên chỉ định các thuốc này trong VNTMNK vẫn còn rất hạn chế.
12. DAPTOMYCIN
12.1. Lịch sử
- Daptomycin là kháng sinh nhóm lipopeptid với tác dụng trên vi khuẩn Gram dương hiếu khí cũng như kỵ khí còn mạnh hơn cả các glycopeptid. Thuốc có nguồn gốc từ vi khuẩn Streptomyces roseosporus.
- Sau khi ra đời vào cuối những năm 1980, thuốc đã thất bại trong thử nghiệm lâm sàng điều trị VNTMNK với liều 2 mg/kg cùng với tác dụng phụ bệnh lý cơ do thuốc. Tuy nhiên, đến năm 1997 thuốc đã được phát triển trở lại với liều dùng thông thường hiện nay là 4-6 mg/kg và thậm chí còn cao hơn nữa.
12.2. Dược lực học và dược động học
- Cơ chế tác dụng của daptomycin tấn công vào màng tế bào vi khuẩn. Daptomycin gắn và chèn vào màng tế bào, sau đó tập trung lại thành từng đám đa phân tử làm thay đổi độ uốn của màng, tạo thành các lỗ màng làm thoát ion. Hậu quả là sự khử cực diễn ra nhanh chóng, màng mất điện thế không hoạt động được chức năng tổng hợp protein, ADN và ARN dẫn đến chết tế bào vi khuẩn.
- Phổ diệt khuẩn của daptomycin chỉ bao gồm các vi khuẩn Gram dương. Bên cạnh liên cầu, tụ cầu (gồm cả MRSA), daptomycin còn có tác dụng với các Enterococcus (gồm cả các Enterococcus kháng glycopeptid – GRE).
- Thuốc gắn protein tới 90-93%. Thời gian bán thải 8-9h nhưng kéo dài tới 28h khi suy thận. Thuốc thải trừ qua nước tiểu (78%, chủ yếu là dưới dạng thuốc chưa biến đổi) và phân (5,7%).
12.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- Chất hoạt diện (surfactant) phổi làm bất hoạt daptomycin nên không dùng daptomycin nếu có viêm phổi kèm theo.
- VNTMNK do tụ cầu kháng methicillin (lựa chọn thay thế): 8 đến 10 mg/kg truyền tĩnh mạch một lần/24h trong 6 tuần. Những trường hợp nghi ngờ MRSA kháng daptomycin có thể phối hợp thêm cotrimoxazol hoặc nafcillin.
- VNTMNK do các Enterococcus kháng penicillin, aminoglycosid và vancomycin: 10 đến 12 mg/kg truyền tĩnh mạch một lần/24h, kết hợp với ampicillin hoặc ceftaroline trong ít nhất 6 tuần. Với van tự nhiên có thể dùng đơn trị liệu.
- Điều trị theo kinh nghiệm VNTMNK trên van tự nhiên (lựa chọn thay thế): 6 mg/kg truyền tĩnh mạch cách 24h, kết hợp với ceftriaxon hoặc gentamicin.
- Chỉ dùng dung dịch muối đẳng trương hoặc Ringer lactat để pha truyền, tránh dùng các dung môi chứa dextrose.
- Điều chỉnh liều dùng khi suy thận: Nếu mức lọc cầu thận dưới 30 mL/phút thì dùng thuốc cách 48h.
12.4. Tác dụng phụ và xử trí
- Cần theo dõi CPK hằng tuần. Nếu CPK tăng trên 10 lần mức bình thường hoặc có triệu chứng bệnh lý cơ kèm theo CPK tăng trên 1000 đơn vị/l thì phải ngừng daptomycin.
- Trong quá trình điều trị daptomycin cần ngừng statin do sử dụng đồng thời với các statin làm tăng nguy cơ bệnh lý cơ.
- Các tác dụng phụ khác hay gặp là đau đầu, buồn nôn/nôn, tiêu chảy, phát ban, sốt, viêm tĩnh mạch tại chỗ, viêm đại tràng giả mạc, tăng urê.
- Daptomycin tương tác với hóa chất đo thời gian prothrombin dẫn đến kết quả kéo dài giả tạo thời gian prothrombin.
12.5. Ý nghĩa lâm sàng
- Việc không sử dụng để điều trị viêm phổi đã hạn chế rất nhiều vai trò của daptomycin trên lâm sàng. Xu hướng hiện nay không dùng daptomycin đơn độc mà chú ý phối hợp với các kháng sinh khác để tránh phát sinh đề kháng với daptomycin.
- Những trường hợp VNTMNK liên quan dụng cụ điện tử cấy ghép hay gặp mầm bệnh MRSA là chỉ định có lẽ vừa tầm nhất đối với daptomycin hiện nay.
13. LINEZOLID
13.1. Lịch sử
- Linezolid là kháng sinh nhóm oxazolidinone được khám phá từ giữa những năm 1990 và công nhận sử dụng trên lâm sàng từ năm 2000. Những thuốc oxazolidinone đầu tiên được phát triển từ cuối những năm 1980 nhưng có nhiều độc tính. Linezolid là thuốc đầu tiên trong nhóm qua được thử nghiệm lâm sàng giai đoạn 1 mà không có độc tính gì đáng kể.
- Do mới ra đời, chưa có nhiều trường hợp đề kháng, cộng thêm chỉ định nhằm vào các trường hợp vi khuẩn đề kháng các kháng sinh kinh điển, linezolid đang được ưa chuộng sử dụng ngày một rộng rãi đến mức thường bị bỏ quên độc tính về huyết học và thần kinh khi sử dụng kéo dài.
13.2. Dược lực học và dược động học
- Linezolid gắn vào ARN 23S của tiểu phần ribosome 50S là nơi diễn ra hoạt tính peptidyl transferase, từ đó ức chế hình thành phức hợp 70S để khởi đầu của quá trình tổng hợp protein của vi khuẩn. Đối với các Enterococcus và tụ cầu, linezolid chỉ có tác dụng kìm khuẩn nhưng đối với phần lớn các chủng liên cầu thì nó lại có tác dụng diệt khuẩn.
- Hấp thu nhanh và nhiều qua đường tiêu hóa. Sinh khả dụng đường uống đạt xấp xỉ 100%. Thời gian đạt nồng độ đỉnh huyết thanh sau uống thuốc là 1-2h.
- Thuốc gắn protein 31%. Chuyển hóa tối thiểu ở gan (có thể qua trung gian cytochrome P450) tạo ra hai chất chuyển hóa không hoạt tính.
- Thời gian bán thải 4,9h, ở trẻ em dao động 1,8-5,6h.
- Thải trừ qua nước tiểu (khoảng 30% tổng liều là thuốc nguyên dạng, còn khoảng 50% tổng liều là các chất chuyển hóa) và phân (khoảng 9% tổng liều là các chất chuyển hóa). Bệnh nhân suy thận nặng có thể tích lũy các chất chuyển hóa của linezolid.
13.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- VNTMNK do các Enterococcus kháng penicillin, aminoglycosid và vancomycin: 600 mg uống hoặc truyền tĩnh mạch mỗi 12h trong ít nhất 6 tuần.
- Không cần điều chỉnh liều ở bất cứ mức lọc cầu thận nào.
13.4. Tác dụng phụ và xử trí
- Tiếp xúc thời gian ngắn: tiêu chảy, buồn nôn, nôn, phát ban, tăng men gan, viêm đại tràng giả mạc.
- Tiếp xúc thời gian dài trên 2 tuần sẽ xuất hiện các biểu hiện của ức chế tổng hợp protein của ty thể có tương quan với thời gian và liều dùng. Tuy nhiên sau khi ngừng thuốc, tất cả các biểu hiện đều có thể phục hồi hoàn toàn.
- Ức chế tủy xương có hồi phục: giảm tiểu cầu, thiếu máu, giảm bạch cầu trung tính. Hay gặp nhất sau khi điều trị trên 2 tuần. Nguy cơ cao nếu có bệnh thận giai đoạn cuối.
- Sau khi điều trị trên 4 tuần có thể bị nhiễm toan lactic, bệnh thần kinh ngoại vi, bệnh thần kinh thị.
- Linezolid ức chế monoamine oxidase nên có nguy cơ xuất hiện hội chứng serotonin (sốt, kích động, thay đổi trạng thái tinh thần, run) nếu dùng cho bệnh nhân đang sử dụng thuốc ức chế tái hấp thu serotonin có chọn lọc hoặc thuốc ức chế tái hấp thu norepinephrine serotonin.
- Nguy cơ tăng huyết áp nghiêm trọng nếu dùng cùng thức ăn giàu tyramine.
- Các tác dụng phụ khác như lưỡi lông đen, viêm thận kẽ cấp tính, răng xỉn màu.
13.5. Ý nghĩa lâm sàng
- Nên sử dụng linezolid trong điều trị VNTMNK khi bệnh nhân không đáp ứng với các thuốc kháng sinh khác. Tỷ lệ tái phát cao với điều trị linezolid khiến cho chỉ định điều trị VNTMNK của linezolid hiện nay chỉ còn tập trung vào các Enterococcus đa kháng kháng sinh.
14. RIFAMPICIN
14.1. Lịch sử
- Rifampicin là kháng sinh được nhóm nghiên cứu của Piero Sensi và Maria Teresa Timbal phân lập từ vi khuẩn Amycolatopsis (trước kia gọi là Streptomyces và Nocardia) mediterranei vào năm 1957. Do Sensi, Timbal và các nhà nghiên cứu trong nhóm đều rất thích bộ phim hình sự của Pháp nhan đề “Rififi”, họ quyết định đặt tên cho hợp chất mới phân lập là “rifamycin”. Sau đó vào năm 1965 khi có được sản phẩm bán tổng hợp ổn định hơn với hiệu quả cao và khả năng dung nạp tốt, hợp chất mới được gọi là “rifampicin” tồn tại cho đến ngày nay.
- Rifampicin được bán trên thị trường từ năm 1968 và được FDA công nhận từ năm 1971.
14.2. Dược lực học và dược động học
- Rifampicin thường dùng trên lâm sàng để điều trị lao và các vi khuẩn Mycobacterium. Ngoài ra rifampicin còn dùng để điều trị tụ cầu, não mô cầu Neisseria sp., Legionella sp. và một số vi khuẩn khác. Cơ chế tác dụng của thuốc là gắn vào tiểu đơn vị beta của ARN polymerase phụ thuộc ADN, ngăn cản quá trình sao chép ARN và ức chế tổng hợp ARN của vi khuẩn. Tuy nhiên, vi khuẩn rất dễ kháng thuốc do chỉ cần đột biến đơn ở gen rpoB của ARN polymerase.
- Thuốc hấp thu tốt qua đường tiêu hóa. Sau uống thuốc 2-4h đạt được nồng độ đỉnh huyết thanh. Thức ăn làm chậm thời gian đạt được hoặc giảm nhẹ nồng độ đỉnh.
- Thuốc phân bố rất ưa lipid, dễ dàng qua được hàng rào máu não. Tỉ số nồng độ thuốc trong dịch não tủy : trong máu khi màng não viêm là 25%. Thuốc gắn protein tới 80%. Chuyển hóa thuốc ở gan và thuốc tham gia vào chu trình gan ruột.
- Thời gian bán thải là 3-4h, kéo dài hơn khi có suy chức năng gan. Ở bệnh nhân bệnh thận giai đoạn cuối, thời gian này là 1,8-11h.
- Thuốc thải trừ qua phân (60-65%) và nước tiểu (~30%) dưới dạng thuốc không biến đổi.
14.3. Chỉ định, chống chỉ định, liều dùng, cách dùng
- Thông thường rifampicin được dùng đường uống. Nên uống thuốc lúc đói để tránh thức ăn ảnh hưởng hấp thu thuốc.
- Rifampicin hiếm khi điều trị đơn độc mà thường kết hợp với các thuốc khác để đạt được hiệu quả cộng gộp hoặc hiệp đồng và giảm nguy cơ phát sinh đề kháng.
- VNTMNK do tụ cầu trên van nhân tạo: 300 mg mỗi 8h trong ít nhất 6 tuần. Trong trường hợp VNTMNK do MRSA, cần kết hợp rifampicin với vancomycin trong suốt liệu trình và với gentamicin trong 2 tuần đầu. Trong trường hợp VNTMNK do MSSA, cần kết hợp rifampicin với nafcillin hoặc oxacillin trong suốt liệu trình và với gentamicin trong 2 tuần đầu.
- Điều trị theo kinh nghiệm VNTMNK trên van nhân tạo: Rifampicin 300 mg mỗi 8h kết hợp với vancomycin và gentamicin.
- Không cần điều chỉnh liều khi suy giảm chức năng thận.
14.4. Tác dụng phụ và xử trí
- Rifampicin có nguy cơ gây ngộ độc gan, thường biểu hiện trên lâm sàng là viêm gan ứ mật. Thận trọng khi dùng thuốc cho bệnh nhân suy giảm chức năng gan hoặc đã có tiền sử hay hiện tại đang lạm dụng rượu. Nếu tăng bilirubin và/hoặc tăng đáng kể men gan thì ngừng điều trị rifampicin.
- Rifampicin tương tác với rất nhiều các loại thuốc khác nhau. Trước khi điều trị rifampicin cho bệnh nhân hoặc trước khi dùng thuốc cho bệnh nhân đang điều trị rifampicin cần thận trọng tra cứu các tương tác thuốc có thể có để phòng tránh.
- Khi điều trị rifampicin nước tiểu, phân, nước bọt, mồ hôi, nước mắt và dịch não tủy chuyển sang màu đỏ cam. Nước mắt màu đỏ cam có thể làm kính áp tròng bị bắt màu vĩnh viễn.
- Khi điều trị gián đoạn, cho dù là gián đoạn có chủ đích hay kém tuân thủ thì cũng dễ gặp hội chứng giống cúm.
- Có thể xuất hiện giảm tiểu cầu miễn dịch do thuốc, viêm mạch, viêm thận kẽ.
14.5. Ý nghĩa lâm sàng
- Nhược điểm của rifampicin khá nhiều: Từ hoạt tính in vitro hay thay đổi, dễ phát sinh đề kháng cho đến nhiều tác dụng phụ, đặc biệt là tương tác với nhiều loại thuốc. Do đó, vai trò của rifampicin đã được loại bỏ trong điều trị VNTMNK trên van tự nhiên.
- Tuy nhiên đối với VNTMNK trên van nhân tạo, mô hình thực nghiệm cho thấy phối hợp rifampicin với vancomycin và gentamicin đạt được hiệu quả cao nhất. Đây là căn cứ để các Hướng dẫn điều trị VNTMNK Tây Âu cũng như Bắc Mỹ khuyến cáo sử dụng phác đồ có rifampicin. Trên lâm sàng, rifampicin thường được bổ sung sau khi đã có kết quả phân lập vi khuẩn để giảm hơn nữa nguy cơ kháng thuốc và tương tác thuốc.
PHẦN III. ĐIỀU TRỊ VIÊM NỘI TÂM MẠC NHIỄM KHUẨN TRONG MỘT SỐ TRƯỜNG HỢP
1. DỰ PHÒNG VIÊM NỘI TÂM MẠC NHIỄM KHUẨN
Theo khuyến cáo của ESC về VNTMNK cập nhật năm 2015, kháng sinh dự phòng chỉ nên dùng cho bệnh nhân ở mức nguy cơ cao đối với VNTMNK, bao gồm:
- Bệnh nhân với bất kỳ van nhân tạo nào, bao gồm cả van nhân tạo đặt qua ống thông hoặc được sửa van với vật liệu nhân tạo.
- Bệnh nhân có tiền sử VNTMNK.
- Bệnh nhân tim bẩm sinh: (1) tim bẩm sinh có tím; (2) tim bẩm sinh có vật liệu nhân tạo, có thể qua phẫu thuật hoặc can thiệp qua da. Liệu trình kháng sinh dự phòng được sử dụng cho đến 6 tháng sau thủ thuật, hoặc suốt đời nếu còn shunt tồn lưu hoặc hở van tim.
1.1. Thủ thuật cần có kháng sinh dự phòng theo hướng dẫn ESC 2015
a. Các thủ thuật răng miệng
- Kháng sinh dự phòng nên được chỉ định cho các thủ thuật nha khoa đòi hỏi các thao tác qua vùng lợi hoặc vùng quanh chóp răng hoặc gây tổn thương niêm mạc miệng.
- Kháng sinh dự phòng không được khuyến cáo cho các trường hợp: Tiêm gây tê tại chỗ ở vùng không bị nhiễm khuẩn, điều trị sâu răng trên bề mặt, cắt bỏ chỉ khâu, xạ trị răng, thay đổi hoặc sửa chữa các vật liệu phục hình, chỉnh hình răng miệng, niềng răng, sau nhổ răng hoặc chấn thương đến môi hay niêm mạc miệng.
- Kháng sinh được cho một liều duy nhất từ 30 – 60 phút trước thủ thuật và không cần sử dụng nhắc lại liều sau thủ thuật.
Bảng 21.7: Phác đồ kháng sinh dự phòng VNTMNK (theo ESC 2015)
|
Tình huống |
Kháng sinh |
Người lớn |
Trẻ em |
|
Không dị ứng penicillin và ampicillin |
amoxicillin hoặc ampicillina |
2 g uống hoặc đường tĩnh mạch |
50 mg/kg uống hoặc đường tĩnh mạch |
|
Dị ứng penicillin hoặc ampicillin |
Clindamycin |
600 mg uống hoặc đường tĩnh mạch |
20 mg/kg uống hoặc đường tĩnh mạch |
Chú thích: aLựa chọn khác là cephalexin 2 g đường tĩnh mạch với người lớn hoặc 50 mg/kg đường tĩnh mạch với trẻ em, cefazoline hoặc ceftriaxone 1 g đường tĩnh mạch với người lớn hoặc 50 mg/kg đường tĩnh mạch với trẻ em. Cephalosporine không nên được sử dụng ở những bệnh nhân bị sốc phản vệ, phù mạch hoặc nổi mày đay sau khi uống penicillin hoặc ampicillin do phản ứng dị ứng chéo.
VNTMNK: Viêm nội tâm mạc nhiễm khuẩn; ESC: European Society of Cardiology (Hội Tim mạch châu Âu).
b. Các thủ thuật liên quan đến đường hô hấp
Kháng sinh dự phòng không được khuyến cáo cho các thủ thuật liên quan đến đường hô hấp, bao gồm cả: nội soi phế quản, nội soi thanh quản, đặt nội khí quản qua miệng hay qua mũi.
Trong trường hợp có viêm đường hô hấp nên điều trị kháng sinh ổn định trước thủ thuật.
Những bệnh nhân nằm trong nhóm nguy cơ cao bị VNTMNK khi trải qua các thủ thuật đường hô hấp có xâm lấn với mục đích điều trị các nhiễm trùng hiện tại (ví dụ: dẫn lưu ổ áp xe) nên dùng kháng sinh tác dụng trên tụ cầu.
c. Thủ thuật liên quan đến dạ dày – ruột hoặc niệu – sinh dục hoặc siêu âm tim qua thực quản
Kháng sinh dự phòng không được khuyến cáo cho các thủ thuật như: nội soi dạ dày, nội soi đại tràng, nội soi bàng quang, đỡ đẻ tự nhiên qua đường âm đạo hoặc phẫu thuật lấy thai hoặc siêu âm tim qua thực quản.
Những bệnh nhân đang có tình trạng nhiễm trùng liên quan đến hệ dạ dày- ruột, sinh dục – tiết niệu ở nhóm bệnh nhân nguy cơ cao nên sử dụng kháng sinh có tác dụng trên các chủng enterococcus (Ví dụ: ampicillin, amoxicillin hoặc vancomycin nếu không dung nạp với nhóm beta-lactam).
d. Các thủ thuật ở da và mô mềm
Kháng sinh dự phòng không được khuyến cáo cho bất cứ thủ thuật nào (ngoại trừ bệnh nhân nằm trong nhóm nguy cơ cao bị VNTMNK được làm thủ thuật do các nhiễm trùng da, mô mềm, cơ xương khớp (Ví dụ: Áp xe) thì nên sử dụng kháng sinh có tác dụng trên tụ cầu và liên cầu tan huyết nhóm β).
1.2. Khuyến cáo dùng kháng sinh phòng ngừa nhiễm khuẩn khu trú và toàn thân trước các thủ thuật can thiệp tim và mạch máu
- Khuyến cáo sàng lọc tụ cầu vàng vùng mũi họng ở những người mang mầm bệnh, với các phẫu thuật tim mạch có chuẩn bị.
- Dự phòng trước thủ thuật được khuyến cáo cho đặt máy tạo nhịp hoặc máy phá rung tự động (ICD).
- Các ổ nhiễm khuẩn tiềm tàng cần được loại trừ trước phẫu thuật ít nhất 2 tuần: Phẫu thuật van nhân tạo, các thiết bị nhân tạo trong tim hoặc trong mạch máu, ngoại trừ phẫu thuật cấp cứu.
- Kháng sinh dự phòng nên được cân nhắc ở bệnh nhân trải qua phẫu thuật thay van hoặc đặt thiết bị nhân tạo trong lòng mạch (hoặc thủ thuật qua da).
- Điều trị toàn thân một cách hệ thống không được khuyến cáo khi không có sàng lọc nhiễm tụ cầu.
- Kháng sinh dự phòng nên được bắt đầu ngay lập tức trước thủ thuật và lặp lại nếu thủ thuật kéo dài trên 48h.
1.3. Các phương pháp dự phòng VNTMNK không đặc hiệu
- Các phương pháp này nên được áp dụng cho tất cả mọi người nói chung, đặc biệt cần được tăng cường hơn nữa ở các bệnh nhân có nguy cơ cao VNTMNK.
- Vệ sinh da và răng miệng thường xuyên. Theo dõi răng miệng nên được tiến hành 2 lần mỗi năm đối với bệnh nhân có nguy cơ mắc bệnh cao và hằng năm đối với những bệnh nhân còn lại.
- Tránh nhiễm khuẩn vết thương.
- Loại bỏ hoặc làm giảm các ổ mang vi khuẩn mạn tính: ngoài da, đường tiết niệu, đường răng miệng.
- Điều trị khỏi các ổ nhiễm khuẩn (bằng kháng sinh).
- Bệnh nhân không tự ý dùng thuốc kháng sinh.
- Kiểm soát nhiễm khuẩn chặt chẽ khi tiến hành bất kỳ thủ thuật nào có nguy cơ.
- Không khuyến khích xỏ lỗ tai hay xăm trổ.
- Hạn chế tối đa việc đặt đường truyền tĩnh mạch và các thủ thuật xâm lấn. Nếu cần đặt đường truyền tĩnh mạch, ưu tiên sử dụng đường truyền tĩnh mạch ngoại biên hơn là tĩnh mạch trung tâm và thay đường truyền ngoại biên mỗi 3 – 4 ngày.
2. PHÁC ĐỒ ĐIỀU TRỊ
2.1. Kháng sinh theo kinh nghiệm ở những bệnh nhân cấp tính nặng chưa xác định căn nguyên
Bảng 21.8: Kháng sinh theo kinh nghiệm ở những bệnh nhân cấp tính nặng chưa xác định căn nguyên
|
Loại kháng sinh |
Liều lượng và cách dùng |
Chú thích |
|
|
VNTMNK van tự nhiên tại cộng đồng hoặc van nhân tạo muộn (>12 tháng sau phẫu thuật) |
|||
|
Ampicillin kết hợp (flu)cloxacillin hoặc oxacillin kết hợp
gentamicinb |
12 g/24h, TM, 4-6 lần 12 g/24h, TM, 4-6 lần
3 mg/kg/24h, TM hoặc TB 1 lần |
Bệnh nhân VNTMNK cấy máu âm tính nên được hội chẩn với chuyên gia truyền nhiễm |
|
|
VNTMNK van nhân tạo sớm (≤12 tháng sau phẫu thuật) hoặc liên quan và không liên quan nhiễm trùng bệnh viện |
|||
|
Vancomycinb kết hợp gentamicinb kết hợp
rifampin |
30 mg/kg/24h, TM chia 2 lần
3 mg/kg/24h, TM hoặc TB, 1 lần
900-1200 mg, TM hoặc uống, chia 2-3 lần |
Rifampicin chỉ được khuyến cáo cho VNTMNK van nhân tạo và một số chuyên gia khuyến cáo nên bắt đầu muộn hơn vancomycin và gentamicin 3-5 ngày. VNTMNK van tự nhiên, liên quan đến chăm sóc y tế ở những cơ sở y tế tỷ lệ nhiễm MRSA >5%, nên phối hợp cloxacillin với vancomycin đến khi xác định được S. aureus. |
|
Chú thích: aNếu mẫu cấy máu ban đầu âm tính và không có đáp ứng lâm sàng, cân nhắc nguyên nhân gây VNTMNK cấy máu âm tính và xét phẫu thuật, điều trị kháng sinh phổ rộng cho các căn nguyên cấy máu âm tính (doxycycline, quinolone) nên được cân nhắc. bTheo dõi liều gentamicin hoặc vancomycin. TM: Tĩnh mạch.
2.2 Điều trị kháng sinh đối với VNTMNK do Streptococcus đường miệng và Streptococcus bovis
Bảng 21.9: Điều trị kháng sinh đối với VNTMNK do Streptococci đường miệng và Streptococcus bovis (theo ESC 2015)
|
Loại kháng sinh |
Liều lượng và cách dùng |
T.Gian (tuần) |
Lưu ý |
|
|
Chủng Streptococcus đường miệng và tiêu hóa nhạy cảm penicillin (MIC ≤ 0,125 mg/L) |
||||
|
Điều trị chuẩn: Thời gian 4 tuần |
||||
|
Penicillin G hoặc
Amoxicillina hoặc
Ceftriaxoneb |
12 – 18 triệu đơn vị/24h, TM chia 4 – 6 lần hoặc truyền liên tục 100 – 200 mg/kg/24h, TM chia 4 – 6 lần
2 g/24h, TM 1 lần |
4 |
Ưu tiên cho bệnh nhân > 65 tuổi hoặc suy thận hoặc giảm chức năng thần kinh VIII. Khuyến cáo điều trị 6 tuần với bệnh nhân VNTMNK trên van nhân tạo |
|
|
4 |
||||
|
4 |
||||
|
|
Liều trẻ em:c – Penicillin G 200.000 đơn vị/24h, TM chia 4-6 lần – Amoxicillin 300 mg/kg/24h, TM chia 4-6 lần – Ceftriaxone 100 mg/kg/24h, TM 1 lần/24h |
|
||
|
Điều trị chuẩn: Thời gian 2 tuần |
||||
|
Penicillin G hoặc
Amoxicillina hoặc
Ceftriaxoneb Kết hợp Gentamicind hoặc Netilmicin |
12 – 18 triệu đơn vị/24h, TM chia 4-6 lần hoặc truyền liên tục 100 – 200 mg/kg/24h, TM chia 4 – 6 lần 2 g/24h, TM 1 lần
3 mg/kg/24h, TM hoặc Tiêm bắp 1 lần 4-5 mg/kg/24h, TM 1 lần
Liều trẻ em:c Penicillin G, Amoxicillin và Ceftriaxone liều như trên Gentamicin 3 mg/kg/24h, TM hoặc tiêm bắp 1 lần hoặc chia 3 lần |
2 |
Chỉ khuyến cáo cho bệnh nhân VNTMNK trên van tự nhiên không biến chứng với chức năng thận bình thường. |
|
|
2 |
||||
|
2 |
||||
|
2 |
||||
|
2 |
||||
|
|
|
|||
|
Với bệnh nhân dị ứng beta-lactame |
||||
|
Vancomycin
|
30 mg/kg/24h, TM chia 2 lần
Liều trẻ em:c Vancomycin 40 mg/kg/24h, TM chia 2 – 3 lần |
4 |
Điều trị 6 tuần khuyến cáo cho bệnh nhân VNTMNK van nhân tạo |
|
|
|
||||
|
Chủng kháng penicillin tương đối (MIC 0,250- 2 mg/l)f |
||||
|
Điều trị chuẩn |
||||
|
Penicillin G hoặc
Amoxicillina hoặc
Ceftriaxoneb
kết hợp Gentamicind |
24 triệu đơn vị/24h, TM chia 4 – 6 lần hoặc truyền liên tục 200 mg/kg/24h, TM chia 4 – 6 lần 2 g/24h, TM 1 lần
3 mg/kg/24h, TM hoặc tiêm bắp 1 lần |
4 |
Điều trị 6 tuần khuyến cáo cho bệnh VNTMNK van nhân tạo |
|
|
4 |
||||
|
4 |
||||
|
2 |
||||
|
Với bệnh nhân dị ứng beta-lactame |
||||
|
Vancomycinf
kết hợp Gentamicing
|
30 mg/kg/24h, TM chia 2 lần
3 mg/kg/24h, TM hoặc tiêm bắp 1 lần
Liều trẻ em:c như trên |
4 |
Điều trị 6 tuần khuyến cáo cho bệnh nhân VNTMNK van nhân tạo |
|
Chú thích: aHoặc ampicillin, giống liều của amoxicillin; bƯu tiên cho những bệnh nhân ngoại trú; cLiều trẻ em không nên vượt quá liều người lớn; dChức năng thận và nồng độ gentamicin trong huyết thanh nên được theo dõi mỗi lần một tuần. Khi dùng 1 lần/24h, nồng độ trước liều tiếp theo nên < 1 mg/L và nồng độ sau liều (đạt đỉnh 1h sau khi tiêm) nên đạt ∼10-12 mg/L; eGiải mẫn cảm với penicillin có thể thử ở những bệnh nhân ổn định; fNồng độ vancomycin trong huyết thanh nên đạt mức 10 – 15 mg/L trước liều, mặc dù một vài chuyên gia khuyến cáo tăng liều vancomycin lên tới 45 – 60 mg/kg/24h TM chia 2 hoặc 3 lần để đạt nồng độ vancomycin trước liều (nồng độ tối thiểu) ở mức 15 – 20 mg/L như trong viêm nội tâm mạc do Staphylococcus. Tuy nhiên, liều vancomycin không nên vượt quá 2 g/24h trừ khi theo dõi được nồng độ huyết thanh và điều chỉnh tới khi đạt được nồng độ đỉnh là 30 – 45 μg/mL sau khi truyền tĩnh mạch 1h; gNhững bệnh nhân nhiễm chủng kháng penicillin (MIC > 2 mg/L) nên được điều trị như viêm nội tâm mạc do Enterococcus. TM: Tĩnh mạch.
2.3. Điều trị kháng sinh đối với VNTMNK do Staphylococcus spp
Bảng 21.10: Điều trị kháng sinh đối với VNTMNK do Staphylococcus spp (theo ESC 2015)
|
Loại kháng sinh |
Liều lượng và cách dùng |
T.gian (tuần) |
Lưu ý |
||
|
Van tự nhiên |
|||||
|
Staphylococcus nhạy cảm Methicillin |
|||||
|
(Flu)cloxacillin hoặc oxacillin
|
12 g/24h, TM chia 4-6 lần
Liều trẻ em:f 200-300 mg/kg/24h, TM chia 4-6 lần |
4-6 |
Phối hợp gentamicin không được khuyến cáo vì lợi ích trên lâm sàng chưa được chứng minh và tăng độc tính trên thận. *cho Staphylococcus aureus |
||
|
|
|||||
|
Liệu pháp thay thế* Cotrimoxazole
Kết hợp Clindamycin
|
Sulfamethoxazole 4800 mg/24h và Trimethoprim 960 mg/24h, TM chia 4-6 lần
1800 mg/24h, TM chia 3 lần
Liều trẻ emf: Sulfamethoxazole 60 mg/kg/24h và Trimethoprim 12 mg/kg/24h (TM chia 2 lần) Clindamycin 40 mg/kg/24h (TM chia 3 lần) |
1 tuần TM+ 5 tuần uống |
|||
|
1 |
|||||
|
|
|||||
|
Staphylococcus kháng methicillin hoặc bệnh nhân dị ứng penicillin |
|||||
|
Vancomycinb ** |
30-60 mg/kg/24h, TM chia 2-3 lần Liều trẻ em:g 40 mg/kg/24h, TM chia 2-3 lần |
4-6 |
Cephalosporin (cefazolin 6 g/24h hoặc cefotaxime 6 g/24h chia 3 lần) được khuyến cáo cho bệnh nhân dị ứng penicillin không có phản ứng phản vệ trong viêm nội tâm mạc do tụ cầu nhạy cảm methicillin. Daptomycin vượt trội hơn Vancomycin với nhiễm trùng MSSA và MRSA có MIC Vancomycin >1 mg/L *cho Staphylococcus aureus |
||
|
Liệu pháp thay thế** Daptomycinc
|
10 mg/kg/24h, TM 1 lần Liều trẻ em:f 10 mg/kg/24h, TM 1 lần |
4-6 |
|||
|
Liệu pháp thay thế* Cotrimoxazole*
kết hợp
Clindamycin |
Sulfamethoxazole 4800 mg/24h và Trimethoprim 960 mg/24h (TM chia 4-6 lần)
1800 mg/24h, TM chia 3 lần |
1 tuần TM + 5 tuần uống |
|||
|
1 |
|||||
|
Van nhân tạo |
|||||
|
Staphylococci nhạy cảm Methicillin |
|||||
|
(Flu)cloxacillin hoặc oxacillin kết hợp Rifampicind và Gentamicine |
12 g/24h, TM chia 4-6 lần
900-1200 mg, TM hoặc uống chia 2-3 lần 3 mg/kg/24h, TM hoặc tiêm bắp chia 1-2 lần
Liều trẻ em:g Oxacillin và (Flu)cloxacillin như trên Rifampin 20 mg/kg/24h, TM hoặc uống chia 3 lần |
≥6 |
|
||
|
≥6 |
|||||
|
2 |
|||||
|
Đối với bệnh nhân dị ứng beta-lactamh hoặc Staphylococci kháng Methicillin |
|||||
|
Vancomycinb kết hợp
Rifampicind và
Gentamicine |
30-60 mg/kg/24h, TM chia 2-3 lần
900-1200 mg, TM hoặc uống chia 2 – 3 lần
3 mg/kg/24h, TM hoặc tiêm bắp chia 1 – 2 lần
Liều trẻ em:g Như trên |
≥ 6 |
Cephalosporin (cefazolin 6 g/24h hoặc cefotaxime 6 g/24h TM chia 3 lần) được khuyến cáo cho bệnh nhân dị ứng Penicillin không có phản ứng phản vệ với viêm nội tâm mạc nhạy cảm Methicillin. Một số chuyên gia khuyến cáo nên bắt đầu sử dụng Rifampicin sau 3 – 5 ngày điều trị vancomycin và gentamicin. Gentamicin có thể được dùng với liều duy nhất trong ngày để giảm độc tính trên thận. |
||
| 2 |
Chú thích: aChức năng thận, nồng độ cotrimoxazole trong huyết thanh nên được theo dõi 1 lần một tuần (2 lần một tuần với những bệnh nhân suy thận ); bNồng độ tối thiểu của vancomycin (Cmin) nên ≥20 mg/L. Tỷ lệ AUC/MIC >400 được khuyến cáo cho nhóm VNTMNK do MRSA; cTheo dõi nồng độ CPK (creatine phosphokinase) ít nhất 1 lần/tuần. Một số chuyên gia khuyên kết hợp cloxacillin (2g/4h TM) hoặc fosfomycin (2g/6h TM) với daptomycin để tăng độ hoạt động và tránh sự phát triển của đề kháng daptomycin; dDaptomycin và fosfomycin không sẵn có ở một số nước châu Âu; eRifampicin được cho là đóng vai trò đặc biệt ở viêm nội tâm mạc van nhân tạo vì nó giúp loại bỏ vi khuẩn bám dính vào vật liệu kim loại. Vai trò của việc dùng rifampicin liên quan với tần suất cao của sự đề kháng của vi khuẩn và không được khuyến cáo. Rifampicin làm tăng sự chuyển hóa qua gan của warfarin và các thuốc khác; fChức năng thận và nồng độ gentamicin trong huyết thanh nên được theo dõi 1 lần/tuần (2 lần/tuần với những bệnh nhân suy thận); gLiều trẻ em không nên vượt quá liều của người lớn; ** Không có lợi ích về lâm sàng của việc thêm rifampicin hoặc gentamycin. TM: Tĩnh mạch.
2.4. Điều trị kháng sinh đối với VNTMNK do Enterococcus
Bảng 21.11: Điều trị kháng sinh đối với VNTMNK do Enterococcus (theo ESC 2015)
|
Loại kháng sinh |
Liều lượng và cách dùng |
T.gian (tuần) |
Lưu ý |
|
|
Trường hợp nhạy cảm với KS nhóm Beta-lactam và Gentamicin (Các trường hợp kháng 2 nhóm này sử dụng KS theoa,b,c) |
||||
|
Amoxicillin* kết hợp
Gentamicind
|
200 mg/kg/24h , TM chia 4-6 lần
3 mg/kg/24h, TM hoặc tiêm bắp 1 lần
Liều trẻ eme: Ampicillin 300 mg/kg/24h, TM chia 4-6 lần. Gentamicin 3 mg/kg/24h, TM hoặc tiêm bắp chia 3 lần |
4 – 6 |
Khuyến cáo điều trị 6 tuần cho bệnh nhân có triệu chứng >3 tháng hoặc VNTMNK van nhân tạo |
|
|
2 – 6** |
||||
|
|
||||
|
Ampicillin kết hợp
Ceftriaxone
|
200 mg/kg/24h, TM chia 4-6 lần
4 g/24h, TM chia 2 lần
Liều trẻ eme: Amoxicillin như trên Ceftriaxone 100 mg/kg/12h, TM |
6 |
Hai loại kháng sinh này được sử dụng phối hợp để chống lại Enterococcus faecalis có hoặc không có HLAR.
Sự phối hợp này không có tác dụng trên E.faecium |
|
|
6 |
||||
|
|
||||
|
Vancomycin kết hợp Gentamicin
|
30 mg/kg/24h, TM chia 2 lần
3 mg/kg/24h, TM hoặc tiêm bắp 1 lần
Liều trẻ eme: Vancomycin 40 mg/kg/24h, TM chia 2-3 lần. Gentamicin liều như trên |
6 |
|
|
|
6 |
||||
|
|
||||
Chú thích: aĐề kháng mức độ cao với gentamycin (MIC >500 mg/L): Nếu nhạy với streptomycin, thay thế gentamicin bằng streptomycin 15 mg/kg/24h chia 2 lần. bĐề kháng beta-lactam : (i) Nếu do sản xuất beta-lactamase, thay thế ampicillin bằng ampicillin–sulbactam hoặc amoxicillin bằng amoxicillin–clavulanate; (ii) nếu do sự biến đổi PBP5, dùng vancomycin. cĐa kháng với aminoglycoside, beta-lactam và vancomycin: Nên thay thế bằng (i) daptomycin 10 mg/kg/24h kết hợp ampicillin 200 mg/kg/24h TM chia 4-6 liều; (ii) Linezolid 2 lần × 600 mg/24h ™ hoặc uống ≥8 tuần (IIa, C) (Theo dõi độc tính trên huyết học); (iii) Quinupristin – Dalfopristin 3 lần × 7,5 mg/kg/24h ≥8 tuần. Quinupristin – Dalfopristin không có tác dụng chống lại E. faecalis; (iv) sự kết hợp khác (Daptomycin kết hợp Ertapenem hoặc ceftaroline), hội chẩn với chuyên gia bệnh truyền nhiễm. dTheo dõi nồng độ aminoglycoside trong huyết thanh và chức năng thận. eLiều trẻ em không nên vượt quá liều người lớn. fTheo dõi nồng độ vancomycin trong huyết thanh. *Hoặc ampicillin, giống liều như amoxicillin. **Một số chuyên gia khuyến cáo dùng gentamicin chỉ trong 2 tuần (IIa, B).
ESC: European Society of Cardiology (Hội Tim mạch châu Âu); VNTMNK: Viêm nội tâm mạc nhiễm khuẩn; HLAR (High level aminoglycosid resistance: Đề kháng cao với kháng sinh nhóm aminoglycosid; KS: Kháng sinh; TM: Tĩnh mạch; PBP5 (Penicillin-binding protein 5): Protein 5 gắn kết Penicillin.
2.5. Kháng sinh điều trị viêm nội tâm mạc nhiễm khuẩn cấy máu âm tính
Bảng 21.12: Kháng sinh điều trị viêm nội tâm mạc nhiễm khuẩn cấy máu âm tính (theo ESC 2015)
|
Căn nguyên gây bệnh |
Lựa chọn ưu tiêna |
Kết quả điều trị |
|
Brucella spp. |
Doxycycline 200 mg/24h, uống kết hợp Cotrimoxazol 960 mg/12h, uống kết hợp Rifampicin 300 – 600 mg/24h, uống trong ≥ 3 – 6 thángb |
Điều trị thành công khi hiệu giá kháng thể < 1:60. Một số chuyên gia khuyến cáo kết hợp thêm gentamicin trong 3 tuần đầu. |
|
C. burnetii (gây sốt Q) |
Doxycycline 200 mg/24h, uống kết hợp Hydroxychloroquine 200 – 600 mg/24hc uống > 18 tháng. |
Điều trị thành công khi hiệu giá kháng thể pha I IgG < 1:200, và IgA, IgM < 1:50. |
|
Bartonella spp.d |
Doxycycline 100 mg/12h uống trong 4 tuần kết hợp Gentamycin 3 mg/24 h, TM trong 2 tuần. |
Khả năng điều trị thành công ≥ 90%. |
|
Legionella spp. |
Levofloxacin 500 mg/12 h, TM hoặc uống trong ≥ 6 tuần hoặc Clarithromycin 500 mg/12h, TM trong 2 tuần, sau đó chuyển sang uống trong 4 tuần kết hợp Rifampicin 300 – 1200 mg/24h. |
Điều trị tối ưu chưa rõ. |
|
Mycoplasma spp. |
Levofloxacin 500 mg/12 h, TM hoặc uống trong ≥ 6 thánge |
Điều trị tối ưu chưa rõ. |
|
T. whipplei (gây bệnh Whipple)f |
Doxycycline 200 mg/24h kết hợp Hydroxychloroquine 200 – 600 mg/24hc uống trong ≥ 18 tháng |
Điều trị lâu dài, thời gian điều trị tối ưu chưa rõ. |
Chú thích: a.Do số lượng các ca lâm sàng hạn chế, thời gian điều trị VNTMNK do các tác nhân này chưa được biết. Thời gian điều trị được trình bày phụ thuộc vào các báo cáo lâm sàng chọn lọc. Khuyến cáo hội chẩn với các chuyên gia bệnh truyền nhiễm. b.Thêm streptomycin (15 mg/kg/24h chia 2 liều) cho một vài tuần đầu tiên là tối ưu. c.Doxycycline kết hợp hydroxychloroquine (theo dõi nồng độ hydroxychloroquine huyết thanh) có ưu thế vượt trội đáng kể so với doxycycline. d.Một số phương pháp điều trị đã được báo cáo, bao gồm aminopenicillins (ampicillin hoặc amoxicillin, 12 g/24h TM) hoặc cephalosporin (ceftriaxone, 2g/24h TM) kết hợp với aminoglycoside (gentamicin hoặc netilmicin). Liều giống với liều dùng cho viêm nội tâm mạc do Streptococcus và Enterococcus. e.Fluoroquinolone thế hệ mới (levofloxacin, moxifloxacin) có hiệu lực hơn ciprofloxacin trong việc kháng lại các tác nhân vi khuẩn nội bào như là Mycoplasma spp., legionella spp., và chlamydia spp. f.Điều trị viêm nội tâm mạc do T.whipplei. chủ yếu theo kinh nghiệm. Trong trường hợp nhiễm trùng hệ thần kinh trung ương, sulfadiazine 1,5 g/6h đường uống nên được kết hợp với doxycycline. Một liệu pháp thay thế là ceftriaxone (2 g/24h TM) trong 2 – 4 tuần hoặc penicillin G (2 triệu đơn vị/4h) và streptomycin (1 g/24h TM) trong 2 – 4 tuần sau đó uống cotrimoxazole (800 mg/12h). Trimethoprim không có tác dụng kháng lại T. whipplei. Thành công đã được báo cáo với liệu pháp lâu dài (> 1 năm).
ESC: European Society of Cardiology (Hội Tim mạch châu Âu); TM: Tĩnh mạch; VNTMNK: Viêm nội tâm mạc nhiễm khuẩn.
2.6. Kháng sinh điều trị viêm nội tâm mạc nhiễm khuẩn do vi khuẩn gram âm
- HACEK
- Ceftriaxone 2 g/24h đường TM 1 lần x 4 tuần (van tự nhiên) hoặc trong 6 tuần (van nhân tạo).
- Nếu vi khuẩn không tiết beta-lactamase thì có thể dùng phác đồ: Ampicillin 12 g/24h TM chia 4 – 6 lần kết hợp với gentamycin 3 mg/kg/24h chia 2 – 3 lần (kéo dài trong vòng 4 – 6 tuần).
- Không HACEK (ít gặp): Khuyến cáo nên phẫu thuật sớm hơn là chờ điều trị đủ phác đồ kháng sinh beta-lactam + aminoglycoside trong 4 – 6 tuần.
2.7. Điều trị viêm nội tâm mạc nhiễm khuẩn do nấm
- Thường gặp VNTMNK do nấm ở bệnh nhân mang van nhân tạo, lạm dụng thuốc đường TM và trên người suy giảm miễn dịch; tỷ lệ tử vong tương đối cao (> 50%).
- Điều trị chủ yếu bằng amphotericin B truyền TM phối hợp với phẫu thuật thay van. Thời gian điều trị thường trên 6 tuần. Sau phác đồ điều trị cơ bản ban đầu nên duy trì lâu dài bằng thuốc kháng nấm đường uống (fluconazole với Candida và voriconazole với Aspergillus).
3. MỘT SỐ LƯU Ý
- VNTMNK là bệnh nhiễm khuẩn đặc biệt từ tim lan rộng toàn thân cần điều trị kháng sinh nhanh, mạnh và kéo dài để hạn chế thấp nhất tổn thương các cơ quan đích và không để bệnh tái phát.
- Kháng sinh đầu tay điều trị VNTMNK là các beta-lactam, vancomycin và aminoglycoside.
- Mọi mầm bệnh đều có thể là tác nhân gây bệnh VNTMNK. Trong những trường hợp cụ thể, với những mầm bệnh ít gặp cần tích cực thu thập thông tin về hoàn cảnh phát sinh bệnh, diễn biến lâm sàng, đặc điểm mầm bệnh phân lập cùng với mức độ nhạy cảm thuốc kháng sinh để chuyên khoa Tim mạch phối hợp với các đơn vị Vi sinh lâm sàng, Dược lâm sàng và Truyền nhiễm điều trị bệnh nhân cho hiệu quả.
- Thử nghiệm POET (Partial Oral versus Intravenous Antibiotic Treatment of Endocarditis) trên 400 bệnh nhân viêm nội tâm mạc nhiễm khuẩn người lớn van tim bên trái do một trong các vi khuẩn sau Streptococcus, Enterococcus faecalis, Staphylococcus aureus, tụ cầu coagulase âm tính, tình trạng lâm sàng ổn định, thấy rằng trên nhóm bệnh nhân này, việc chuyển sang điều trị bằng kháng sinh đường uống đem lại kết quả không kém hơn so với đường tĩnh mạch. Tuy nhiên, hiện nay việc sử dụng kháng sinh đường uống trong điều trị VNTMNK chưa được đưa vào trong khuyến cáo.
TÀI LIỆU THAM KHẢO
- Nguyễn Thị Trúc. Viêm màng trong tim. Bách khoa thư bệnh học. Tập 2. Nhà xuất bản Giáo dục. Hà Nội, 2008. Trang 454-60.
- Phạm Mạnh Hùng. “Lâm sàng tim mạch học”. Nhà xuất bản Y học (2019).
- Gilbert Habib, Patrizio Lancellotti, ESC Scientific Document Group, 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC) Endorsed by: European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM), European Heart Journal, Volume 36, Issue 44, 21 November 2015, Pages 3075–3128.
- Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for Healthcare Professionals From the American Heart Association. Circulation 2015;132:1435-1486.
- Grayson, M. Lindsay et al (Ed.) Kucers’ the use of antibiotics: a clinical review of antibacterial, antifungal, antiparasitic and antiviral drugs. 7th Ed. Boca Raton : CRC Press, 2017.
- Sanford Guide. Web Edition. Truy cập tại https://webedition.sanfordguide.com/en
UpToDate®. Web Edition. Truy cập tại: https://www.uptodate.com