1000 câu hỏi tim mạch
1. Rifampicin nên dùng cho tất cả các bệnh nhân bị viêm nội tâm mạc nhiễm khuẩn?
Viêm nội tâm mạc nhiễm khuẩn vẫn còn là một cấp cứu tim lớn.
Điều trị thuốc ban đầu và 1 số người sẽ đề xuất phẫu thuật
(Chủ yếu là thay van). Nhưng các bác sĩ yêu cầu bệnh nhân phải điều trị ổn định vì tỷ lệ tử vong phẫu thuật rất cao ở những bệnh nhân bị nhiễm khuẩn không kiểm soát được và CHF suy tim sung huyết chưa ổn định. Mặc dù có hướng dẫn dùng kháng sinh, nhưng phần lớn viêm nội tâm mạc nhiễm khuẩn điều trị không thành công với phần lớn các bệnh nhân.
Chúng tôi đã quan sát và nghiên cứu thấy rằng rifampicin có tác dụng rất tốt với các bệnh nhân viêm nội tâm mạc nhiễm khuẩn
2. Có thời gian cửa sổ để can thiệp trong đau thắt ngực không ổn định / NSTEMI?
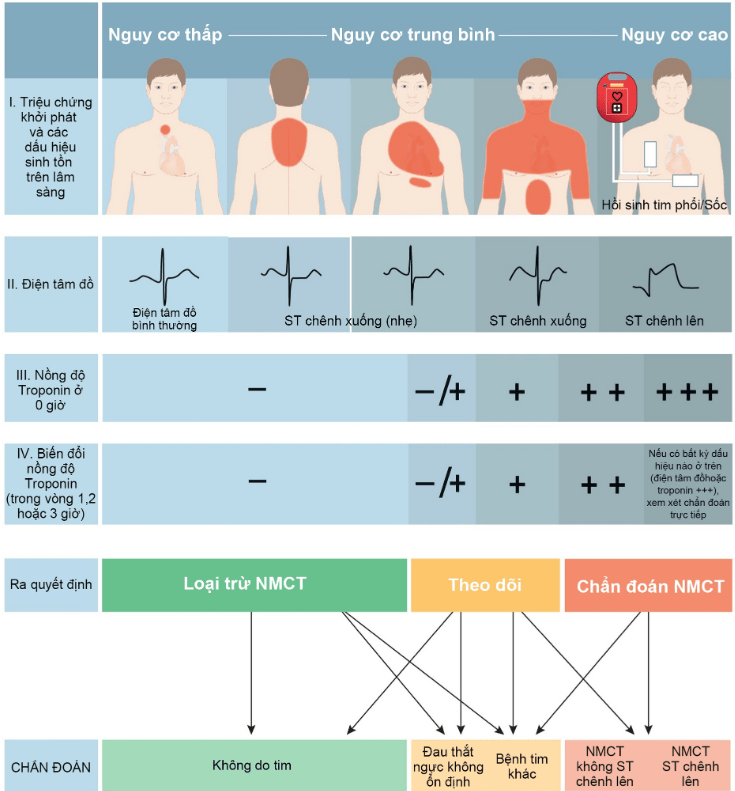
ACS (hội chứng vành cấp) là cấp cứu tim hay gặp nhất. Quyết định điều trị bằng cách tái tưới máu (can thiệp mạch vành qua da PCI hoặc thuốc làm tan huyết khối.)
Các nguyên tắc điều trị UA (đau thắt ngực không ổn định) khác STEMI một cách cơ bản, như không có vấn đề cấp cứu cơ tim trong UA . Mục đích chính là giảm đau và ngăn ngừa nhồi máu. Vì vậy, theo nghĩa hẹp không có thời gian cửa sổ trong đau thắt ngực không ổn định / NSTEMI.
Nhưng 48 giờ là thời gian giới hạn để can thiệp. Sau 48h từ khi xuất hiện triệu chứng thấy không có sự khác biệt lớn giữa can thiệp hay điều trị thuốc tan huyết khối
3. Có xơ vữa động mạch động mạch phổi? chẩn đoán nó?
Xơ vữa động mạch là nguyên nhân gây tử vong liên quan mạch vừa và lớn, hay gặp ở não, động mạch cảnh, động mạch vành, động mạch chủ, thận và động mạch ngoại vi. Nhưng làm thế nào mà không ai nhắc đến động mạch phổi? Một lời giải thích hợp lý là tuần hoàn phổi có áp lực thấp và tối đa dưới 30mmhg. Áp lực này không đủ để gây tổn thương nội mạc có xơ vữa do tăng lipid máu.
lời giải thích khác có thể là do sự khác biệt về cấu trúc so với động mạch chủ. Nhưng ở bệnh nhân tăng áp lực phổi nguyên phát hoặc thứ phát, mặc dù áp lực có cao hơn nhưng hiếm khi xơ vữa động mạch.
4. Thời gian cửa sổ để làm tan huyết khối trong tắc mạch phổi cấp?
Cứu nhu mô phổi không phải là mục tiêu trong điều trị thuyên tắc phổi, Do đó Thời gian cửa sổ là không tưởng.
Có thời gian cửa sổ để làm tan huyết khối trong nhồi máu cơ tim (STEMI). Thời gian cửa sổ này để cứu tim trước khi nó die. Thời gian cửa sổ trung bình trong STEMI là 12 giờ.
Khi nào thì phổi bắt đầu chết trong thuyên tắc phổi? nhu mô phổi chết xảy ra chỉ trong số ít bệnh nhân có thuyên tắc phổi vì Các động mạch phế quản vẫn tiếp tục cung cấp máu nuôi phổi.
Vì vậy, mục tiêu ở đây là để phục hồi tuần hoàn phổi và oxy hóa. Do đó không có thời gian cửa sổ chặt chẽ trong điều trị thuyên tắc phổi.
đồng thuận chung là, người ta có thể cố gắng làm tan huyết khối đến 7 ngày sau khi chẩn đoán thuyên tắc phổi. quá thời gian này sử dụng thuốc làm tan huyết khối không hiệu quả.
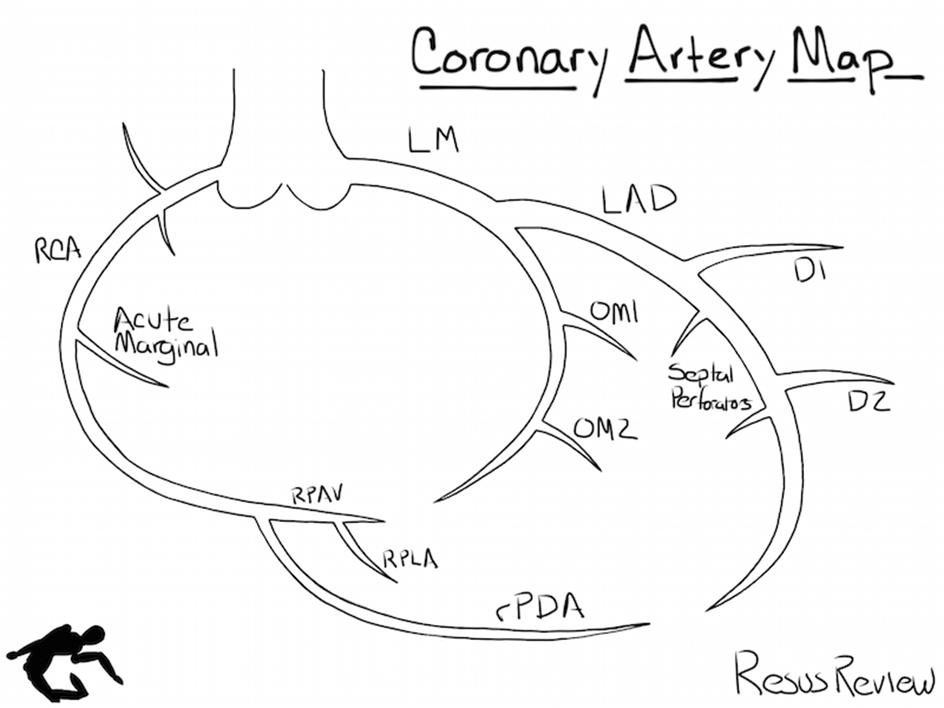
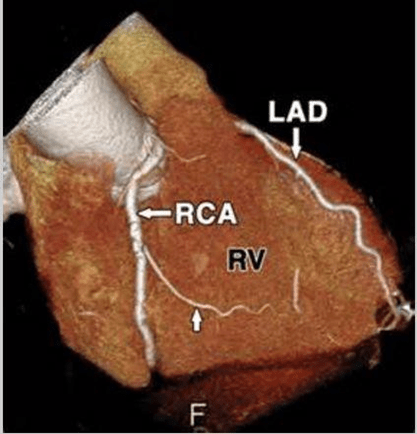
5. Làm thế nào phân biệt đau thắt ngực LAD với RCA?
Hiện đã phát hiện được mối tương quan giữa đau thắt ngực và vị trí tắc của động mạch. Nếu đau thắt ngực lan đến hàm hoặc cổ thường tắc động mạch vành phải RCA, hiếm khi tổn thương LAD / LCX. Nếu đau lan đến vai trái hầu như luôn luôn là tắc RCA
6. Tại sao nhĩ trái không phì đại ngay cả trong hẹp van hai lá nặng?
Tâm nhĩ về cơ bản gồm ít các tế bào cơ để phì đại. Dày nhĩ trái chỉ khoảng 2mm.
về cơ bản chúng được thiết kế một cách thụ động để đổ đầy các tâm thất. Nhưng điều này không phải lúc nào cũng theo sinh lý. Chúng ta gọi nó như là bơm tăng áp và 30% đổ đầy tâm thất do hoạt động của tâm nhĩ trái.
Lý do thứ hai nhĩ trái không phì đại vì có chỗ giải áp (Van an toàn) trong nhĩ trái cụ thể là các tĩnh mạch phổi.
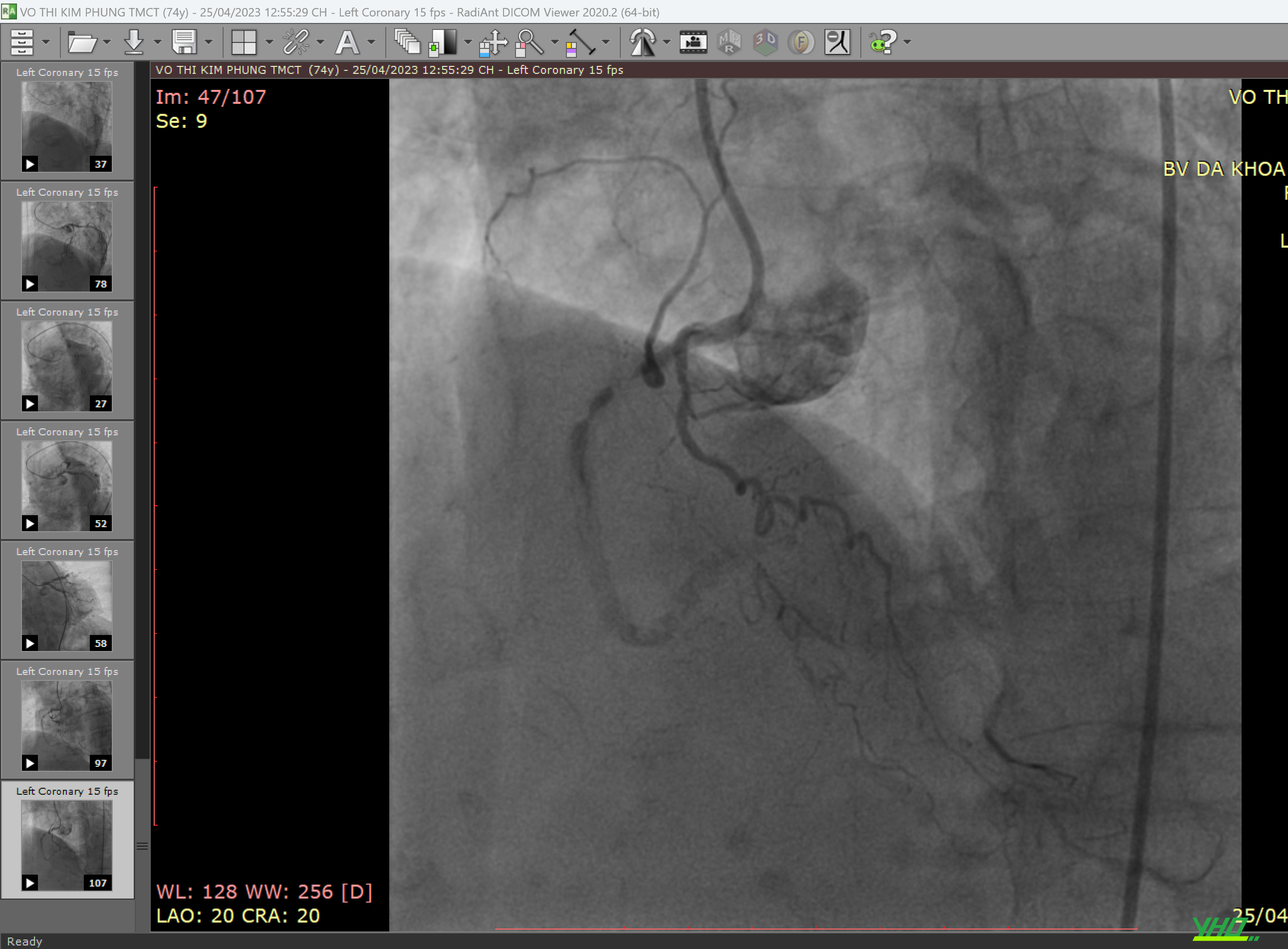
7. Chụp động mạch vành bình thường là gì?
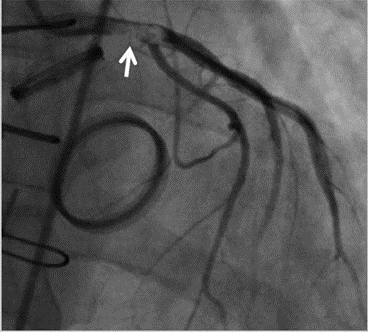
Chụp mạch vành là video ghi lại hình ảnh lòng động mạch sau bơm cản quang. có thời gian gọi là chụp cản quang mạch vành. có thể cung cấp đầy đủ thông tin về tình trạng dòng chảy trong đọng mạch vành, nhưng không thể cho biết tổn thương ở 3 lớp cấu trúc thành động mạch vành.
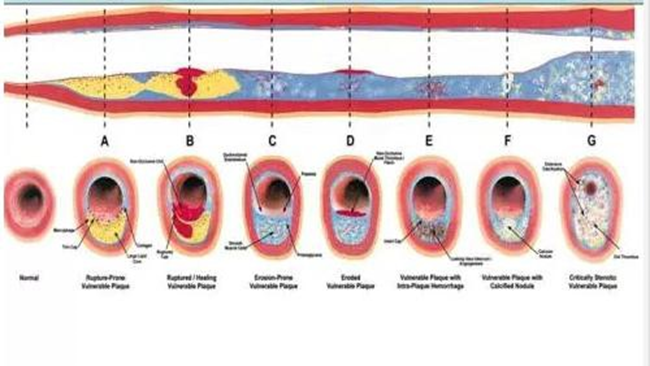
Tổn thương từ a-f có thể bị bỏ qua nếu chỉ chụp mạch vành
Một bệnh nhân chụp mạch vành bình thường có thể có xơ vữa động mạch lan toả hoặc xơ vữa động mạch khu trú trong thành động mạch vành. Những mảng xơ vữa động mạch phát triển ra bên ngoài và không xâm phạm lòng mạch sẽ khó phát hiện khi chụp mạch vành. Những mảng xơ vữa mặc dù không ảnh hưởng huyết động, không ảnh hưởng dòng chảy nhưng có nguy cơ vỡ đột ngột và dẫn đến hội chứng mạch vành cấp.
Vì vậy chụp mạch vành bình thường không bao giờ có thể nói đây là động mạch vành bình thường.
Một người chụp động mạch vành bình thường không có gì đảm bảo rằng ông sẽ không gặp vấn đề về mạch vành trong tương lai tới đây
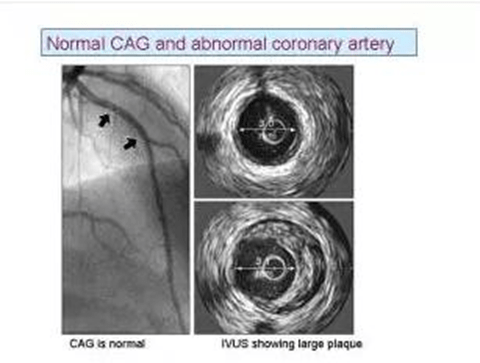
Nếu chụp mạch vành có những hạn chế lớn như vậy thì phải làm sao đây?
Siêu âm lòng mạch (IVUS) có thể cung cấp cho chúng ta hình ảnh về giải phẫu động mạch vành. Khi chụp động mạch vành bình thường, hãy nói với bệnh nhân họ có thể có động mạch vành bình thường. Không nên làm họ lo lắng bằng cách nói rằng, mặc dù CAG bình thường vẫn có thể có xơ vữa động mạch trong động mạch của họ. Lo âu có thể thúc đẩy hội chứng vành cấp.
8. Trớ trêu trong tim mạch – mất nhịp xoang trong trận chiến với rung nhĩ có suy tim!
những phát hiện gần đây thấy rằng, đưa về nhịp xoang không cải thiện chất lượng cuộc sống cũng không làm giảm tỉ lệ đột quỵ. Phát hiện sau đó đã rất ngạc nhiên khi thấy rằng đột quỵ xảy ra do các nguyên nhân khác như SHT, CAD, DM hơn là do rung nhĩ AF. Phòng đột quỵ ở bệnh nhân rung nhĩ bằng thuốc chống huyết khối + theo dõi INR chặt chẽ. Và than ôi, khi chúng tôi đưa AF-CHF về nhịp xoang thấy nó không cải thiện gì ở bệnh nhân có rung nhĩ và suy tim
Tại sao . . . tại sao . . . tại sao ?
Điều này quá vô lý
Rung nhĩ tự nó là một cơ chế để khuếch đại dự trữ tim khi tỷ lệ thất tương đối cao giúp cải thiện các chỉ số tim. Mặc dù tỷ lệ thất tối ưu trong AF là khoảng 80-90 lúc cần thiết nó có tăng lên 120-130. Bệnh nhân CHF độ 3 và AF thường ở ngưỡng này. Điều này không thể có ở những bệnh nhân dùng thuốc kiểm soát nhịp và nhịp không thể tăng đột ngột từ 80 -130.
Vì vậy, AF có thể là một cơ chế an toàn trong CHF khi có bất thường nhịp thất. Rung nhĩ giúp giải cứu tâm thất như một máy tạo nhịp tim tuyệt vời
Có nhiều phương pháp để đưa về nhịp xoang nhưng nó quá cồng kềnh và kết cục vẫn không thay đổi.
Nhưng nên nhớ răng, thay đổi nhịp như nào đi nữa cuối cũng vẫn sẽ quyết định bởi chức năng LV, chức năng của van hai lá…
Nhiều khuyến cáo nên khôi phục và duy trì nhịp xoang ở bệnh nhân rung nhĩ và suy tim. Phương pháp này dựa một phần vào số liệu chỉ ra rằng rung tâm nhĩ là một yếu tố dự báo tử vong ở bệnh nhân suy tim và gợi ý rằng đàn áp rung nhĩ có thể ảnh hưởng đến kết quả. Tuy nhiên, những lợi ích và rủi ro của phương pháp này chưa được nghiên cứu đầy đủ.
Chúng tôi đã tiến hành một nghiên cứu đa thử nghiệm ngẫu nhiên so sánh việc duy trì nhịp xoang (kiểm soát nhịp) với kiểm soát tần số thất ở những bệnh nhân phân suất tống máu thất trái còn 35% hoặc thấp hơn, có triệu chứng của suy tim sung huyết và rung tâm nhĩ. Theo dõi tử vong do nguyên nhân tim mạch.
Nghiên cứu trên 1376 bệnh nhân trong thời gian trung bình là 37 tháng.
Kết luận bệnh nhân rung nhĩ / suy tim sung huyết, việc điều chỉnh nhịp thường xuyên không làm giảm tỷ lệ tử vong do nguyên nhân tim mạch so với nhóm chỉ kiểm soát tần số
9. Đừng hoảng hốt khi bạn bị chẩn đoán có vấn đề động mạch vành trái chính sau chụp mạch vành. Mất tiền oan đấy!
Chẩn đoán tổn thương mạch vành trái khá phổ biến trong chụp mạch vành. Đây là thói quen và cũng là chẩn đoán vô thưởng vô phạt đáng báo động ở các phòng can thiệp tim mạch cũng như các bác sĩ tim mạch và phẫu thuật viên. Những tổn thương nhánh trái thường gặp ở bệnh nhân đau thắt ngực ổn định mãn tính với các triệu chứng ổn định
Có một quy tắc bất thành văn, chứ không phải ép buộc, tổn thương mạch vành nhánh chính trái khi chụp mạch chưa cần cấp cứu
Câu hỏi ở đây là “chúng ta có nên mặc định tổn thương nhánh động mạch vành chính trái như 1 trường hợp cấp cứu”?
Không thực sự, đặc biệt khi nó xảy ra trong một cơn đau thắt ngực ổn định. Có thể chờ
đợi, theo dõi thêm. Trên thực tế cũng thừa nhận rằng, bắc cầu chủ vành thường không hiệu quả tốt khi làm cấp cứu.
bài này là để truyền tải thông điệp, mặc dù tổn thương nhánh chính trái mạch vành là nguy cơ nguy hiểm nhưng không có nghĩa là phải hoảng loạn và phải làm cấp cứu. Đã có quá nhiều bệnh nhân tử vong khi cấp cứu dấu hiệu hiển nhiên có trong bệnh đau thắt ngực ổn định này.
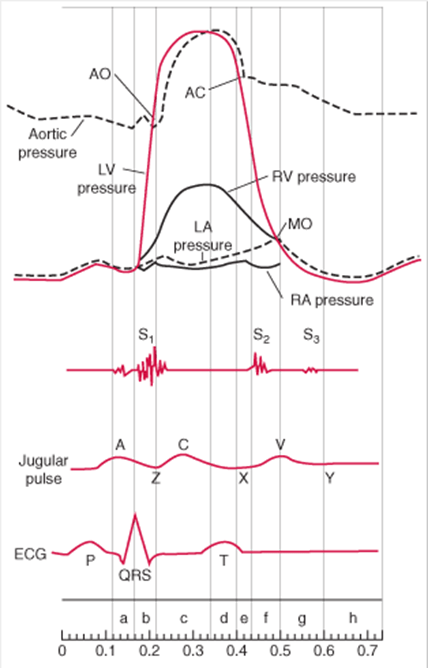
10. Mạch hụt (pulse deficit ) là gì? cơ chế? nó xảy ra ở đâu?
Mạch hụt là dấu hiệu lâm sàng trong đó người ta thấy có sự khác biệt giữa nhịp tim (nhịp mỏm tim hoặc tiếng tim) và mạch ngoại vi . Đây là trường hợp tim co mà mạch không đến được ngoai vi xảy ra trong các tình huống sau.
1. Rung tâm nhĩ.
2. nhịp thất lạc chỗ thì tâm trương rất sớm
3. Một số bệnh nhân có máy tạo nhịp tim.
Cơ chế ở đây là các cơn co thắt tâm thất quá yếu và không thể mở van động mạch chủ, nhưng lại đủ để đóng van hai lá. Để mở van động mạch chủ nó phải tạo ra áp lực ít nhất 60-80 mmHg, trong khi van hai lá đóng ngay cả khi LV tạo ra áp lực 8-14mmhg. Vì vậy gián đoạn tiếng thứ 2 mất trong khi tiếng thứ 1 vẫn còn, tạo thành nhiều âm thanh ở tim nhưng đếm được ít xung ở ngoại vi.
Tại sao một số các cơn co thắt của LV quá yếu không đủ để mở van động mạch chủ? Bởi vì khoảng RR khác nhau, làm thời gian đổ đầy tâm thất cũng khác nhau, thời gian tâm trương liên tục thay đổi một số thì tâm trương quá ngắn và LV hầu như không được đổ đầy, nên lực co LV, chiều dài sợi cơ và thể tích thất trái cuối thì tâm trương yếu nên không đủ để mở van động mạch chủ
Hiện nay theo quan sát doppler, hiện tượng có dòng chảy đảo ngược ở thất trái trong rung nhĩ giải thích mạch hụt.
http://www.ncbi.nlm.nih.gov/pubmed/3221309
Ý nghĩa lâm sàng mạch hụt?
Hiện nay không có ý nghĩa lâm sàng lớn về hiện tượng này. Tuy nhiên, một thầy thuốc tinh tế sẽ nhận ra có rối loạn chức năng cơ bản của thất trái. Ở những bệnh nhân có máy tạo nhịp, mạch hụt cho thấy có sự cố máy tạo nhịp tim .1 vài bệnh nhân có chèn ép tim & mạch cấp sẽ làm huyết áp tâm thu giảm quá thấp làm cho khi bắt mạch ngoại vi yếu hoặc không sờ thấy, bắt chước mạch hụt nếu không để ý
11. Khó thở khi nằm trong suy tim giai đoạn cuối
Trong khi khó thở kịch phát về đêm là một dấu hiệu sớm của suy tim, thì khó thở khi nằm (orthopnea) là một biểu hiện muộn của suy tim. Đây là triệu chứng chủ yếu do phân bố lại thể tích từ tuần hoàn hệ thống sang tuần hoàn phổi khi bệnh nhân nằm.khi siêu âm tim đầu giường, chúng tôi đã phát hiện ra có sự thay đổi theo tư thế trong chức năng tâm trương của thất trái.
Nhiều bệnh nhân đổ đầy thất trái hạn chế khi bệnh nhân nằm. Trong khi ngồi dậy thì lại trở về bình thường . Chứng tỏ thực tế mọi bệnh nhân rối loạn chức năng tâm thu nặng cũng có rối loạn chức năng tâm trương đáng kể tại một số thời điểm của bệnh
12. Tại sao ngất hiếm khi gây tử vong?
Ngất theo định nghĩa là sự mất ý thức thoáng qua của ý thức do giảm tưới máu não và mất trương lực cơ, bệnh nhân ngã nhưng hồi phục hoàn toàn và tỉnh nhờ hỗ trợ hoặc tự tỉnh. Mạch máu và tim thường không bị ảnh hưởng. Nếu bệnh nhân không hồi phục sau ngất, có thể đây là đột quỵ hoặc anh ta sẽ không bao giờ dậy nữa (ngừng tim đột ngột) . Vì vậy, về mặt định nghĩa, tất cả các bệnh nhân ngất sẽ không thể tử vong.
Có mối liên kết giữa ngất và ngừng tim đột ngột (SCD) ở các bệnh nhân của rối loạn nhịp thất?
Một số trường hợp có hội chứng QT kéo dài có thể gây tử vong đột ngột đặc biệt là ở trẻ em. Một bệnh nhân chức năng VT không ổn định có thể gây ngất. Trong số ít này, có thể tiến triển rung thất và tử vong
Làm thế nào phát hiện ngất trong nhồi máu cơ tim cấp tính?
Ngất vô cùng hiếm gặp trong cơn nhồi máu cơ tim cấp tính.
Ngất là tiền triệu của tai biến mạch não?
Ngất gặp ở bệnh nhân có bệnh lý động mạch cảnh và mạch máu não. Nhưng khi xuất hiện cơn đột quỵ thì không coi đó là ngất
Có nhiều nguyên nhân gây ngất Nhưng đơn giản là
A.Tim
– loạn nhịp, chậm hoặc nhanh
– Cơ học (van tim tắc nghẽn và bệnh liên quan cấu trúc tim khác)
B. Không do tim
Phản xạ phế vị (90% trường hợp ngất)
C. Chuyển hóa Thiếu máu
Hạ đường huyết Thiếu oxy
* Nguyên nhân chuyển hóa cùng với phản xạ phế vị (thần kinh tim) chiếm phần lớn nguyên nhân ngât .
Làm thế nào để tiếp cận một bệnh nhân bị ngất?
Đầu tiên, cần phải xác nhận đây thực sự là ngất. cần hỏi gia đình tiền sử của bệnh nhân
.ngất do tim thường đột ngột, phản xạ phế vị thường có yếu tố môi trường hoặc tình cảm. cần làm ecg, siêu âm tim, holter
Ngất là một trong những triệu chứng phổ biến trong tim mạch và điều trị nói chung. ngất không bao giờ gây tử vong nhưng cần loại trừ nhịp nhanh và nhịp chậm là mục tiêu quan trọng. (20-30%) không xác định các nguyên nhân dù có các công cụ chẩn đoán hiện đại. ngất không rõ nguồn gốc được xếp cùng nhóm liên quan thần kinh tim
Mnemonic
I GET SMASHED
• I: idiopathic
• G: gallstones
• E: ethanol (alcohol)
• T: trauma
• S: steroids
• M: mumps (and other infections) / malignancy
• A: autoimmune
• S: scorpion stings/spider bites
• H: hyperlipidaemia/hypercalcaemia/hyperparathyroidism (metabolic disorders)
• E: ERCP
• D: drugs
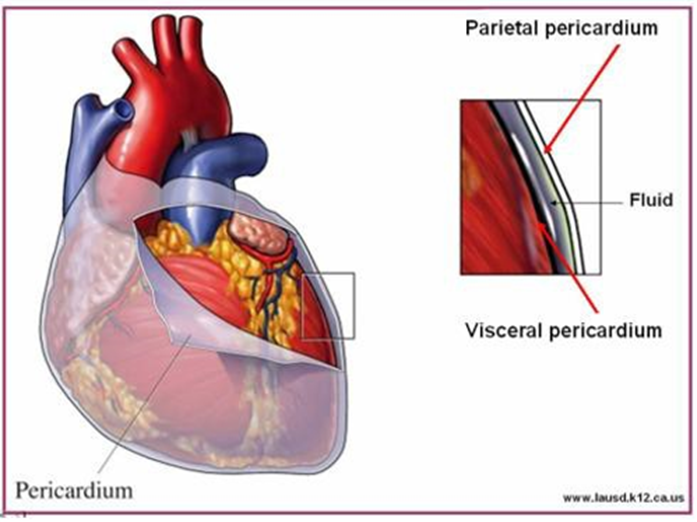
13. Có sự liên tục giữa khoang màng phổi và màng ngoài tim?
Màng phổi và màng ngoài tim có cấu trúc giải phẫu tương tự nhau trong lồng ngực.
Cả hai đều chứa nồng độ tối thiểu dịch sinh lý. Người ta thấy có hiện tượng viêm cùng lúc của cả 2 trong viêm thanh mạc hoặc bệnh ác tính. Trong suy tim cũng tràn dịch cả 2 màng do áp lực tĩnh mạch tăng lên.
Nhưng luôn luôn có một mối quan hệ kỳ lạ giữa hai khoang này. Trong thực tế, tràn dịch màng phổi gặp nhiều hơn tràn dịch màng ngoài tim. Dẫn lưu dịch màng phổi giúp giảm bớt dịch màng ngoài tim rất tốt.
Người ta thấy rằng có 1 số kênh bạch huyết thông thương giữa 2 khoang.
14. Cơ chế tiếng cọ màng ngoài tim là gì?
Tim được bao phủ bên ngoài bởi hai lớp màng ngoài tim. khoang màng ngoài tim được hình thành giữa các đỉnh và các lớp nội tạng của màng ngoài tim. Đó là một không gian hẹp mà thường được bôi trơn bằng lớp dịch sinh lý lên đến 25ml. Khi hai bề mặt mô tiếp xúc nhau, báo hiệu bởi tiếng cọ màng ngoài tim. Thường gặp trong viêm, tiếng cọ màng ngoài tim là một dấu hiệu lâm sàng đặc biệt nhưng không thường gặp
Điều kiện lâm sàng thường gặp
Viêm màng ngoài tim cấp tính
Viêm màng ngoài tim do tăng urê huyết. viêm màng ngoài tim do thấp khớp sau nhồi máu cơ tim
– Màng ngoài tim có hai lớp. Có bốn khả năng xuất hiện tiếng cọ màng ngoài tim.
1. giữa hai lớp màng ngoài tim
2. giữa màng ngoài tim lá tạng và lớp thượng tâm vị của trái tim
3. Giữa đỉnh màng ngoài tim và thành ngực
4. màng ngoài tim chà xát với màng phổi liền kề
Các cơ chế thứ hai và thứ ba là rất hiếm.
Vị trí
Bờ xương ức trái, khoang liên sườn 2 hoặc 3. Tốt nhất nghe trong tư thế ngồi, nghiêng về phía trước thì hít vào. Nhiều âm thanh có thể lẫn như s3 hoặc s4.
Cơ chế tiếng cọ màng ngoài tim trong giai đoạn sau nhồi máu cơ tim là gì?
Sự có mặt của tiếng cọ màng ngoài tim sau nhồi máu cơ tim gợi ý có tổn thương xuyên thành tim hoặc ít nhất có tổn thương thượng tâm vị. Dấu hiệu này rất quan trọng vì khi có cọ màng ngoài tim làm tăng nguy cơ vỡ thành và tràn dịch do xuất huyết nếu sử dụng thuốc chống đông.
Mối quan hệ giữa tràn dịch màng tim và tiếng cọ màng ngoài tim là gì?
Nói chung tiếng cọ mất khi xuất hiện tràn dịch màng ngoài tim nhưng điều này chưa hẳn đã đúng. Tiếng cọ sau khi đụng dập ngực và gãy xương sườn có thể không có tràn dịch. Tiếng cọ màng ngoài tim có liên quan với bệnh lý viêm cấp tính gây đau đớn nặng nề (như viêm màng phổi) .Nhưng viêm màng ngoài tim có liên quan với bệnh viêm mạn tính ít khi gây đau. lý do chính xác chưa được biết.
Tiếng cọ màng phổi- màng tim là gì?
Thực thể lâm sàng này vẫn chưa được xác định, thường được giảng dạy bởi các giáo sư kỳ cựu trong lâm sàng nghe tim. Có thể nghe thấy trong viêm màng phổi ở đoạn giữa vòm hoành hoặc không có tràn dịch màng ngoài tim ở bệnh nhân viêm phổi không điển hình.
15. Amlodipin chống đau thắt ngực
Amlodipin là thuốc chống tăng huyết áp phổ biến nhất được sử dụng trên toàn thế giới có tác động rất lớn đến lưu lượng máu qua động mạch vành. 3 thập kỉ trước đây nifedipine đã được biết đến với đặc tính chống đau thắt ngực cực kì hiệu quả. Sau đó amlodipine đã được giới thiệu với các tác dụng gần như tương tự. Nhưng trong những năm qua, amlodipin được dùng chủ yếu như thuốc chống tăng huyết áp và dần dần nhiều bác sĩ tin rằng nó chỉ là một loại thuốc dùng nếu huyết áp tăng cao.Trong thực tế, các bác sĩ nói chung hiện nay khi được hỏi về amlodipine thì không ai thừa nhận từng thuốc này như một loại thuốc chống đau thắt ngực. Và vài người trong số họ đã rút amlodipine khi bệnh nhân có đau thắt ngực!
Tại sao tác dụng chống đau thắt ngực của amlodipin lại ảm đạm không ai dùng vậy? Câu trả lời là quá đáng tiếc! nhiều phác đồ chính thống trong tim mạch đã bỏ qua thuốc cực kì đặc biệt này. Amlodipin, vẫn có thể được sử dụng như một loại thuốc chống đau thắt ngực đặc biệt ở bệnh nhân đau thắt ngực kèm nhịp chậm, rối loạn chức năng thất trái đáng kể. Amlodipine và nifedipine còn dùng trong đau thắt ngực do co thắt mạch máu mà chống chỉ định dùng chẹn beta.
16. Không có dòng chảy ngược (reflow) là gì? Cơ chế là gì?
Không có dòng chảy ngược là thuật ngữ được sử dụng chủ yếu trong các phòng can thiệp, ngay cả sau khi thông và đặt stent động mạch vành lưu lượng máu mạch vành không được khôi phục đến cơ tim. Điểm nhấn mạnh ở đây là máu vượt qua tắc nghẽn nhưng không xâm nhập vào phần cơ tim mà động mạch vành cung cấp. Vì vậy, tình trạng nghịch lý ở đây động mạch đã thông nhưng cơ tim đóng cửa không tiếp nhận máu chảy đến. Điều này được gọi là không có dòng chảy ngược. Trên thực để tránh nhầm lẫn, nó được gọi là “không có dòng chảy” (Sau PCI). Trong thực tế không có dòng chảy có thể tiềm tàng nguy cơ PCI thất bại. Còn 1 tên khác là phân ly thượng tâm vị – cơ tim.
Cơ chế
Trường hợp kỳ lạ động mạch vành mở nhưng cơ tim đóng kín!
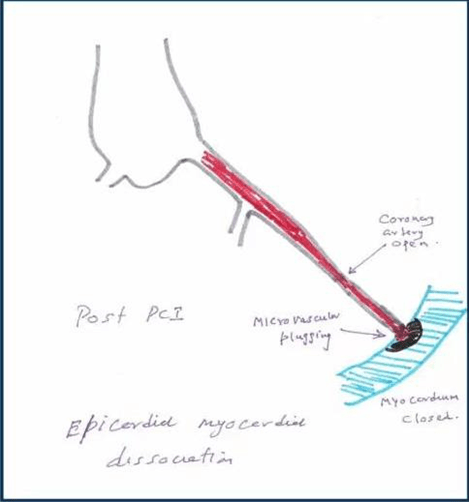
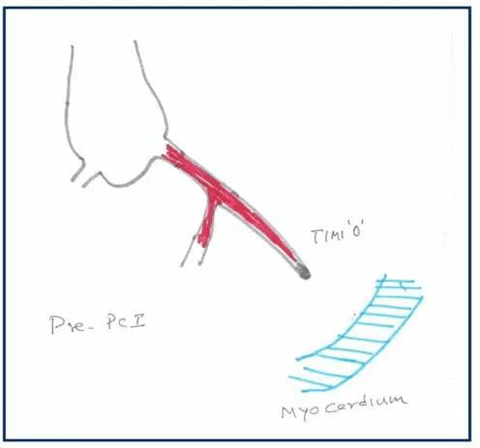
Tắc mạch nhỏ động mạch vành chủ yếu do huyết khối và xơ vữa động mạch, phù nề cơ tim, co thắt vi mạch máu
Nó có thể xảy ra ở đâu?
Thường xảy ra sau nong mạch chính.
xảy ra sau dùng thuốc làm tan huyết khối trong STEMI. Có thể xảy ra trong ghép tĩnh mạch.
Làm thế nào để bạn nhận ra không có dòng chảy reflow?
Trong phòng can thiệp sẽ phát hiện khi chụp mạch kiểm tra. độ tương phản siêu âm tim, PET, ECG thấy sau MI có ST chênh lên liên tục
Điều trị.
Vô cùng khó khăn. Hầu hết các thuốc giãn vành đã được dùng thử. (Nitrates, Nicorandil, chẹn canxi, vv) .thành công dưới 30%. Áp lực cao bơm nước muối sinh lý bên trong động mạch vành được nhiều nơi khuyến cáo.1 số khác e rằng sẽ rất nguy hiểm khi làm vậy. Vì vậy, việc phòng ngừa là chính. Tránh làm PCI phức tạp, tổn thương huyết khối. Sử dụng thiết bị hút huyết khối (Medtronic). ..
17. Đáp ứng khác nhau với thuốc làm tan huyết khối của động mạch vành phải và trái?
Dùng thuốc làm tan huyết khối là điều trị cụ thể cho nhồi máu cơ tim cấp tính. Tỉ lệ thất bại khoảng (30-40%). ST chênh 120 phút sau khi dùng thuốc làm tan huyết khối đồng nghĩa với đã thất bại. Tỉ lệ thất bại thường gặp ở động mạch vành trái.
Trong một nghiên cứu đơn giản, chúng tôi đã ghi nhận bệnh nhân MI thành dưới hiếm khi có ST chênh dai dẳng và thuốc làm tan huyết khối điều trị thành công trong phần lớn các bệnh nhân (Ngoại trừ số ít bệnh nhân có liên quan MI thành bên)
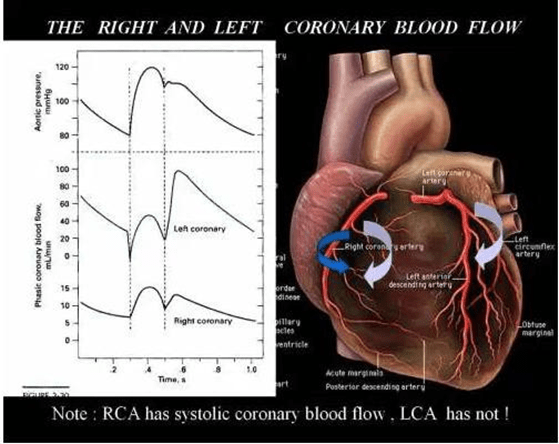
Cơ chế làm tan huyết khối trong động mạch vành phải tốt hơn trái rất đơn giản. Trong thời gian cửa sổ, có liên quan trực tiếp với áp lực và thời gian tiếp xúc giữa các thuốc tiêu sợi huyết và huyết khối. Trong lưu thông mạch vành bên phải dòng máu chảy liên tục ở cả tâm thu và tâm trương tạo điều kiện cho việc cung cấp tối đa các tác nhân tan huyết khối. Hơn nữa gradient áp suất tạo bởi cơ tim trong thất phải cao hơn đáng kể so với áp suất do cơ tim thất trái.

18. Trong nhịp nhanh sốc điện không hiệu quả và chống chỉ định
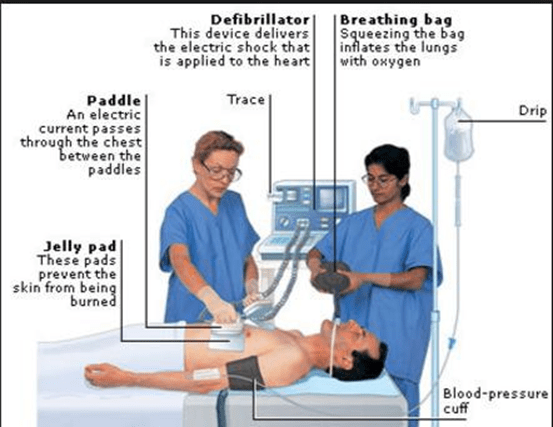
Sốc điện có hiệu quả ngay lập tức trong rất nhiều các rối loạn thất và nhĩ nguy hiểm. Chúng ta vẫn thường được dạy, bất kỳ khi nào huyết động không ổn định, nhịp tim nhanh
― trơ‖ với điều trị nội khoa sẽ đáp ứng sốc điện. Nhưng cũng nên nhớ rằng điện được trong thực tế cũng được coi như một loại thuốc! nó sẽ được dùng ở liều thích hợp.
Sự thật là hầu hết các rối loạn nhịp tim đều phản ứng với sốc điện, có rất ít rối loạn không đáp ứng hoặc đáp ứng kém. Và trong những rối loạn nhịp này, sốc điện không chỉ không hiệu quả mà có thể thúc đẩy rung thất. Rối loạn nhịp có tăng cường tính tự động và nhịp nhanh có nhịp lạc chỗ rất khó giải quyết nhịp nhanh bằng sốc điện.
Những rối loạn nhịp mà sốc điện không hiệu quả A.nhịp nhanh nhĩ đa ổ
B. rối loạn nhịp do Digoxin. Bệnh nhân đang dùng digoxin sẽ làm tăng tính tự động.nếu sốc điện sẽ thấy rõ những ổ lạc chỗ
C. ở người già có rung nhĩ và rối loạn chức năng nút xoang có thể rấtnguy hiểm nếu sốc điện làm cho nút xoang đi vào trạng thái ngủ say
D. trong cơn VT, nếu nhiều hơn ba lần sốc điện trong vòng một phút, VT sẽ kéo dài vĩnh viễn và các liệu pháp điện sẽ thất bại. Những bệnh nhân này sẽ yêu cầu dùng những loại thuốc chuyên sâu (như magiê, bretyllium…)
E. Và cuối cùng, với nhịp xoang nhanh (bất kể tỷ lệ nào) là một chống chỉ định tuyệt đối cho sốc điện
Verapmil thường có hiệu quả trong nhịp nhanh nhĩ đa ổ MAT nhưng có thể gây thiếu oxy máu và toan. Với loạn nhịp do digoxin có thể dùng phenytoin
Phải làm gì khi sốc điện không hiệu quả?
Đây sẽ là một tình huống khó khăn và tự hỏi phải làm gì tiếp theo ? Đặt máy tạo nhịp
Dùng sóng cao tần
19. Điều gì sẽ xảy ra nếu bạn vô tình dùng thuốc tan huyết khối cho hội chứng tái phân cực sớm?
Chỉ định dùng thuốc làm tan huyết khối khi có ST chênh trong MI chủ yếu được xác định bởi lâm sàng và điện tâm đồ. ST chênh cao hơn 1mm trong hai chuyển đạo chính
liên tiếp kèm nghi ngờ lâm sàng hội chứng vành cấp tính đòi hỏi dùng thuốc làm tan huyết khối ngay lập tức.
hội chứng tái phân cực sớm (ERS) là một dạng na ná giống STEMI điển hình. Trong ERS, đoạn ST chênh lên ở nhiều chuyển đạo đặc biệt ở các chuyển đạo trước tim.được cho là biến thể di truyền gặp ở 3-5% dân số liên quan tới việc kích hoạt kênh kali
Nếu bệnh nhân vào cấp cứu vì đau ngực, sẽ có thể nhầm nó với ACS. Và sẽ cho dùng ngay thuốc làm tan huyết khối
Điều gì thực sự có thể xảy ra nếu bạn vô tính dùng thuốc làm tan huyết khối?
Nói chung không có gì xảy ra. Nhưng khi dùng thuốc, những thay đổi trên điện tâm đồ vẫn tồn tại. Và troponin sẽ âm tính, siêu âm tim sẽ không thể cho biết được bất kỳ sự thay đổi nào trong rối loạn vận động các thành.
20. Có phải chúng ta phải chịu trách nhiệm nếu dùng tan huyết khối gây chảy máu – đột quỵ?
Giống như khi bạn muốn bắt một tội phạm thực sự , bạn phải giữ tất cả các nghi phạm bị nghi ngờ trước khi để họ đi. Đáng tiếc là trong trường hợp này, một số người vô tội có thể bị đe doạ tính mạch bởi những người thi hành pháp luật.
Tương tự như vậy nếu một bệnh nhân có ERS tiến triển trong co thắt thực quản nặng và đau thắt ngực điển hình thì hoàn toàn chắc chắn để dùng thuốc làm tan huyết khối Làm thế nào để ngăn chặn dùng thuốc làm tan huyết khối do sơ xuất trong ERS?
Luôn luôn nhìn lại ECG trước đó. Trong ERS đoạn ST thường lõm hướng lên trên.
ACC / AHA hướng dẫn STEMI, biết được thực tế này nhưng vẫn còn những lời khuyên dùng thuốc làm tan huyết khối cho tất cả các ST chênh lên không phân biệt hình thái của ST. Đây có thể không phải cố ý, có thể họ sợ những trường hợp STEMIs lại chẩn đoán nhầm thành ERS dẫn đến không dùng thuốc làm tan huyết khối.
Những cập nhật mới nhất về ERS là gì?
Nhiều dữ liệu cho thấy ERS không phải là thứ phát. 1 vài trường hợp hoàn toàn lành tính (Ngay cả một phần nhỏ dân số cũng có thể mắc ERS với số lượng đáng kể) có thể có sự chồng lấp lên hội chứng Brugada và có thể dễ bị loạn nhịp thất nguy hiểm khi kèm theo thiếu máu cục bộ hoặc stress khác.
21. Ưu điểm của phì đại thất trái (LVH)
Phì đại thất trái là một trong những chẩn đoán lâm sàng thường gặp bằng ECG hoặc siêu âm tim. Nó có thể hàm ý một tình trạng bệnh lý hoặc dấu hiệu của trái tim khỏe mạnh như trong phì đại sinh lý ở các vận động viên.
LVH do tăng huyết áp lành tính?
Không thực sự như vậy, LVH đã được chứng minh là một yếu tố nguy cơ tim mạch độc lập. (Nghiên cứu Framingham nổi tiếng) Hơn nữa LVH có thể dẫn đến rối loạn chức năng tâm trương và nguy cơ tăng suy tim. Nhưng một thầy thuốc tinh tế sẽ rất vui và đánh giá cao LVH trong hội chứng vành cấp. Điều này đã được kiểm chứng lâm sàng phù hợp. (Chúng ta sẽ gọi nó là lớp ACC / AHA bằng chứng C. Xem lại đã up về 3 phân loại theo bằng chứng của ACC/AHA)
LVH là của quý trong ACS?
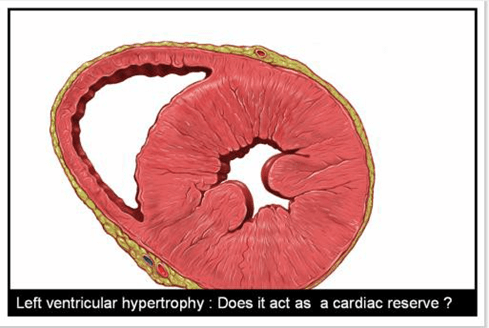
Tim phì đại dễ tổn thương do thiếu máu cục bộ, nhưng thực sự nó không bị tổn thương nhiều. Một khả năng khác là trong LVH các tế bào cơ kháng tình trạng giảm oxy tương đối tốt. Bệnh nhân LVH hiếm khi thấy khiếm khuyết vận động thành đáng kể sau STEMI. Đây có lẽ vì hoại tử xuyên thành gần như không bao giờ có thể xảy ra ngay cả khi MI lan rộng. Điều này cũng thấy trên thực tế là ECG những bệnh nhân LVH hiếm khi tiến triển có sóng Q sau STEMI, ST chênh lên dai dẳng và dùng thuốc làm tan huyết khối thất bại cũng ít gặp với bệnh nhân có LVH.
LVH có khả năng giúp miễn dịch tương đối chống lại sự tiến triển của sốc tim. Sốc tim hiếm khi có thể xảy ra với LVH. Trong một phân tích lâu dài với số lượng lớn, chúng tôi thấy không ai trong số các bệnh nhân LVH tiến triển thành sốc tim sau STEMI.
Bệnh nhân LVH cũng được bảo vệ tránh được nguy cơ vỡ thành tim
“Thiếu bằng chứng không làm nên sự thật, đúng là chuyện hoang đường”
Nhiều khi áp dụng 1 cái gì trong điều trị là bị vặn vẹo hỏi lấy ở đâu, ai áp dụng chưa, chỗ nào, có uy tín không… đúng là suy nghĩ quá tầm thường
LVH dù là bệnh lý hay sinh lý, đều có tác dụng bảo vệ cơ tim, hạn chế biến chứng của STEMI. Nên nếu có bị phì đại thất trái hãy nên nhớ rằng mình còn hạnh phúc chán.
22. Tại sao thuốc làm tan huyết khối chống chỉ định trong đau thắt ngực không ổn định?
Huyết khối động mạch vành gây hội chứng mạch vành cấp (cả STEMI và NSTEMI.) Nhưng thuốc làm tan huyết khối là liệu pháp điều trị dùng trong STEMI và chống chỉ định ở NSTEMI / UA.
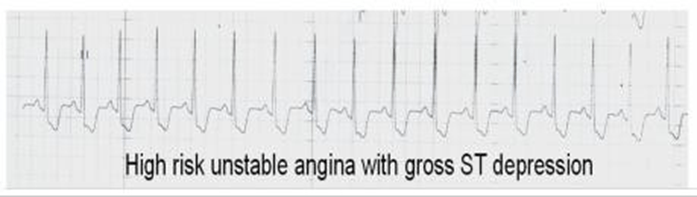
Tại sao có nghịch lý hiển nhiên này? Sự khác nhau cơ bản giữa UA và AMI là gì? Trong STEMI có tắc đột ngột và toàn bộ một động mạch vành thường do huyết khối. Mục tiêu trước mắt là mở thông mạch máu. Mỗi phút giây đều cực kỳ quan trong vì quá trình liên tục hoại tử do thiếu máu cục bộ. Vì vậy, làm tan huyết khối (hoặc cụ thể hơn là hủy fibrin nên cố gắng ngay lập tức). Lựa chọn khác là nong mạch vành sẽ không được thảo luận ở đây.
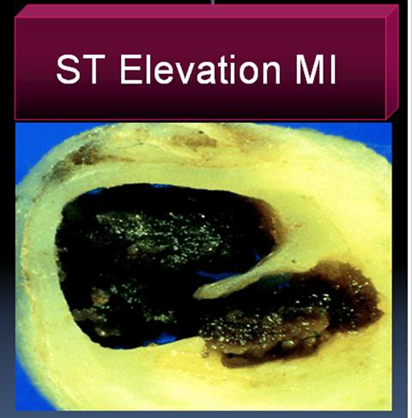
Huyết khối trong STEMI là RBC & fibrin thường là một cục máu đỏ. Các thuốc tiêu sợi huyết như streptokinase, yếu tố hoạt hoá mô palsminogen, (TPA) Reteplace, Tenekteplace … đã được thử nghiệm và hình thành nền tảng xử trí STEMI. Tác dụng không mong muốn như đột quỵ khi dùng thuốc làm tan huyết khối đã được công nhận, nhưng chỉ số lợi ích- rủi ro thiên về dùng thuốc làm tan huyết khối trong hầu hết các tình huống trừ bệnh nhân rất cao tuổi và tiền sử đột quỵ hoặc rối loạn chảy máu.
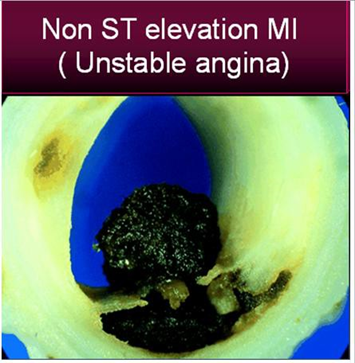
đau thắt ngực không ổn định là bạn đồng hành thân thiết của STEMI. Nhiều lần nó đi trước STEMI thường được gọi là đau thắt ngực tiền nhồi máu. Trong giai đoạn này lưu lượng máu trong động mạch vành di chuyển chậm chạp và bệnh nhân đau thắt ngực tiến triển. Nhưng không giống như STEMI có tắc hoàn toàn, tình trạng cấp cứu cơ tim không phải là mục tiêu điều trị nhưng phòng MI trở thành mục tiêu. mặc dù huyết khối có mặt
Trong UA, nhưng kinh nghiệm cho thấy thuốc làm tan huyết khối không có tác dụng gì trong việc ngăn ngừa nhồi máu
Tại sao thuốc làm tan huyết khối không tác dụng gì trong UA?
1. trong đau ngực không ổn định UA tắc nghẽn thường do mảng bám hơn là huyết khối gây tắc hoàn toàn lòng mạch nên thuốc này ít có tác dụng.
2. Ngay cả khi hiện tại có huyết khối, nó thường có mảng bám trong lòng mạch hạn chế tác dụng của thuốc lên cục huyết khối.
3. Hơn nữa UA / NSTEMI tắc chậm và dần dần (Không giống như tắc mạch đột ngột và toàn bộ trong STEMI) các tiểu cầu bị tổn thương và bị mắc kẹt bên trong . mảng bám huyết khối trong UA chủ yếu là màu trắng. Thông thường, lõi trung tâm là tiểu cầu và từ đó có thể tiến triển thành cục máu đông
4. thuốc làm tan huyết khối tác dụng như một tác nhân tiêu sợi huyết, do đó sẽ khó khăn khi li giải cục máu đông nhiều tiểu cầu. Đây cũng là rủi ro nhỏ khi các thuốc này ly giải nắp fibrin làm lộ lõi tiểu cầu sẽ kích hoạt tạo cục máu đông mới. Điều này đã được minh chứng trong nhiều thử nghiệm (đặc biệt TIMI 3b) Vì vậy, nếu chúng ta dùng thuốc làm tan huyết khối trong UA, sẽ có thể gây hội chứng ACS thường gặp trong giai đoạn hậu tan huyết khối.
5. UA là bán cấp cứu không cần chạy đua với thời gian để cứu vãn cơ tim. Cân nhắc lợi – hại thì không nên dùng thuốc làm tan huyết khối
23. Làm thế nào thuốc lợi tiểu giúp giảm huyết áp?
Thuốc lợi tiểu là thuốc chống tăng huyết áp.Thiazide thường được kê đơn nhất nhiều thập kỷ trước đây, ít phổ biến trong những năm gần đây, một lần nữa lại được khuyến cáo nên dùng sau khi công bố thử nghiệm ALLHAT. Bây giờ thuốc lợi tiểu đã trở thành thuốc được lựa chọn đầu tiên trong hầu hết các bệnh tăng huyết áp trừ chống chỉ định cụ thể.
Các thiazide thường được sử dụng nhất là hydrochlorothiazide và chlorthalidone. Huyết áp sẽ giảm hiệu quả và êm dịu, thuốc phổ biến hiện nay như các chất ức chế ACE và ARB thường kết hợp với thiazide.
Làm thế nào để một thuốc lợi tiểu làm giảm huyết áp?
A. muối nhạy cảm, đáp ứng tốt với các thuốc lợi tiểu.
B. điều chỉnh thể tích / nước tự do có thể là một yếu tố
C. tác dụng trực tiếp trên cơ trơn mạch máu. Kênh vận chuyển natri sẽ bị khóa và do đó ngăn trao đổi canxi.sẽ gây cạn kiệt lượng canxi trong tế bào cơ trơn mạch máu .làm giảm tương tác actin myosin và do đó giãn mạch
D. Thiazide kết hợp tốt với tất cả các thuốc chống tăng huyết áp khác (ức chế men chuyển, ARB, Beta blockers, thuốc chẹn canxi)
E. thuốc lợi tiểu quai như furesemide không bao giờ có thể là một thuốc hạ huyết áp tốt.
24. Tại sao một số bệnh nhân suy tim không bao giờ gây phù ?
Phù được coi là biểu hiện chính của suy tim trong nhiều thập kỷ. Nó là một trong những tiêu chí nhỏ của giao thức Framingham để chẩn đoán suy tim.
Các cơ chế phù nề trong suy tim là đa yếu tố. Các cơ chế chính là do tăng áp lực tĩnh mạch. Điều này tác động ngược trở lại vào máu và kết quả làm gia tăng áp lực thủy tĩnh đoạn cuối tĩnh mạch của mao mạch dẫn đến phù nề.
Mặc dù đây được xem là cơ chế thống trị trong nhiều thập kỷ trước, nhưng nó có thể không đúng. giảm rõ rệt cung lượng tim và giảm kết quả lưu lượng máu thận gây nên phản ứng thiếu máu thận và kích hoạt Rass (hệ thống renin aldosterone angiotensin). Đây là sự kích thích mạnh mẽ cho việc giữ natri và nước. Điều này là cơ chế chủ yếu của chứng phù tim. Đây là giải thích ngắn gọn các cơ chế phù nề trong suy tim và 1 số trường hợp không có phù.
24. Có sự kích hoạt thần kinh nội tiết ở 1 số bệnh nhân suy tim?
Kích hoạt RAAs sẽ thúc đẩy hoạt hoá hormon lợi niệu nhĩ (atrial natriuretic peptide) làm giảm tái hấp thu nước ở ống lượng xa ngăn tiến triển phù ở 1 số người. Vì vậy, có một nhóm riêng biệt bệnh nhân suy tim hiếm khi tiến triển gây phù nề.
các loại suy tim gây phù phổ biến?
suy tim phải bệnh tim –phổi bệnh van ba lá
viêm màng ngoài tim co thắt
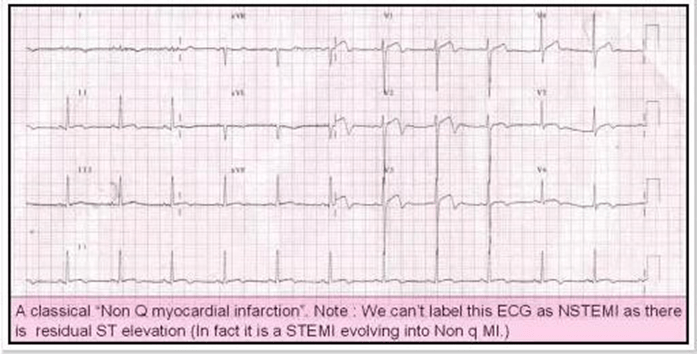
25. thuật ngữ “Non q MI” lỗi thời hay vẫn còn có liên quan?
Hội chứng mạch vành cấp (ACS) hiện đang được phân loại là STEMI và NSTEMI. phân loại ra chủ yếu để xét xem có đủ điều kiện dùng thuốc làm tan huyết khối, như ST chênh lên là tiêu chí duy nhất để dùng thuốc làm tan huyết khối.trước đó thuật ngữ không có sóng Q trong MI phần lớn được sử dụng để biểu thị ngày xuất hiện NSTEMI. Có sóng Q trong MI để chỉ có tổn thương xuyên thành, không có sóng Q thì không xuyên thành (Tất nhiên, bây giờ chúng ta biết mối quan hệ giữa sóng q và thành cơ tim là không tốt) Vì vậy, chúng ta vẫn có thể sử dụng thuật ngữ không có sóng q trong MI?
Những thuật ngữ STEMI và NSTEMI dùng khi nhập viện tại các phòng cấp cứu. ACS là đơn vị năng động, những bệnh nhân này có thể có thay đổi nhanh chóng đoạn ST, từ chênh xuống đến chênh lên và ngược lại. thay đổi sóng T cũng có thể xảy ra. Sóng Q có thể hoặc không thể tiến triển triển, phụ thuộc vào tổn thương lâu dài đến cơ tim và hiệu quả của thuốc tan huyết khối / PCI. Vì vậy, cần phải nhấn mạnh ở đây STEMI, NSTEMI, q MI, non q MI là sự miêu tả của cùng một nhóm các bệnh nhân trong khung thời gian khác nhau. Nói lên sự tiến triển STEMI là q MI và NSTEMI là non q MI. nhưng có thể đổi ngược lại cho nhau
Vấn đề ở đây là NSTEMI chuyển đổi thành STEMI thì không có vấn đề gì về danh pháp. Nhưng khi STEMI giảm bớt chuyển về NSTEMI có rõ ràng không có danh pháp tương thích, điều này làm cho bệnh nhân không có lựa chọn nào khác hơn là ” STEMI tiến hóa thành non q MI‖ . Bởi vì người ta không thể chẩn đoán STEMI tiến triển NSTEMI
Điểm quan trọng cần nhớ ở đây là NSTEMI được chuyển đổi thành STEMI là biến chứng bất lợi và trong thực tế, bệnh nhân sẽ phải dùng tan huyết khối ngay lập tức hoặc PCI, trong khi một STEMI chuyển đổi thành non Q MI thường là một thành công lớn trong điều trị . (Trục vớt hiệu quả và ngăn chặn sóng q)
Đặc trưng trên điện tâm đồ NSTEMI là gì?
Nhồi máu cơ tim không ST chênh (NSTEMI) là 1 biểu hiện chính của hội chứng mạch vành cấp. Biểu hiện có cơn đau thắt ngực không ổn định trên lâm sàng và men tim hoặc troponin tăng cao.
ECG có thể có những biểu hiện sau 1.ST chênh xuống(70-80%)
2.đảo ngược sóng T (10-20%)
3. ST chênh xuống và sóng T đảo ngược
4. sau NSTEMI -ECG thay đổi (nhưng trớ trêu ở chỗ, có thể vân còn ST chênh lên) 5.ECG bình thường
Đa phần NSTEMI có ST chênh xuống. NSTEMI thuần túy với sóng T đảo ngược ít gặp nhưng hay xảy ra trong quá trình chu phẫu, trước CAD.NSTEMI có ECG bình thường rất hiếm gặp nhưng có thể xảy ra.
Nhồi máu cơ tim cấp tính không đáp ứng với thuốc tiêu huyết khối xảy ra ở 30-40% bệnh nhân. Cách tiếp cận bệnh nhân dùng tiêu huyết khối thất bại thường đặt stent và kết quả
Không rõ ràng. Cách lặp lại dùng thuốc tiêu huyết khối chưa được nghiên cứu rộng rãi và không phổ biến giữa các bác sĩ tim mạch.
Chúng tôi trình bày kinh nghiệm của chúng tôi với sáu bệnh nhân (Tuổi 42-56, M-6, F-0) thất bại khi dùng liều thuôc tiêu huyết khối đầu tiên. Bệnh nhân có MI và đã dùng một trong hai loại urokinse hoặc streptokinase (giữa 4-9 giờ) sau khi khởi phát đau ngực. Tất cả trong số họ đều vẫn còn ST chênh lên, đau thắt ngực không đáp ứng với liều tối đa IV NTG và thuốc chẹn beta. Liều ban đầu thuốc tiêu huyết khối coi như đã thất bại. Lặp lại với streptokinase (15 lkahs = 1.500.000UI) dùng giữa giờ thứ 16 và 24. Kết quả lâm sàng sau khi dùng lần 2 thấy giảm đau thắt ngực, đoạn ST chênh xuống 50% và chụp mạch vành sau 2-4 tuần cho thấy lòng động mạch vành không có huyết khối ở 4/6 bệnh nhân. Một lời giải thích hợp lý từ các nguyên tắc cơ bản về dược lý lâm sàng gợi ý rằng nguyên nhân phổ biến thất bại của bất kỳ loại thuốc nào là do liều đầu tiên không đủ.
Kết luận: Chúng tôi kết luận rằng lặp lại liều thuốc tiêu huyết khối có thể hiệu quả để làm tan huyết khối trong MI
Quan điểm cá nhân
Lặp lại liều thuốc tiêu huyết khối vẫn được coi là điều trị trong tưởng tượng của hầu hết các chuyên gia tim mạch! hiệu quả của phương thức điều trị này sẽ không bao giờ được viết lên cho nhân loại cũng như kế hoạch cho một nghiên cứu như vậy, sẽ được gọi là phi đạo đức của các bác sĩ tim mạch hiện đại ngày nay.
Trong khi các bác sĩ can thiệp đều khuyên phải can thiệp, họ sẵn sàng mỉa mai phương pháp dùng thuốc tiêu sợi huyết để điều trị và khi nó thất bại . tất nhiên, tỷ lệ thất bại khi dùng thuốc làm tan huyết khối có thể lên tới 50% . hiện cũng không có nhiều sáng kiến cải tiến để nâng cao hiệu quả của các loại thuốc này.
Nếu liều đầu tiên không hiệu quả, hãy luôn suy nghĩ đến liều tăng dần nếu thấy an toàn để sử dụng. Chúng ta có thể tăng liều lượng thuốc tiêu huyết khối như nào để không làm tăng nguy cơ chảy máu đến mức nguy hiểm?
Đây là một câu hỏi thử nghiệm lâm sàng.
Ở những bệnh nhân có huyết khối chi dưới và thuyên tắc phổi cấp, chúng tôi có dữ liệu an toàn khi dùng liều 1 vạn đơn vị trong một giờ cho đến 48 giờ.
Phác đồ tương tự có thể dùng ở bệnh nhân STEMI nếu thuốc tiêu huyết khối liều đầu đã thất bại và không thể có ngay can thiệp mạch
Thật không may, chúng ta không thể đi một mình trong y học, Chúng ta cần dữ liệu khoa học (có hoặc không có lý!) .Nhưng bây giờ, cảm giác và kết quả của chúng ta cũng là một phần không thể thiếu của phương pháp điều trị này được gọi là bằng chứng cấp 3/ theo đồng thuận của AHA / ACC.
Theo kinh nghiệm của chúng tôi, truyền liên tục streptokinase 1 lakh (1000000/ giờ trong 24-48 giờ) ở bệnh nhân MI có thể là 1 lựa chọn, đặc biệt khi không thể can thiệp ngay lập tức cho bệnh nhân
26. Rung nhĩ là một rối loạn nhịp tim lành tính?
Rung thất luôn gây tử vong nếu không được điều trị. Còn rung nhĩ có thể gây tử vong?
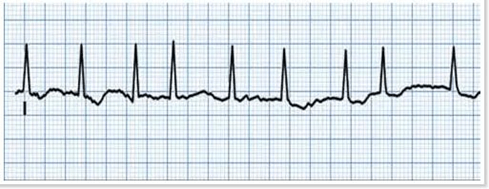
Rung nhĩ là rối loạn nhịp tương đối lành tĩnh đặc biệt khi nó xảy ra độc lập với các cấu trúc bình thường của tim. đôi khi được gọi rung nhĩ đơn độc. Rung nhĩ hiếm khi gây tử vong, ngoại trừ trong vài trường hợp. Rung nhĩ AF thường mất ổn định ở các bệnh nhân có bệnh van tim hoặc bệnh cơ tim. (sau MI, bệnh cơ tim giãn)
Có vài tình huống mà AF có thể nguy hiểm đe doạ tính mạng
Ở những bệnh nhân có hội chứng WPW, AF sẽ có thể chuyển thành cuồng nhĩ , làm tăng tần số lên 400-600. Lúc này có thể bn không chết vì rung thất đã chết do rung nhĩ.
AF trong NMCT cấp thường gây suy thất trái LVF, nhưng hiếm khi gây chết.
Ở những bệnh nhân bị hẹp động mạch chủ nặng hoặc bệnh cơ tim phì đại, khởi phát đột ngột AF có thể gây suy tim cấp tính.
AF thường là hậu quả cuối của tăng áp động mạch phổi nguyên phát. Trong khi rung nhĩ ít có khả năng gây tử vong, nhưng nó lại là rối loạn nhịp tim rất bệnh hoạn, Nó là một trong những nguyên nhân quan trọng gây đột quỵ ở người già cũng như trẻ!
CASE
Bệnh nhân nữ 76 tuổi tiền sử bệnh động mạch vành (CAD), tăng huyết áp, tăng lipid máu, cơn thiếu máu thoáng qua (TIA), và đái tháo đường (DM) kiểm soát bởi thuốc vào viện 2 ngày trước vì viêm phổi và được điều trị bằng kháng sinh. Bệnh nhân đột nhiên xuất hiện rung nhĩ (AF) với tỷ lệ thất nhanh (RVR)
Mà không có triệu chứng. phác đồ điều trị thuốc hiện tại là aspirin, atorvastatin, lisinopril, metoprolol succinate, metformin và moxifloxacin. điện tâm đồ
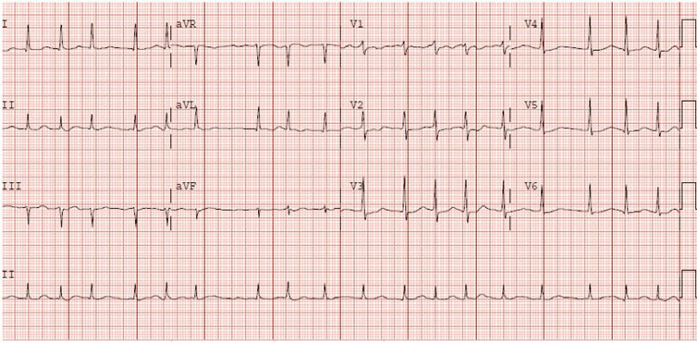
THẢO LUẬN TRƯỜNG HỢP
Trường hợp này trình bày một số vấn đề phải quyết định trên lâm sàng ở bệnh nhân RN. Những quyết định này xoay quanh 4 mục tiêu chính trong điều trị AF cấp tính:
1. Có cần sốc điện trong các trường hợp rung nhĩ cấp tính
2. Kiểm soát tỷ lệ thất trong AF
3. Chiến lược kiểm soát nhịp và tần số
4. Đánh giá nguy cơ huyết khối tắc mạch và chảy máu, lợi ích và rủi ro khi áp dụng biện pháp điều trị.
Thông thường trong các hệ thống mạch máu thì động mạch và tĩnh mạch luôn đi cùng nhau, nhưng thật kì lạ trong tuần hoàn phổi chúng lại không bao giờ đi cùng nhau .
Nghịch lý khác là động mạch phổi mang máu đã khử ôxy và tĩnh mạch phổi lại mang dạng máu tinh khiết nhất của máu trong cơ thể , có lẽ chúng được tách rời hẳn nhau ví lo sợ ảnh hưởng đến sinh lý.
27. Điều gì quyết định sự ổn định huyết động trong nhịp nhanh thất?
Nhịp nhanh thất được coi là một trong những rối loạn nhịp tim nguy hiểm nhất. Hơn nữa VT luôn có nguy cơ tiến triển thành rung thất.
Điều gì quyết định sự ổn định huyết động ở VT?
Nguồn gốc và vị trí của VT Tần số thất
Có hay không có AV phân ly
Ảnh hưởng đến dòng máu qua van hai lá
rối loạn chức năng thất trái hoặc bệnh van tim.
VT trong hội chứng mạch vành cấp. (Thiếu máu cục bộ VT) lựa chọn thuốc phù hợp
Nguồn gốc và vị trí
VTs xuất phát từ phía trên của tâm thất giúp tâm thất co có tổ chức và ổn định.Distal VT (VT khởi phát vùng dưới tâm thất) có nguồn gốc từ các cơ tim đã được dẫn truyền đang rất hỗn loạn nên VT vị trí này rất không ổn định.
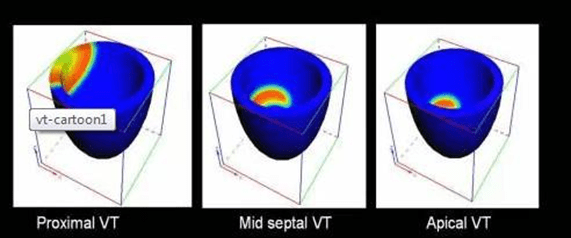
Thuật ngữ VT fascicular (VT bó)chưa nghe đến những VT có nguồn từ các bó hoặc nhánh thì có. Thường vị trí này cũng ổn định và khi đáp ứng tốt với các thuốc chẹn canxi chỉ ra rằng vị trí này rất gần ngã 3 AV mà mang đặc tính nhịp nhanh bộ nối. Độ rộng của QRS có thể giúp ước lượng sơ qua về vị trí VT. QRS hẹp thường gợi ý nguồn gốc khởi phát VT ở trên cao (Nhưng nhớ ngay cả ở VT, QRS có thể tiếp tục rộng ra khi dẫn truyền từ trên đi xuống)
Rối loạn chức năng thất trái LV.
Đây có lẽ là yếu tố quyết định quan trọng nhất trong VT. Bệnh nhân có rối loạn chức năng LV nặng (EF <30%) tiên lượng rất xấu .Biểu hiện lâm sàng thường gặp nhất là giãn cơ tim. ! số sẽ xuất hiện dẫn truyền vào lại các nhánh (BBR). Đây là dạng VT đã ổn định trong nhiều giờ.
Tần số thất.
Thông thường VT có tần số từ 120-200. Tần số thất cao hơn thường bất ổn . Điều này cũng không phải luôn đúng như trong trường hợp có fascicular VT. Vị trí VT và rối loạn chức năng LV thường ảnh hưởng đến tỉ lệ thất
Lưu lượng dòng chảy qua van hai lá đổ đầy thất trái giúp ổn định huyết động trong VT. Trong thiếu máu cục bộ cơ tim có VT, dòng máu qua van 2 lá bị ảnh hưởng nghiêm trọng . sẽ không thể đổ đầy thất trái giúp ổn định huyết động.
nếu có bệnh lí liên quan tới van tim, động mạch chủ và van hai lá có thể làm nặng thêm rối loạn huyết động ở bệnh nhân có VT.
28. Triệu chứng tim mạch: hồi hộp – một số quan sát
Đánh trống ngực là một trong những triệu chứng hay gặp nhất mà các bệnh nhân thường gọi là hồi hộp đánh trống ngực. Giống như khó thở, tim hồi hộp có thể là một
Biểu hiện sinh lý bình thường hoặc trạng thái bệnh lý nguy hiểm của tim. Điều này làm cho các bác sĩ phải khám và đánh giá cẩn thận. Theo định nghĩa đánh trống ngực là những biểu hiện bất thường ở tim mà bệnh nhân nhận thấy được. Các nguyên nhân do thần kinh gây đánh trống ngực chưa rõ ràng. Khi tim chạm vào thành ngực có thể theo các dây thần kinh ở thành ngực dẫn truyền tín hiệu.
Nguyên nhân đánh trống ngực là gì? Do tim
Tăng tuần hoàn ở thất phải, trái hoặc cả hai.
tổn thương trào ngược ở van 2 lá hoặc van động mạch chủ
Bệnh tim bẩm sinh (Chủ yếu là shunt trái sang phải ASD / VSD..) bệnh nhân thay van tim giả, đặt máy tạo nhịp tim
Loạn nhịp tim (Cả nhanh và chậm), nhịp thất lạc chỗ Sa van hai lá, thường lành tính
Không do tim
Sinh lý
Trạng thái lo lắng Thiếu máu
Mối quan hệ giữa phân số tống máu và đánh trống ngực là gì?
Nói chung đánh trống ngực chỉ trạng thái tăng hoạt động của tim . Nguyên nhân phổ biến nhất là do hồi hộp, lo lắng . Ngoài ra cũng do nguyên nhân thiếu máu, sốt, nhiễm độc giáp, mang thai … Trong tất cả các tình huống, đánh trống ngực là dấu hiệu của tăng sức co tâm thất tạo ra dp / dt (Tỷ lệ gia tăng áp lực tâm thất). Vì vậy, khi có biểu hiện hồi hộp, đánh trống ngực có thể là bằng chứng gián tiếp chứng tỏ chức năng LV còn khá tốt. “Bệnh nhân có giãn cơ tim hoặc CHF hiếm khi thấy đánh trống ngực khi gắng sức mà thường thấy khó thở do LV co yếu”
Đánh trống ngực có thể do loạn nhịp, nhịp nhanh hoặc chậm.
“ASD là nguyên nhân phổ biến nhất gây hồi hộp bên thất phải”
29. Làm thế nào ngồi xổm lại giúp giảm khó thở khi gắng sức ở bệnh nhân tứ chứng Fallot?

Thực tế ngồi xổm cũng được biết đến là một tư thế bù thích nghi đơn ở trẻ em bị bệnh tim có tím tái khi phải gắng sức để dễ thở hơn. Trẻ bị tứ chứng Fallot thường thiếu oxy do shunt phải sang trái . Khó thở khi phải gắng sức. Nếu ngồi sẽ cải thiện bão hòa oxy ngay lập tức.
Huyết động học của ngồi xổm có hai giai đoạn
Ngay lập tức (trong 15 giây đầu) sau khi ngồi xổm có giảm đột ngột phản hồi dòng máu tĩnh mạch.
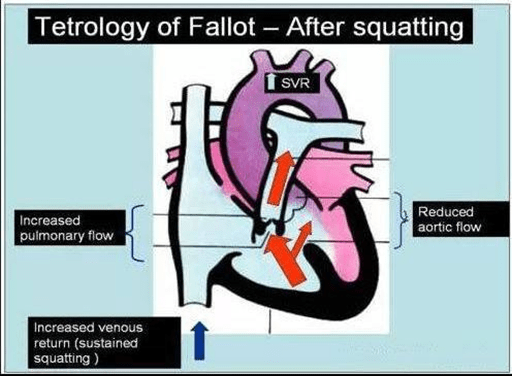
ngồi xổm tiếp 1-2 phút sẽ gia tăng ổn định quá trình hồi lưu máu về tĩnh mạch, tăng kháng trở mạch máu.
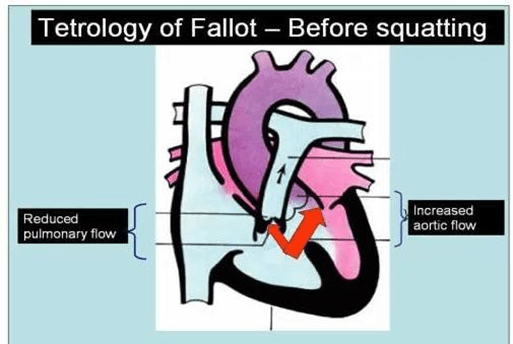
Khi khó thở do gắng sức mà ngồi xổm sẽ tăng kháng trở mạch máu và động mạch chủ sau khi đủ tải sẽ chuyển hướng dòng máu vào động mạch phổi. Ngồi xổm giúp tăng thoáng qua hoặc duy trì lưu lượng máu lên phổi giúp giảm tương đối shunt trái
30. Đau thắt ngực ổn định có thể xảy ra khi nghỉ ngơi?
Đau thắt ngực, theo cổ điển thường xảy ra khi gắng sức và đỡ đau khi nghỉ ngơi .Đây được gọi là cơn đau thắt ngực ổn định mạn tính điển hình như mô tả của Heberden (CSA). Thuật ngữ cơn đau thắt ngực không ổn định (UA) được mô tả đầu tiên bởi Noble O Fowler vào đầu năm 1970. (Cũng được gọi là hội chứng mạch vành trung gian, đau thắt ngực tiền nhồi máu..) và được sử dụng nhiều trong những năm gần đây.
1. Tất cả các trường hợp đau ngực khi gắng sức ở bất kỳ mức độ nào để có thể là biểu hiện đầu tiên của cơn đau thắt ngực ổn định.
2. Đau khi nghỉ ngơi > 30 phút không đỡ dù dùng nitroglycerine ngậm dưới lưỡi. 3.Đau ngực sau MI
4.Đau ngực ở những bệnh nhân đã đặt stent qua PCI.
Làm thế nào để nhận biết một bệnh nhân từ đau ngực ổn định sang không ổn định UA? Nghi ngờ UA khi
5.Đau thường xuyên hơn bình thường
6.Đau ngực có khi mức độ đau nhẹ hơn bình thường
7.Đau ngực lan tới vị trí mới (đau lan ra hàm chứ không phải cánh tay trái như bình thường hoặc ngược lại )
Đau thắt ngực là biểu hiện lâm sàng của thiếu máu cục bộ. Cơn đau ngực đầu tiên không thể coi thường, có thể là khởi đầu của bệnh mạn tính hoặc là tắc mạch vành tiến triển trong đau ngực không ổn định / NSTMEI, hay thậm chí là STEMI.
Ngược lại một bệnh nhân đau thắt ngực ổn định mạn tính có đau ngực có thể dự đoán, đau khi gắng sức, đau cùng một chỗ, cùng một kiểu và bệnh nhân biết chắc chắn sẽ hết đau khi dùng nitroglycerine.
Các bệnh lý tiềm ẩn trong UA là gì?
Nói chung hiếm khi mảng xơ vữa ổn định lại gây cơn đau thắt ngực không ổn định. mảng bám không ổn định nghĩa là mảng bám bị xói mòn, nứt, vỡ hoặc tạo huyết khối động.
Các cơn đau thắt ngực khi nghỉ ngơi lại được gọi là cơn đau thắt ngực không ổn định?
Không, bác sĩ tim mạch tin rằng là do cơn đau thắt ngực không ổn định.
các tình huống mà đau thắt ngực ổn định CSA có thể xảy ra lúc nghỉ ngơi?
đau thắt ngực khi stress, sau bữa ăn rất hay gặp ở bệnh nhân CSA, đỡ khi giảm căng thẳng. Một số bệnh nhân CSA trong cơn sốt có thể đau thắt ngực lúc nghỉ ngơi .Đây được coi là biến thể của đau thắt ngực ổn định.
đau thắt ngực sau bữa ăn, có thể xem xét là yếu tố không ổn định
31. Làm thế nào mà thường có sự nhầm lẫn chẩn đoán xảy ra giữa CSA và UA? Nói chung, vấn đề này ít được đề cập đến trong giáo trình tim mạch, với lý do đơn giản, không có phân biệt rõ ràng giữa 2 cái này!
Theo Hội tim mạch Canada chia 4 mức độ CSA gần tương tự như UA, vì nó biểu thị đau thắt ngực xảy ra khi gắng sức tối thiểu hoặc thậm chí lúc nghỉ ngơi. Trong thực tế lớp CCSC 4 nên coi như UA.
ECG có giúp xác định đau thắt ngực ổn định từ đau thắt ngực không ổn định?
ECG thỉnh thoảng sẽ cứu chúng tôi khi có sự lầm lẫn giữa UA và CSA mặc dù nghỉ ngơi ST chênh xuống vẫn có thể xảy ra ở cả đau thắt ngực ổn định và không ổn định. Theo thống kê, nếu ST chênh xuống hiện trong cơn đau ngực thì nhiều khả năng nó là UA hơn CSA . Ngoài ECG, Troponin T hoặc I có thể tăng trong một số bệnh nhân bị đau thắt ngực không ổn định. Hiếm khi đau thắt ngực ổn định có tăng troponin.
Ở những bệnh nhân tăng huyết áp hệ thống và LVH hoặc bệnh cơ tim, đau ngực khi nghỉ ngơi có ST chênh xuống có thể không phải là UA
Vì vậy, sự khác biệt giữa UA và CSA đòi hỏi đánh giá cẩn thận tiền sử, khám lâm sàng (hẹp động mạch chủ / HCM có thể gây đau thắt ngực ổn định) và ECG, đánh giá enzyme. CUỐI CÙNG
Với bất kì bệnh nhân nào vào cấp cứu với chẩn đoán ban đầu ACS / UA / NSTEMI, sau đó thường chẩn đoán là UA. Lỗi này xảy ra vì đau ngực hoặc ECG có sự thay đổi do các yếu tố không do tim như stress , sau hậu phẫu hoặc sốt.
Trong bối cảnh này, cần có một định nghĩa mới cho đau thắt ngực không ổn định.
Trong cơn đau thắt ngực, ở bất kỳ mức độ nào mà do vấn đề cấp máu (huyết khối cấp tính / mảng bám gây tắc động mạch vành có nguy cơ xảy ra nhồi máu cơ tim) gọi là UA.
Tất cả đau ngực sau MI và PCI gọi là UA
đau thắt ngực khi nghỉ ngơi xảy ra do tình trạng tăng nhu cầu có thể coi là ACS với lí do đơn giản không phải huyết khối hay mảng bám có khả năng gây ra đau ngực ở bệnh nhân này. Hiếm khi tiến triển thành MI. cơ chế gây đau thắt ngực lúc nghỉ ngơi thường do nhịp tim nhanh và kết quả tăng MVO2 (Tiêu thụ oxy của cơ tim) .Hiện nay chúng được gọi là đau thắt ngực không ổn định thứ phát.trong thực tế thuốc chống huyết khối được lạm dụng trong những tình huống này do đáp ứng các tiêu chí của UA / NSTEMI.
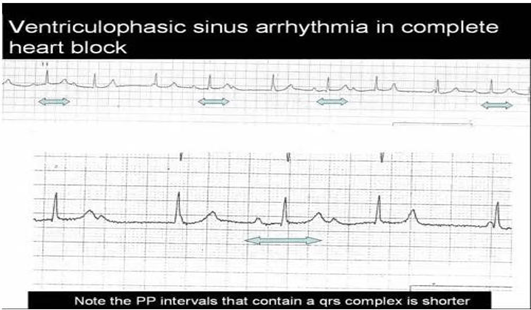
32. Loạn nhịp xoang thì thất trong block AV hoàn toàn
là rối loạn nhịp xoang không liên quan hô hấp gặp trong block AV hoàn toàn. Khoảng PP kèm theo phức hợp QRS ngắn hơn so với khoảng thời gian PP không kèm theo QRS.
Cơ chế
Là do tăng lưu lượng máu vào động mạch nút SA trong thì tâm thu thất kích thích tạo nhịp tim sớm và do vậy làm giảm độ dài chu kỳ xoang.
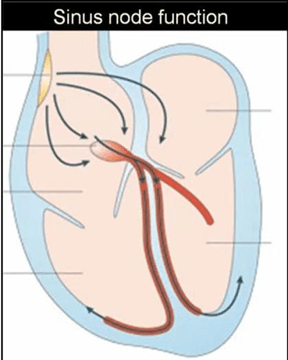
Cơ chế nhịp ngừng xoang?
Nút xoang như máy tạo nhịp tim, nó tạo nhịp tim đều đặn trong suốt cuộc đời. Nhưng nó có thể tạm dừng một chút, tất nhiên tạm dừng dưới 15% chiều dài nhịp xoang cơ bản. Sự thay đổi độ dài chu kỳ xoang được gọi loạn nhịp.nhịp xoang là sinh lý. Khi nó vượt quá 15% của chu kỳ xoang trước đó nó được gọi là ngừng xoang
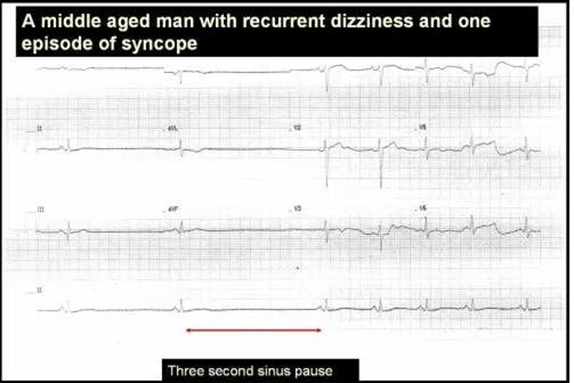
Điều gì xảy ra sau ngừng xoang?
Sau ngừng xoang thường có nhịp trì hoãn, nhiều khi theo sau với nhịp thoát bộ nối.
Cơ chế điện sinh lý của ngừng xoang là gì?
Đơn giản là do nhịp tim chậm. Thường gặp nhất là tăng phản xạ phế vị. thường gặp ở các vận động viên trẻ. Cho dù tăng phản xạ phế vị có ý nghĩa vô thưởng vô phạt, nhưng cũng có thể phải cần can thiệp.
Chặn đường ra dẫn truyền từ nút xoang (Sinus node exit block) block SA Độ 1, độ 2 xảy ra hoàn toàn như trong nút nhĩ thất.
block SA độ 1 không thể chẩn đoán bằng ECG bề mặt. block SA độ 3 giống như ngừng xoang và phải dùng máy tạo nhịp tim ở những bệnh nhân này. block SA độ 2 thường được chẩn đoán khi ngừng xoang là bội số của chu kỳ xoang. Tất cả những rối loạn nhịp tim này được gọi chung là rối loạn chức năng nút xoang (SND)
Làm thế nào để xử trí những bệnh nhân này?
rối loạn nút xoang có thể xảy ra trong 1số các bệnh hệ thống -> cần phải được loại trừ.
– Thâm nhiễm các bệnh như amyloidosis, suy giáp có thể dẫn đến SND. Thuốc gây SND như beta blocker và chẹn kênh canxi chẹn là nguyên nhân hay gặp và cần được loại trừ
Một số bệnh tim bẩm sinh (SVC ASD) có thể liên quan đến nút xoang.
Bệnh nút xoang thiếu máu cục bộ hiếm gặp nhưng có thể xảy ra sau nhồi máu cơ tim thành sau dưới
Rối loạn nút xoang thường liên quan đến thoái hoá tâm nhĩ, bệnh cơ tim …
Khi ngừng xoang cần chú ý huyết động của bệnh nhân. Thanh niên thường có thể chịu được 2 , 3 nhịp nhừng xoang nhưng thường có thể ngừng tới3s . Ngừng xoang bệnh lý có thể lên đến 5 giây (ngừng 5s nhịp tim tương ứng 12 nhịp/ phút sẽ gây ngất). ngừng 3 giây tương ứng với 20 nhịp / phút.
Làm thế đánh giá một bệnh nhân bị ngừng xoang?
Có nhiều nghiên cứu điện sinh lý phức tạp (EP) có sẵn như ECG nút xoang, nghiên cứu chức năng nút xoang như thời gian phục hồi nút xoang, thời gian kích hoạt…
33. Sự chồng chéo giữa các rối loạn chức năng nút xoang và ngất do thần kinh tim là gì? SND có thể xảy ra như một hội chứng chồng chéo với ngất do thần kinh tim neurocardiogenic. (NCS) .NCS cũng là một nguyên nhân hay gây ngất . NCS có hai
Nhánh, 1 nhánh ức chế tim, 1 nhánh giảm mạch .khi khó xác định có thể làm nghiệm pháp bàn nghiêng kiểm tra.
Điều trị
Ngừng tất cả các loại thuốc có thể gây nhịp tim chậm là điều hết sức quan trọng. Đặt máy tạo nhịp ở các bệnh nhân có triệu chứng
*Uống Aminophylline sẽ đối kháng thụ thể adnosine ở nút xoang. 1 số thuốc khác có thể tăng nhịp tim trong thời gian ngắn như Orcipranaline (kích thích Beta 2 / Alupent) Probantheline (chặn M 1)
Vấn đề chính là để tránh cấy máy tạo nhịp tim không cần thiết ở những bệnh nhân có ngừng xoang không đáng kể.
34. Khái niệm bị lãng quên và thuốc tim mạch: lignocaine (lidocaine) dùng cho nhịp nhanh trên thất và rung thất
Lignocaine, có lẽ là loại thuốc đã được nghiên cứu nhiều hơn bất kỳ loại thuốc tim mạch khác trên toàn thế giới.
Nó là thuốc được lựa chọn duy nhất cho nhịp nhanh thất cho đến năm 1990, cả trước và sau khi dùng thuốc tiêu huyết khối ở các đơn vị chăm sóc mạch vành. Điều này đã giúp cứu sống hàng chục ngàn bệnh nhân nhịp nhanh trên thất không ổn định về nhịp xoang bình thường. Dùng lignocaine tĩnh mạch vừa đơn giản, vừa hiệu quả lại có tác dụng với hầu như tất cả các dạng VT. Trước đây được bolus 2 hoặc nhiều lần sau đó truyền duy trì. Những gì đã xảy ra với loại thuốc tuyệt vời này?
Sức mạnh của thống kê và giải thích không phù hợp bởi cộng đồng khoa học làm mọi người xa lánh và không còn sử dụng loại thuốc này cho VT dù tác dụng thần kỳ của nó ai cũng hiểu.
Tại sao lignocaine thất thế trong trận chiến? có 3 lí do 1.Sự ra đời của nhiều người thích sử dụng Amiodarone
2.Một nghiên cứu tiêu cực về sử dụng các thuốc chống loạn nhịp sau MI (CAST) 3.Và hai cái gọi là nghiên cứu tích cực cho Amiodarone (ALIVE & ARREST) đã lên tiếng chuông khai tử cho loại thuốc kỳ diệu đã cứu hàng triệu con người này nghiên cứu CAST http://content.nejm.org/cgi/content/abstract/321/6/406
Nghiên cứu CAST không nên dùng thuốc chống loạn nhịp ở bệnh nhân loạn nhịp thất không triệu chứng sau MI. Nhưng bạn có biết, làm sao có thể giải thích “lignocaine không có vai trò trong loạn nhịp thất sau MI ” vì điều buồn cười nhất là lignocine chưa bao giờ được sử dụng trong nghiên cứu CAST.
Đọc thêm 2 nghiên cứu dưới đây và kết luận tuỳ suy nghĩ của bạn http://content.nejm.org/cgi/content/abstract/346/12/884 http://content.nejm.org/cgi/content/full/341/12/871?ijkey=8fa241f3cebb86a177632ec6cc adfb5a3ded7bc2
CUỐI CÙNG
– Lignocaine không chỉ là thuốc gây tê tại chỗ, nó là thuốc gây mê cơ tim mạnh mẽ và nhẹ nhàng khi dùng cho bệnh nhân sau giai đoạn MI.
-Nó khử rung thành công và ngăn loạn nhịp thất tiến triển nặng lên
-Thời gian thử nghiệm và điều trị hiệu quả đã được chứng minh.
-Thật kinh tởm và dối trá khi có những bác sĩ tim mạch nói amiodarone xử trí thành công VT hơn lignocaine.
-Bất kỳ chuyên gia tim mạch giàu kinh nghiệm nào cũng sẽ nhận ra, nhiều lần thậm chí VT kháng Amiodarone thường đáp ứng với lignocaine.
-Mấu chốt của vấn đề là không có nghiên cứu nào có chất lượng về lignocaine vì vậy nó bị bỏ rơi. Vì nó là thuốc thông thường và không có giá trị kinh tế
Với tôi, Lignocaine vẫn có một vai trò rất lớn để xử trí các rối loạn nhịp thất nguy hiểm
.nhưng không nên sử dụng thường xuyên và bừa bãi ở bệnh nhân không triệu chứng và VT không liên tục (Theo kết luận của CAST).
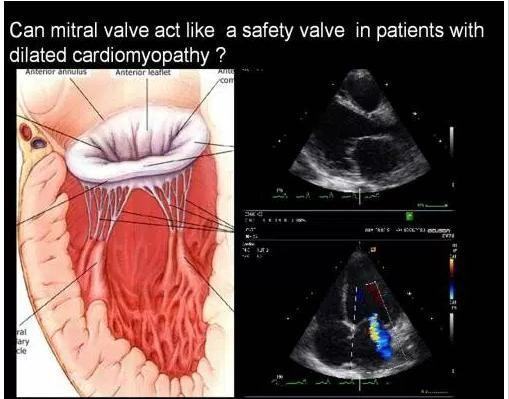
35. Van hai lá có tác dụng như một van an toàn ở những bệnh nhân có bệnh giãn cơ tim DCM?
van hai lá rất quan trọng trong điều hòa huyết động của tim. Hiện tượng trào ngược van hai lá gặp ở 10-20% dân số bàng siêu âm doppler tim. Khi làm lâm sàng thường các bác sĩ siêu âm có kinh nghiệm sẽ không nói với bệnh nhân điều này vì nó có thể làm tăng sự lo lắng của bệnh nhân.
van hai lá trào ngược mức độ nhẹ có thể là một lợi thế về huyết động học?
tâm thất trái, về sinh lý chỉ có một đường tống máu ra ( LVOT) là van động mạch chủ. Khi suy tim tăng lên thì áp lực lên LV càng lớn. Cơ tim thất trái càng giãn thì áp lực để bơm máu vào động mạch chủ lên thành và vách tim càng tăng (theo định luật Laplace) dẫn tới tăng hậu tải. Quan niệm về suy tim gây thúc đẩy tăng lực co cơ thất trái về cơ bản là 1 quan điểm sai lầm (Ngoại trừ trong suy tim cấp tính). Do đó lựa chọn chính điều trị hiện nay là giảm hậu tải, ACEi là thuốc điều trị hiệu quả nhất và đã được chứng minh để cải thiện sự sống còn.
Tác động của van 2 lá tới hậu tải LV?
về huyết động học, van 2 lá giúp tăng co bóp LV và giảm tương đối áp lực tâm thất trái (Dp / Dt) ở hậu tải. Ở những bệnh nhân bị suy tim, cải thiện nhẹ lực co LV có thể dẫn đến cải thiện triệu chứng. Kinh nghiệm cho thấy bệnh nhân có giãn cơ tim kèm trào ngược van 2 lá nhẹ giúp bệnh nhân ổn định hơn van 2 lá bình thường hoặc xơ cứng..
Các vấn đề liên quan
* trào ngược van hai lá được cho là xảy ra khi bệnh nhân bị suy tim và giãn vòng van hai lá (mitral annular ring). Trong khi trào ngược van hai lá nhẹ có tác động tốt vậy nhưng khi nó xảy ra cấp tính (thậm chí kể cả trào ngược nhẹ), nó có thể gây nguy hiểm và dẫn đến phù phổi đột ngột . thường gặp trong NMCT cấp hoặc viêm nội tâm mạc nhiễm khuẩn…
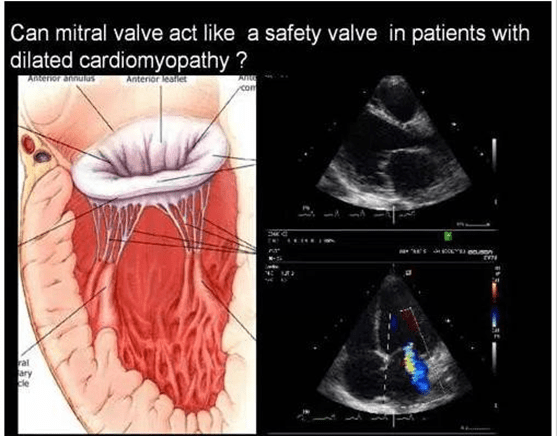
Trào ngược mức độ nhẹ ở van hai lá trên 1 số bệnh nhân có bệnh cơ tim giãn có thể mang lại một lợi thế tuyệt vời về huyết động học.
Vì vậy, không nên lo lắng khi trào ngược van 2 lá nhẹ ở những bệnh nhân có giãn cơ tim DCM.nó là lối thoát hiểm an toàn khi quá tải thất trái
36. Nhịp nhanh thất thượng tâm mạc là gì?
nhịp nhanh thất là một nhóm các rối loạn nhịp tim. Hầu hết điều trị bằng thuốc, ít khi phải dùng máy khử rung trừ khi có rối loạn chức năng LV nặng.
quan điểm trước đây VT phát sinh từ phía màng trong của cơ tim. Bây giờ chúng tôi nhận ra nhiều khi VT bắt nguồn từ thượng tâm mạc của tâm thất. Nhịp nhanh thất thượng tâm mạc (VT) được định nghĩa là VT mà vị trí vòng vào lại hoặc nguồn gốc từ mô dưới thượng tâm mạc kết thúc trong vòng 10s http://www.springerlink.com/content/w608142674154tp5/
Làm thế nào để nhận ra VT có nguồn gốc thượng tâm mạc bằng điện tâm đồ bề mặt? Sóng S kết thúc ở V2 và q sâu ở chuyển đạo 1 gợi ý VT có nguồn gốc dưới thượng tâm mạc sóng delta giả
RS > 120msec
Đề nghị nguồn gốc thượng tâm mạc của VTs. link
http://www.circ.ahajournals.org/cgi/content/full/113/13/1659
tiêu chuẩn Berruezo, http: //circ.ahajournals.org/cgi/content/full/109/15/1842 (Phải đọc) http://cogprints.org/4222/2/tada.pdf
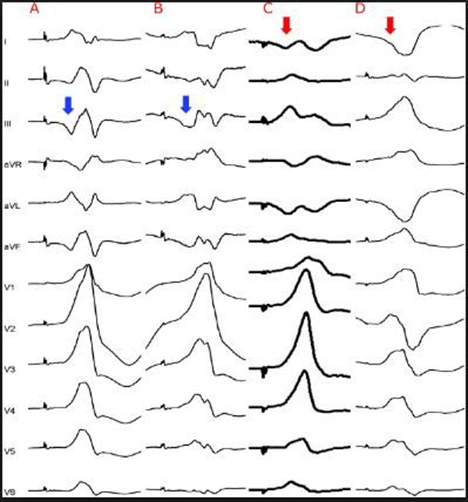
ý nghĩa lâm sàng của VT thượng tâm mạc là gì?
Cắt bỏ màng trong tim không hết VT
Có thể chọn cách tiếp cận qua màng ngoài tim
37. Tăng huyết áp tâm trương
Tăng huyết áp là yếu tố quyết định quan trọng tới sức khỏe tim mạch của dân số toàn cầu Hàng triệu bị, hàng trăm hiệp hội, nhiều khuyến cáo và các loại thuốc vẫn đang phải vật lộn để kiểm soát các mối đe dọa từ THA. 1 phần của THA là tăng huyết áp tâm trương đơn thuần IDH) đã bị lãng quên và không bao giờ nhận được sự quan tâm khoa học, mà nó xứng đáng!
Trong nghiên cứu của chúng tôi nó đã xảy ra trong 7,2% bệnh nhân THA.
JNC, chưa bao giờ coi IDH như một thực thể riêng biệt, và đến bây giờ vẫn không có hướng dẫn cụ thể. Và thật trớ trêu khi không có 1 nghiên cứu lớn nào phân tích tác động khác nhau của các loại thuốc chống tăng huyết áp trên huyết áp tâm thu và tâm trương Tăng huyết áp tâm trương độc lập
tăng huyết áp là một yếu tố quyết định chính lên bệnh lí tim mạch. Trong khi tăng huyết áp tâm thu độc lập (ISH) đã được xác định là một thực thể lâm sàng cụ thể, thì tăng huyết áp tâm trương độc lập (IDH) đã không được báo cáo như là một nhóm riêng biệt. Khi chúng tôi phân tích dữ liệu thấy một nhóm riêng biệt của bệnh nhân có tăng huyết áp tâm trương mà huyết áp tâm thu bình thường. IDH đã được định nghĩa là tâm trương hơn 90mmHg và huyết áp tâm thu dưới 140 mmHg.
IDH có mặt ở 32 (7,2%) bệnh nhân. Tỷ lệ nam nữ là 3: 1, độ tuổi trung bình là 42 (Range 32-56) huyết áp tâm trương trung bình là 96 mm (Range 90-110) . huyết áp tâm thu là 136mm (Range 128-140). LVH 4 bệnh nhân (12,5%). rối loạn chức năng tâm trương được phát hiện bằng siêu âm tim ở 20 bệnh nhân(62%)
Chúng tôi kết luận rằng tăng huyết áp tâm trương cô lập tạo thành một tập hợp con đáng kể ở những bệnh nhân tăng huyết áp và họ cần nghiên cứu sâu hơn về cơ chế bệnh sinh, biểu hiện lâm sàng và điều trị
38. kiểm soát tỷ lệ thất trong nhịp nhanh thất
Nhịp nhanh thất được coi là một bất thường nhịp tim nguy hiểm, có thể ngay lập tức tiến triển thành rung thất và dẫn đến ngừng tim đột ngột SCD. Có 1 số bệnh nhân VT có thể âm thầm không có bất kỳ triệu chứng . 1 số VT phát triển chậm và tái phát mà không ảnh hưởng nhiều đến huyết động
KIỂM SOÁT TẦN SỐ THẤT TRÊN VT
Xử trí huyết động trong nhịp nhanh thất tái phát ổn định vẫn còn là một vấn đề lâm sàng tinh tế. Quay trở lại nhịp xoang được coi là mục tiêu duy nhất của điều trị kiểm soát tần số VT. Trong khi kiểm soát nhịp được chấp nhận trong điều trị rung nhĩ, thì với VT không phải như vậy. chúng tôi đã cố gắng phân tích ảnh hưởng của Amiodarone trên tần số thất trong nhịp nhanh thất ổn định mà không phải chuyển đổi nhịp xoang.
nhóm nghiên cứu gồm 49 bệnh nhân VT ổn định, lúc vào huyết áp tâm thu> 100mmHg và không có giảm tưới máu các cơ quan đích, tuổi trung bình 52 (từ 26-68) , tỷ lệ nam nữ là 4: 1. 36 bệnh nhân không đáp ứng với IV lignocaine, Amiodarone (150-300mg bolus) hoặc sốc điện. 13 bệnh nhân không đáp ứng với một trong những xử trí trên được tiếp tục dùng Amiodarone truyền (1000mg) trong 24 giờ.
trước dùng Amiodarone tần số thất là 152 (124 -196). Sau dùng amiadaorne (trong 24 giờ) tần số thất là 128 (88-142). Thời gian để làm giảm nhịp tim xuống 50% là 6.6h (4-
24h). Huyết áp tâm thu trung bình tăng từ 100 đến 112mmhg. Bệnh nhân đã được xuất viện trong tình trạng lâm sàng ổn định dùng Amiodarone đường uống.
Có thể kết luận rằng Amiodarone, ngoài khả năng khử rung còn có tác dụng kiểm soát tần số thất ở bệnh nhân VT tái phát mạn tính.
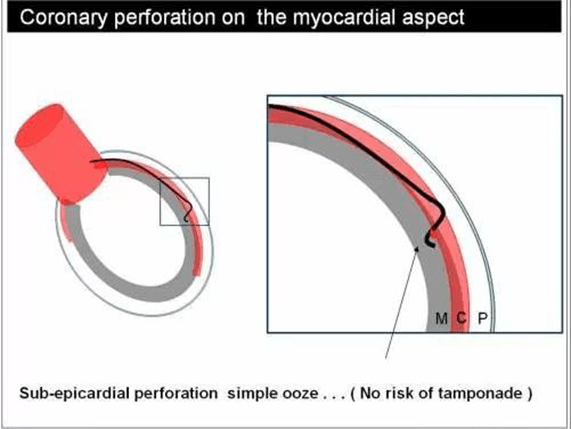
Tại sao thủng động mạch vành trong PCI lại lành tính?
thủng động mạch vành là một biến chứng đáng sợ của PCI.
Tuy nhiên, thực tế thấy rằng nhiều lỗ thủng ở mạch vành không đe dọa tính mạng?
Khi guidewire gây tổn thương và thủng mạch vành, sẽ làm thuốc cản quang ngấm ra
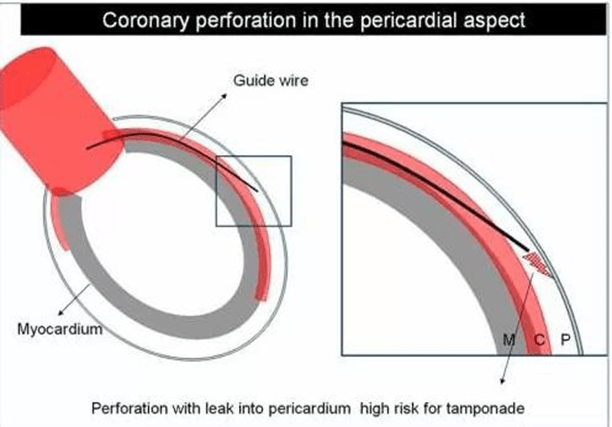
50% chu vi của động mạch vành được ôm bởi cơ tim và 50% hoặc hơn có liên quan trực tiếp đến màng ngoài tim.

Khi guide wire chạm vào cơ tim sẽ gặp lực cản lớn hơn khi chọc ra màng ngoài tim . Vì vậy, nói chung nguy cơ chọc ra màng ngoài tim cao hơn chọc vào cơ tim
Ngay cả khi, động mạch vành bị đâm thủng chọc vào cơ tim, thường không nguy hiểm do chảy máu bởi bản chất đàn hồi của cơ tim có hiệu quả phong bế rò rỉ rất tốt.

Trong khi, chọc vào khoang màng ngoài tim, thường có nguy cơ chảy máu gây chèn ép tim. Thực tế là khoang màng ngoài tim có áp lực âm và áp lực động mạch vành bình khoảng 40mmhg, do đó sẽ hút máu vào và tự liền.
40. Làm thế nào để xác định nguồn gốc nhịp nhanh nhĩ với sóng P đơn hình trong ECG? cách đơn giản và chính xác để dự đoán về nguồn gốc của nhịp nhanh nhĩ phải (RAT) nhịp nhanh nhĩ trái (LAT) là gì?
Nhìn vào những sóng P trong V 1 (Đừng nhìn cái khác!)
Sóng p âm hoặc hai pha (+/-) ở V 1 là 100% nhịp nhanh nhĩ phải
Sóng P dương ở V1 hoặc 2 pha (- / +) ở V1 có độ nhạy 100% là nhịp nhanh nhĩ trái
tỷ lệ nhịp nhanh nhĩ ở trái và phải?
Phải 75%
Trái 25%
Nguyên nhân nhịp nhanh nhĩ phải là gì?
Mào tận tâm nhĩ phải (60%)
Vòng quanh van ba lá lỗ xoang vành
bệnh mô quanh nút xoang Bệnh phần phụ nhĩ phải
Nguyên nhân nhịp nhanh nhĩ trái ? Bệnh lý tĩnh mạch phổi phải và trái (50%) Vòng phía trên van hai lá
LAA
vách ngăn bên trái
(lưu ý quy tắc này không áp dụng cho nhịp nhanh vào lại nút nhĩ thất, rung nhĩ, nhịp nhanh nút AV)
Nguồn:
Hình thái sóng p trong nhịp nhanh nhĩ http://content.onlinejacc.org/article.aspx?articleid=1137857&issueno=5
Nghiên cứu giành giải thưởng nghiên cứu lâm sàng, New Orleans, Louisiana, 2005.
41. Hãy gọi HEPARIN là 1 thuốc tiêu huyết khối!
Heparin được phát minh vô tình bởi Jay McLean, một sinh viên y khoa lâm sàng 26 tuổi năm 1916. Nó là một trong những khám phá vĩ đại trong y học, giúp chúng ta ngăn ngừa cục máu đông.
Như chúng ta đã biết cơ chế tác dụng của heparin, nó ràng buộc với các phân tử antithrombin 3 và ngăn hình thành cục máu đông nội tại và hoạt động như 1 tác nhân chống đông quan trọng.
Làm thế nào heparin hoạt động như tác nhân tiêu huyết khối?
Hệ thống huyết học của chúng ta có một cơ chế tiêu sợi huyết tự nhiên mạnh mẽ để bảo vệ chống lại tình trạng đông máu nội mạch không do bệnh lý. Gián tiếp qua anti thrombin, protein C, protein S, hệ thống hoạt hóa plasminogen … nồng độ chất hoạt hóa plasminogen mô (tPA) cũng giúp li giải cục máu đông trong lòng mạch.
Có một hằng số, cân bằng tinh tế giữa chất trợ đông, chất chống đông máu và phân tử tiêu sợi huyết. cục máu đông trong lòng mạch xảy ra khi chấn thương mạch máu .
Nhưng, một khi bị lăng nhục, máu lưu thông không còn là một khán giả im lặng. nó sẽ tấn công các cục khuyết khối. Antithrombin 3 là một phân tử như vậy. Thành công của việc ly giải phụ thuộc vào sức mạnh của các lực lượng tự nhiên. Hiện có hàng trăm quá trình li giải vi thể diễn ra mỗi ngày, ở bệnh nhân có bệnh mạch máu có thể sẽ nhiều hơn nữa. Tiêm liều cao heparin tĩnh mạch làm gì?
Heparin ngay lập tức ngăn quá trình trợ đông máu lại .Một trong những nguyên tắc quan trọng trong huyết học là “Thrombos hạ sinh huyết khối”. Đó là một vòng luẩn quẩn. Điều này ngay lập tức được giải quyết bằng heparin .
Điều này sẽ làm nhỏ cục máu đông chỉ giữ ở mức 2 cm. Sau đó, máu trong vùng lân cận ngay lập tức bắt đầu thấm vào cục máu đông. Heparin sẽ chuyển sang tác dụng tiêu sợi huyết, hủy fibrin hoặc làm tan huyết khối.
Có bằng chứng lâm sàng để gọi heparin là thuốc tiêu sợi huyết?
Trái ngược với các nguyên tắc khoa học thông thường, chúng tôi chỉ có bằng chứng lâm sàng. bằng chứng xét nghiệm không thể chứng minh heparin có thể làm tan cục máu đông. Là 1 người chuyên ngành về tim mạch và can thiệp, quan sát trên lâm sàng thấy heparin có tác dụng cục tốt giúp cục máu đông thoái triển về kích thước (Hoặc làm tan hoàn toàn) với phác đồ điều trị heparin .Hiệu quả thấy trong 48-72 giờ. Thậm chí 24 giờ đầu tiên. các tình huống lâm sàng chúng tôi đã dùng heparin đã ly giải thành công các cục máu là gì?
Thuyên tắc phổi cục máu đông LV cục máu đông LA
Huyết khối tĩnh mạch vỏ não Huyết khối tĩnh mạch sâu huyết khối mạch vành
Huyết khối tĩnh mạch cửa huyết khối tĩnh mạch thận
Nếu đó là sự thật, heparin là thuốc tan huyết khối, tại sao nó không được gọi là thuốc làm tan huyết khối?
Tại sao không ? Bạn tự quyết định!
Làm thế nào để heparin so sánh với các thuốc làm tan huyết khối lớn như Strepotiknase, Urokinase, Altepase, Retepalse, Teneckteplase (TNK TPA)?
trừ streptokinase không có các nghiên cứu so sánh sẵn có. Cố gắng nghiên cứu tác dụng heparin trên người sẽ bị coi là phi đạo đức.
Trong thuyên tắc phổi thuốc làm tan huyết khối và heparin có tác dụng tương tự trên huyết khối trong phổi. Một điểm quan trọng cần nhớ ở đây là, các thuốc tiêu huyết khối đều được dùng trong thời gian ngắn (Bolus / truyền 1 giờ) .luôn dùng sau truyền heparin. Tại sao chúng ta làm điều đó ? bởi vì chúng ta biết điều đó là quan trọng. Và không bao giờ chúng ta biết, bao nhiêu phần trăm cục máu đông ly giải bởi thuốc tan huyết khối và bao nhiêu bởi heparin. Trong liệu pháp tan huyết khối, heparin được coi như là một thuốc hỗ trợ cho streptokinsae nhưng trong thực tế streptokinase có thể bổ sung tác dụng cho heparin
Tầm quan trọng của heparin trong MI cấp
Dùng sớm heparin ngăn ngừa hình thành cốt lõi của các cục máu đông .Dùng sớm aspirin trong nghi ngờ STEMI cũng được công nhận bởi các bác sĩ. bolus heparin (10000 u) ngay lập tức có thể có ảnh hưởng lớn đến kết quả
Heparin được đánh giá như 1 thuốc làm tan huyết khối chỉ vì nó không có tác dụng trực tiếp trên huyết khối mà nó được coi là thuốc hạng dưới. (Một lý do khác vì nó rất rẻ!)
Heparin có tác dụng trong thời gia cửa sổ MI cấp (Class 3 bằng chứng theo AHA) Nên sử dụng sớm đặc biệt trong tình huống khẩn cấp
42. Sóng J không phải là sóng “kích thích”. . . nó chỉ là 1 sóng trong ECG Điểm J là một điểm quan trọng trong ECG trong quá trình khử cực để tái cực, là thời gian đóng các kênh natri và mở kênh kali trong giai đoạn 0-1.
Nếu các kênh kali kích hoạt hơi sớm và giành quyền chỉ huy từ kênh natri ta có mô hình tái cực sớm .Khi điều này xảy ra, các điểm J của ECG cho ta thấy một sóng dễ thấy được gọi là sóng J, ban đầu được hiểu là sóng nối giữa QRS và đoạn ST (Bây giờ có người hiểu là sóng kích thích). Kênh Kali hoạt động sớm nâng đoạn ST chênh lêleehay gặp nhất trong thiếu máu cục bộ không có ST chênh
* J sóng ở hạ thân nhiệt được gọi là sóng Osborne và có thể không liên quan đến ERS
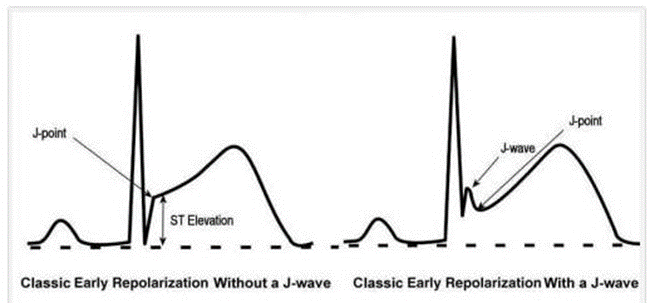
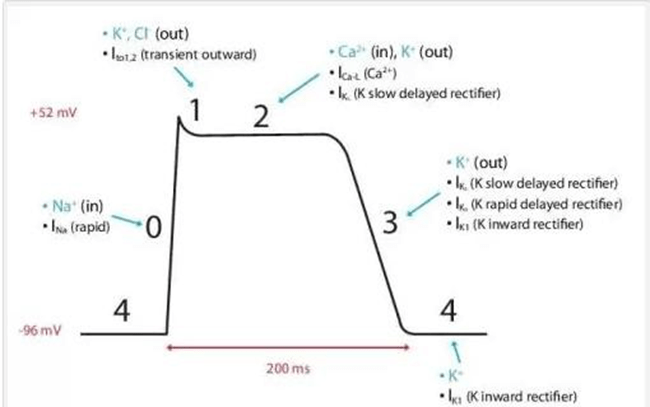
Phase 1 khi ion kali nhanh chóng ra ngoài và giảm điện thế hoạt động. phụ thuộc vào mật độ của kênh K + ở thượng tâm vị được phân bố không đồng nhất .ở đó có vẻ có gradient nồng độ dọc theo thượng tâm và màng trong tim, làm cho sóng J dễ xuất hiện và thấy rõ. Điều này đặc biệt đúng với nam giới chơi thể thao, có 1 số bằng chứng cho thấy có liên quan tới androgen. ở đây sẽ có sự chồng chéo giữa hội chứng Brugada và ERS
1 số nghiên cứu gần đây thấy ECG có sóng J làm tăng nguy cơ VF trong giai đoạn
―reentry- vào lại‖ khi bệnh nhân có ACS tiến triển. (hình ảnh có sóng J hay gặp ở những bệnh nhân có VF nguyên phát sau stemi).
Hiện tại người có hội chứng ERS (tái cực sớm) không triệu trứng có sóng J không nên làm điện sinh lý (có thể gây VF nếu bị kích thích thích hợp)
Thực tế sóng J ở thanh niên thường gợi ý họ có trái tim khỏe mạnh.
43. Có nhịp ngoại tâm thu (nhịp lạc vị) xảy ra ở nút xoang? Nó được gọi là xoang tâm thu sớm SPD
nhịp lạc vị hoặc khử cực sớm là rối loạn nhịp hay gặp nhất.
Phần lớn nhịp ngoại tâm thu là lành tính. Khi xaỷ ra trong điều kiện thiếu máu tim cục bộ sẽ có thể dẫn tới loạn nhịp
Trươc đây nhịp ngoại tâm thu gặp trong A.Ventricle: Ngoại tâm thu thất (VPD) B.Atrium: ngoại tâm thu nhĩ (APD)
C. bộ nối AV: ngoại tâm thu bộ nối (JPD).
Nếu bạn lưu ý, một trong những cấu trúc quan trọng không có tron danh sách.
Vâng, đó là nút xoang SA node. Liệu nó cũng có thể khử cực sớm?
Khi nào bạn nghi ngờ SPD (ngoại tâm thu xoang)
Thường xuấ hiện đột ngột, nhịp xoang trùng vào nhịp xoang trước đó. Tiếp đó sẽ có khoảng ngừng xoang.
sóng P tương tự như sóng p trước.
dễ có xu hướng chẩn đoán APD hơn là SPD. SPDS có xu hướng xảy ra ở nhịp đôi (bigeminy) Chẩn đoán phân biệt
Loạn nhịp xoang và ngừng xoang APD
Nút xoang có 1 phần vòng lại (Part of SA node reentry) Block xoang
Làm thế nào để phân biệt loạn nhịp xoang với(SPD)?
Loạn nhịp xoang thường xảy ra với nhịp tim chậm
Nó không có kiểu ―có-mất‖ mà nó thay đổi từ từ
Ý nghĩa lâm sàng
Đây là một rối loạn nhịp tim không quan trọng trên lâm sàng. Có lẽ vì thế mà nó không mấy phổ biến
* Nhưng nó có thể làm bối rối trong việc chẩn đoán
44. Nếu thiếu máu cục bộ dễ gây rối loạn nhịp thất, Tại sao loạn nhịp ít gặp trong NSTEMI?
hội chứng mạch vành cấp là cấp cứu tim hay gặp nhất. STEMI và NSTEMI là hai chi lâm sàng của ACS.
Những bí ẩn kể từ khi giải mã, sự khác biệt chính giữa hai thực thể này là STEMI là tắc đột ngột và hoàn toàn trong khi NSTEMI xảy ra chậm và không hoàn toàn
Loạn nhịp tim trong ACS
1/3 số bệnh nhân STEMI đến viện còn sống, lí do là STEMI rất dễ gây rung thất
Trái ngược với điều này, gần như tất cả các bệnh nhân NSTEMI đến bệnh viện đều còn sống! vì sao ?
Cả hai đều là ACS, nếu thiếu máu cục bộ là nguyên nhân nguy hiểm gây loạn nhịp thất thì NSTEMI cũng có thể dẫn đến loạn nhịp thất?
những yếu tố gì bảo vệ chống lại chứng loạn nhịp tim trong NSTEMI?
45. Uống amiodarone khác amiodarone dùng đường tĩnh mạch IV?
Amiodaron đã mang lại một sự thay đổi lớn trong điều trị loạn nhịp thất trong vài thập kỷ qua. Nó là một loại thuốc chống loạn nhịp mạnh mẽ, với 4 lớp hành động (phân loại williams vaugan.) Nó chẹn natri, kali, canxi và beta receptor . Do đó không có gì ngạc nhiên, amiodarone được đặt tên là loại thuốc chống loạn nhịp phổ rộng vì nó hoạt động trên rất nhiều các thụ thể tim.
Tất nhiên, tác động lớn nhất được cho là trên kênh kali (lớp tác dụng thứ 3) kéo dài thời gian trơ giúp chấm dứt loạn nhịp. Trong khi, amiodarone do cấu trúc tương tự như hormone tuyến giáp, phải mất một thời gian dài để đạt được nồng độ ổn định trong huyết tương . dùng đường uống có thể mất đến 1 tuần mới phát huy tác dụng.
Nếu amiodarone là một loại thuốc tác dụng chậm, có ngạc nhiên không khi amiodarone IV lại dùng trong các trường hợp cấp cứu VT?
có sự khác biệt giữa cơ chế hoạt động đường dùng amiodarone uống và IV
lớp tác dụng thứ 3 của amiodarone xuất hiện cuối cùng khi dùng đường uống. QT kéo dài hiếm khi xảy ra sau liều bolus iv amiodarone. Vì vậy, VT sẽ châm dứt ngay. Nhiều người tin rằng tác dụng chẹn kênh canxi và beta receptor là yếu tố góp phần gây loạn nhịp thất trở lại
46. Vấn đề điều trị trong STEMI sau dùng tiêu huyết khối thrombolysis xuất hiện nhịp xoang nhanh
Nhịp xoang nhanh trong những giờ đầu của STEMI là rối loạn nhịp tim rất hay gặp. vấn đề tưởng như đơn giản này thực sự đáng lo ngại đối với nhiều chuyên gia tim mạch và làm họ lo đến mất ngủ (trong khi bệnh nhân thì ngủ thoải mái!)
Tầm quan trọng của nhịp xoang nhanh trong STEMI chủ yếu nằm trong việc trả lời những câu dưới đây
A. nhịp xoang nhanh có bù? khi tâm thất trái đang vật lộn để duy trì cung lượng tim và làm việc cật lực để duy trì các chỉ số tim quan trọng
Hoặc là
B. nhịp xoang nhanh nhưng bù không thích hợp? Đó là đáp ứng với trương lực adrenergic cao và đáp ứng thần kinh từ cơ tâm thất bị thương.
Cần nhớ lại, tim đập nhanh dưới mọi hình thức đều bất lợi sau STEMI vì nó làm tăng mức tiêu thụ oxy của cơ tim MVo2. Đây là lý do, các thuốc chẹn beta được dùng trong tình huống này. nhịp tim nhanh bù trừ chống LVF sắp xảy ra.
Nhịp tim thường khoảng 120 / phút. nó có thể vượt lên đến 140 hoặc hơn. (Thông thường dao động quanh 120 (+/- 5) .stress hay lo âu làm dao động lớn hơn
Nhịp nhanh kèm s3 gợi ý chẩn đoán LVF.
Làm thế nào để kiểm soát nhịp nhanh xoang trong STEMI?
chẹn beta là chính. Bất kỳ thuốc chẹn beta nào như metoprolol, atenolol, carvidilol đều có thể dùng. Uống metoprolol có thể lên đến 50 mg. sử dụng thuốc chẹn beta chủ yếu có tác dụng trong nhịp nhanh mất bù. Vì vậy, điều quan trọng là phải nhận ra, carvidilol
không thể được sử dụng tự do, chỉ dùng trong nhịp xoang nhanh có nguy cơ LVF sắp xảy ra hoặc STEMI có triệu chứng.
* Các nguy cơ gây nhịp nhanh như dopamine, dobutamine vv nên loai trừ
Các thuốc khác được lựa chọn là
Digoxin (nó vẫn rất tốt trong NMCT cấp với nhịp nhanh xoang dai dẳng, Ưu điểm là, nó có thể được sử dụng mà không cần phải phân biệt được đó có bù hay mất bù) Ivabradine, một loại thuốc kỳ diệu chọn lọc giảm tần số xoang mà không ảnh hưởng co bóp
47. Các khái niệm sai lầm trong co thắt mạch vành!
co thắt động mạch vành là một thực thể thường được thảo luận trong tim mạch lâm sàng. Được mô tả bởi nhiều thập kỷ trước là cơn đau thăt ngực Prinzmetal .không có khái niệm cơn co thắt vành ổn định ở bệnh nhân đau thắt ngực không ổn định như nào là co thắt động mạch vành?
Tình trạng này được cho là rất phổ biến trong ACS, nhưng rất khó khăn để xác định. thực tế nhiều trường hợp nghi ngờ trên lâm sàng và không bao giờ có thể kiểm chứng. Hiện đã có rất nhiều test để kiểm tra co thắt mạch vành như ergonavine … không có xét nghiệm nào chứng minh được điều này.
Các tình huống lâm sàng khi co thắt mạch vành xảy ra?
Lâm sàng đã dạy chúng ta co thắt mạch vành có thể xảy ra trong tất cả trường hợp hội chứng mạch vành cấp tính hoặc thậm chí hội chứng mạch vành mạn tính.
Một số người tin ở STEMI sẽ có sự góp phần của co thắt mạch vành.
Trong NSTEMI / UA co thắt mạch vành là một cơ chế bệnh sinh quan trọng
Mối liên hệ giữa sự co thắt mạch vành và điện tâm đồ là gì?
Những sai lầm phổ biến nhất ở các bác sĩ tim mạch là co thắt mạch vành phải có ST chênh. Các giáo trình tim mạch cổ điển giảng dạy tất cả các nơi trên thế giới đã dạy các bạn như vậy. Thực tế sự co thắt động mạch vành, không bao giờ có thể có tác động trực tiếp đến điện tâm đồ. (Trừ khi, cơ trơn mạch vành tạo ra được sóng ST). Vì vậy, hiệu quả co thắt của nó là thông qua tác động của nó tới lưu lượng máu cơ tim.
Do đó, không phải co thắt động mạch vành sẽ dẫn tới chuyển động của đoạn ST. những tác động của lưu lượng máu cơ tim tới cơ tim, màng trong tim, thượng tâm, thượng tâm vị sẽ tác động tới đoạn ST
Biểu hiện trên ECG của co thắt động mạch vành là gì?
ST chênh xuống ST chênh lên
thay đổi sóng T (cao hoặc âm sâu)
Đoạn ST Flattish hoặc ECG hiếm khi, hoàn toàn bình thường cho thấy lực lượng ST cân bằng. Đa số sẽ thấy ST chênh xuống. hình ảnh cổ điển trong nhiều trường hợp NSTEMI / UA.
ST chênh xuống biểu hiện ưu thế của co thắt mạch vành
Làm thế nào co thắt mạch vành có thể nâng đoạn ST chênh lên?
Nếu nó có thể gây ra thiếu máu cục bộ xuyên thành sẽ nâng đoạn ST chênh lên. Nhưng hiếm khi gặp. Để dẫn đến thiếu máu cục bộ xuyên thành, phải co thắt toàn bộ và kéo dài ít nhất vài phút.
* 1 số ít trường hợp co thắt ảnh hưởng vùng trên thượng tâm vị nhiều hơn màng trong tim gây st chênh lên.
Tác dụng của nitroglycerine trên co thắt mạch vành?
Tác động rất mạnh. Nó giữ ST ở vị trí trung lập .giảm đau thắt ngực trong UA / NSTEMI do giảm co thắt mạch vành
co thắt mạch vành do thần kinh hay sinh hóa?
Nguyên nhân liên quan sinh hóa, tín hiệu thần kinh cũng dẫn truyền trung gian bởi sinh hóa .
các chất trung gian sinh hóa gây co thắt mạch vành là gì?
Canxi ở cơ trơn: là nguyên nhân trực tiếp cho sự co thắt Dẫn truyền thần kinh: catecholamine,
Thromoxane A2 mà là một chất co mạch mạnh mẽ
co mạch vành và co thắt mạch vành là 1?
hai thuật ngữ đồng nghĩa. Co mạch thường được sử dụng để chỉ co mạch nhỏ trong khi co thắt thường liên quan tới mạch thượng tâm vị lớn.
các yếu tố quyết định tới co thắt động mạch vành là gì?
Vị trí (RCA> LCA)
Đặc điểm tổn thương Thành phần huyết khối Tính cấp tính
Hoạt động của hệ adrenergic và thần kinh
48. Tại sao inferior MI ít nguy hiểm?
Nhồi máu cơ tim (STEMI) xảy ra ở 2 vùng cấp máu riêng biệt . LAD cung cáp thành trước, RCA/LCX cấp máu thành sau dưới.
NMCT thành dưới ít nguy hiểm hơn so với thành trước. Đúng hay sai ?
Trả lời: Về cơ bản đúng trong hầu hết các tình huống.
Thành dưới của tim (nói đúng ra không có thành của tim, chỉ có bề mặt và pha trộn với bề mặt tạo bởi cơ hoành mà mặt sau tim.nmct thành dưới có thể do tắc RCA hoặc LCX.theo ước tính 75% thất trái cấp máu bới LCA.
Khi làm tan huyết khối, nhiều nghiên cứu cho rằng độ chênh của ST đa phần đều giảm kể cả không dùng tiêu huyết khối, điều này có nghĩa dùng thuốc tiêu huyết khối phần lớn thành công khi tắc RCA. Sự khác biệt nổi tiếng trong khiếm khuyết về dẫn truyền giữa thành trước và dưới trong NMCT (block AV ở thành dưới trong MI, thường thoáng qua, không tiến triển hiếm khi cần dùng máy tạo nhịp vĩnh viễn). Trong giai đoạn cấp tính sốc tim xảy ra (có thể kèm sốc- RV). Ngay cả khi đó phân suất tống máu ở nmct thành dưới hầu như luôn luôn trên 40%. Trong nhiều trường hợp EF không bị ảnh hưởng gì cả.
yếu tố giải phẫu
Mặc dù có những yếu tố trên nhưng nmct thành dưới không nên coi nhẹ, đặc biệt khi nó lan rộng về phía sau và bên (hiếm khi ra thành trước) . Trong khi lan ra thành sau thường tiên lượng tốt thì thành bên lại không như vật. có lẽ do khi lan rộng ra phần bên liên quan các vách của LV dễ gây LVF. Lan rộng ra thành sau chủ yếu liên quan bề mặt thất phải, ít ảnh hưởng huyết động.
49 huyết động ở mạch vành khi tắc 100%?
Tắc hoàn toàn động mạch vành hay gặp trong CAD đặc biệt là trong đau thắt ngực ổn định mạn tính. Bình thường lưu lượng máu mạch vành là 5% lưu lượng tim khoảng 250-300ml /
p. nhịp tim trung bình 70l/p có thể bơm 5cc chia đều cho hai động mạch vành. Điều này có nghĩa, chỉ vài CC (2-3cc) của máu vào từng động mạch vành với mỗi chu kỳ tim.
Khi một trong những động mạch vành tắc hoàn toàn điều gì sẽ xảy ra?
A.Tổng lượng máu động mạch vành vẫn có thể duy trì bình thường lúc nghỉ hoặc giảm nhẹ
B. Người ta tin rằng, động mạch vành không bị tắc có thể nhận máu thay bên đối diện. Điều này có thể giải thích vì sao đường kính động mạch vành tăng lên ở các động mạch không bị tắc nghẽn.
C. theo tự nhiên, các động mạch vành bên đối diện sẽ chia sẻ 50% lượng máu cấp qua các nhánh bên nếu có.
D. nếu không có các nhánh bên, các động mạch vành không bị tắc có thể được tưới máu gấp đôi .
50. Tại sao chúng ta nhìn V1 chẩn đoán RVH nhưng nhìn V4R để chẩn đoán nhồi máu RV?
Tâm thất phải là buồng tim nằm phía trước nhất và có hình tam giác. Mặc dù các thành của RV không được phân định rõ ràng, nó có trước, sau và mặt tự do.
Cấu trúc giải phẫu của RV là như vậy nên nó không thể có RVH đồng tâm (như LVH). Trong thực tế, phía bờ tự do (mặt bên) phì đại trong PHT/ Hẹp động mạch phổi. mặt sau dưới thất phải ít khi phì đại
RV nằm phía trước nhất, ngay bờ trái xương ức nên RV rất gần với thành ngực. nhìn V1 thấy R cao
Điều gì xảy ra trong RVMI?
Thật không may, khi chúng ta đề cập đến RVMI, chúng tôi thường không cố xác định hoặc ước tính kích thước. Hầu hết RVMI xảy ra như ở thành sau, dưới MI . do đó ít gặp ở mặt trước của RV. Tuy nhiên, nó có thể gặp khi RCA tắc nhánh RV lớn ở mặt trước RV Mặt trước RVMI có thể xảy ra như 1 phần của LAD MI, nếu có nhánh đi qua bề mặt RV.
Hầu hết RVMI không liên quan đến mặt trước của RV vì vậy ít khi có ST chênh lên. Hơn nữa, nếu thành sau RV MI xảy ra (Mà thường là trường hợp!) V1 không bao giờ có ST chênh lên mà có xu hướng chênh xuống trong V1, V2.
Lợi thế của V4 R?
V4R ghi lại áp lực RV từ xa, không bị ảnh hưởng bởi ST thành sau dưới. Do đó ST chênh lên 1mm trong chuyển đạo bên thất phải có độ nhạy và đặc hiệu cao trong chẩn đoán RVMI.
Khi nào V1 có ST chênh lên trong RVMI?
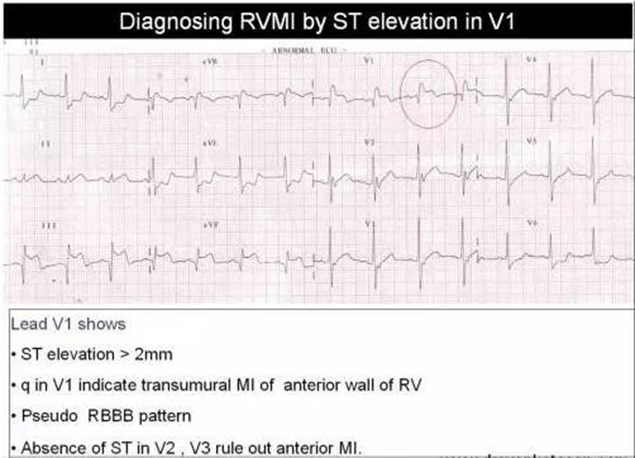
Nếu thành trước RV tham gia (Tức là RVMI thành trước) ST chênh lên có thể gặp ở V1 Hiếm khi q RBB có thể xảy ra ở V1 trong trường hợp chỉ có RVMI đơn thuần
51. Na đi vào Kali đi ra Canxi đi vào mới có hoạt động điện thế. Câu hỏi đặt ra là tại sao kali ảnh hưởng lớn đến ECG còn nồng độ Na thì ngược lại?
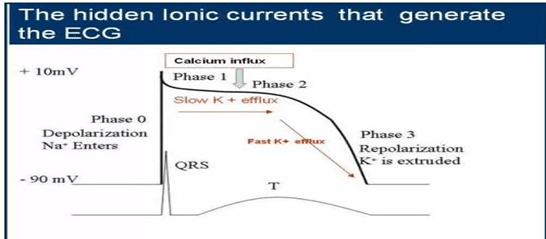
ECG ghi hoạt động điện của tế bào cơ từ bề mặt cơ thể . ECG thể hiện dòng chảy của các ion. Khi nhìn vào phức QRS, ta sẽ thấy các ion Na đi vào trong .Khi đoạn ST / QT bắt đầu là lúc canxi đi vào (Một số clorua cũng vaò theo) và K + bắt đầu rời tế bào . nhìn thấy sóng T nhọn hoặc tù cho chúng ta thấy sự hoạt động của kênh kali.
phase 0 có sự di chuyển nhanh chóng của các ion natri vào trong tế bào. Trái ngược với điều này, trong pha tái khử cực của các tế bào cơ kali đi ra chậm hơn cũng với dòng canxi đi vào chậm tạo hình mái vòm .phase 3 bắt đầu có sự đi ra nhanh chóng của K tương ứng với sóng T.Phase 4 xảy ra trong giai đoạn khử cực tâm trương.
Lưu ý: * Na thoát ra từ các tế bào xảy ra rất nhanh ( không được đề cập trong các sơ đồ.Tất cả các loại thuốc chống loạn nhịp nhóm 1 đều chặn kênh này)
Rõ ràng, sóng T liên quan nhiều tới sự thay đổi nồng độ kali. sóng t cao cho thấy nồng độ kali nội bào cao và sự di chuyển ra ngoài của K + sẽ kéo dài. Tương tự khi có hạ kali máu, sóng T đảo ngược có liên quan tới sự kéo dài khoảng QT.
Trong khi sóng T có liên quan đến K +, QRS lại liên kết chặt chẽ với nồng độ Na +, nhưng nồng độ natri hiếm khi thay đổi QRS tại sao?
Hạ natri máu là một rối loạn điện giải thông thường, đặc biệt là ở người già và bệnh nhân điều trị bằng thuốc lợi tiểu. hạ natri máu do dư thừa nước tự do hay gặp trong bệnh nhân CHF. Trong khi ECG rất nhạy để chẩn đoán tăng kali huyết, hiếm có nhạy với tăng natri huyết.
Điều này chủ yếu là do hai lý do .quá trình khử cực do Na gây ra rất nhanh (tối đa 80ms). Tốc độ K + ra ngoài chậm lên đến 400 ms. Không giống như K +, Na + không thể kéo dài khoảng QT điều này là do thực tế các kênh Natri có gradient lớn ngay cả khi nồng độ natri huyết thanh giảm. Hơn nữa, Na là một cation di động và có ảnh hưởng rất nhỏ với tế bào cơ.
Nhưng, thi thoảng vẫn gặp QRS rộng hoặc dẫn truyền bất thường do tăng natri huyết . Tương tự như vậy các ion K + có tác động lớn đến nút xoang và nút nhĩ thất. Nó có thể ức chế chúng, mặc dù có thể có hậu quả nghiêm trọng.
Lưu ý: * Na thoát ra từ các tế bào xảy ra rất nhanh (không được đề cập trong biểu đồ), điều này rất quan trọng. các thuốc chống loạn nhịp loại 1 hoạt động trên kênh này
52. ATROPIN NGƯỜI HÙNG THẦM LẶNG
Atropine, chiết xuất từ cây Belladona là một loại thuốc tim mạch quan trọng. nó cứu sống bệnh nhân tim mạch nhiều hơn so với bất kỳ loại thuốc nào khác. Nó xử trí ngay lập tức các trường hợp nhịp chậm như ma thuật. Nó là thuốc chống loạn nhịp mạnh nhất, nhưng điều đáng mỉa mai là nhiều sách vở phác đồ chính thống về tim mạch lại không đề cập đến điều này trong khi thảo luận về các chất chống loạn nhịp tim.
Trong thời đại của sartans, ức chế 2b3a, fondaparinux . Chúng ta không có thời gian rảnh rỗi để nhận ra rằng nhiều trường hợp tử vong tim mạch đã được ngăn ngừa bằng atropine hơn tất cả các loại thuốc này lại với nhau. Nó vẫn được dùng hàng ngày, được coi như 1 thuốc tầm thường nhưng không bao giờ được công nhận xứng đáng chỉ vì nó quá rẻ, thậm chí nó không tiếp thị, không quảng cáo cũng như không có cả ngày sinh nhật Cơ chế tác dụng
Vị trí tác dụng: Nó chặn M2 (thụ thể Muscaranic).
+Tác dụng hạn chế những hoạt động tim mạch.
-nút xoang tăng tốc
-Nút nhĩ thất tăng tốc
+Tác dụng trên điện tâm đồ Nhịp xoang nhanh
khoảng PR ngắn
dây thần kinh phế vị phân bố đa dạng ở thần kinh tim và mạch máu. hội chứng mạch vành cấp tính đặc biệt liên quan đến thành sau dưới làm tăng trương lực phế vị gây nhịp chậm nghiêm trọng va tụt huyết áp. Trong phòng can thiệp mạch, các thao tác với guide wire có thể gây những phản xạ mạch máu
Hơn nữa, bất cứ khi nào đau nhiều, trung tâm nhận cảm đau trong thân não và đồi thị có tác dụng kích thích nhân dây phế vị (Vagal)
Điều gì xảy ra nếu phản xạ phế vị không được điều trị?
Chúng ta đã thường xuyên dùng thuật ngữ “phản ứng phế vị‖ 1 cách vô thưởng vô phạt. Lý do chính là do sự xuất hiện phổ biến của “ngất do phản xạ phế vị” – thực thể lành tính. ở những người khỏe mạnh khi chuyển từ tư thế đứng thẳng sang nằm có thể gây ngất.
Điều này hoàn toàn khác khi xảy ra ở bệnh nhân trong can thiệp mạch vì có thể gây ngừng tim và tử vong
Atropine là Đấng Cứu Thế ở đây. Bạn có thể tưởng tượng một thế giới sẽ thế nào nếu không có atropin.
nó hoạt động nhanh chóng và kịp thời với gần 100% thành công trong đảo ngược phản xạ phế vị trong vòng chưa đầy 60 giây chỉ với 2cc atropin
Có thuốc nào thay thể trong xử trí phản xạ phế vị hơn atropine?
Không hề có
Các ứng dụng khác của atropine trong thực hành tim mạch
Phối hợp với dobutamine để tăng nhịp tim.
Nó có thể được sử dụng để phân biệt 2 type block AV cấp 2. Các mobitz loại 2 trở nên xấu hơn trong khi loại một tăng tốc.
Atropin cũng được sử dụng với các chuyên khoa khác như khoa Mắt, tiền mê, hen phế quản, ngộ độc.
tương lai với loại thuốc này?
Vẫn sáng sủa nhưng có rất ít công ty điều chế loại thuốc này. Nó là một loại thuốc không thu được lợi nhuận nhưng lại là cứu cánh tuyệt vời trong tim mạch
cùng với 1 loại thuốc cũng đóng vai trò cực lớn trong tim mạch như digoxin cũng gần như không chịu nổi so với sự phát triển của các thuốc khác trong thời đại y học hiện đại
53. Tại sao không có RS ở chuyển đạo trước tim đặc hiệu trong chẩn đoán VT? Các tiêu chí phổ biến nhất để phân biệt VT và SVT được dựa vào tiêu chuẩn Brugada vào năm 1991.
Sự vĩ đại của tiêu chuẩn này luôn kèm theo một câu hỏi duy nhất là có thể khẳng định VT trong đa số trường hợp hay không?
Nếu không có RS ở chuyển đạo trước tim? Nếu câu trả lời là có thì nó là VT 100% Giải thích vấn đề này khá dễ dàng?

Điều này là do, khi dùng thuật ngữ “không có RS” nghĩa là có sự xuất hiện của 3 phức hợp điển hình sau đây của VT
1. QS
2. QR
3. R đơn hình
Hai trong số chúng gợi ý có sóng Q ở V 1-V6 .Đây là bằng chứng cho thấy có tổn thương thất và rất ít hoạt động điện thế đi về phía trước thành ngực, hầu như luôn gặp ở VT
thứ ba là R đơn hình
QRS rộng, đơn hình lần nữa khẳng định đây là VT vì hiếm khi SVT đi cùng với RSR ‘(Các giai đoạn trơ nhánh phải có ít nhất 1 r nhỏ còn SVT thì không)
Vì vậy, nếu không có RS thì nó phải là VT!
những khó khăn phải đối mặt khi áp dụng bước đầu tiên này của tiêu chí Brugada là gì?
Điều thú vị cần lưu ý, các tiêu chuẩn y học hoàn hảo thường chỉ có trong sách giáo khoa thôi! Có thể nhìn ra phức RA dễ dảng? để phân biệt RS từ QS ngay cả bởi một bác sĩ tim mạch giàu kinh nghiệm cũng có thể rất khó khăn chứ không nói là chúng mình
Trong thực tế, chúng ta nên mong chờ Brugada tìm ra tiêu chuẩn mới hơn cho dễ áp dụng
Nếu không có RA ở chuyển đạo trước tim sẽ chẩn đoán 100% VT. Nhưng để nhìn ra được RS hay không lại là chuyện khác =)) so funny!
54. Hãy để tôi giúp bạn xóa hoang tưởng về nhịp nhanh thất: là loại nhịp nhanh đều hay không đều?
nhịp nhanh thất QRS rộng là loại nhịp nhanh hay gặp nhất. Bạn thường được dạy VT là loại nhịp nhanh có QRS rộng và nhịp đều, nhưng thực tế chả phải như vậy
Có vài trường hợp nhịp không đều. Tất nhiên, không đều này có thể do các rối loạn liên quan thấy được trên ECG
Chúng ta biết trong AV phân ly, các xung xoang luôn cố gắng đi vào tâm thất và tìm cửa tại nút AV để đi qua.thậm chí một phần nhỏ của một giây là đủ cho sự thúc đẩy dẫn truyền xoang lẻn qua nó, câu hỏi duy nhất là thời gian. cần lưu ý rằng dẫn truyền AV nguyên vẹn hiếm khi xuất hiện nhịp kết hợp và nhịp bắt giữ (fusion – capture beat). Vì vậy, bất cứ khi nào dẫn truyền AV có vấn đề, sẽ xuất hiện 2 nhịp kia, rõ ràng sẽ xuất hiện VT không đều. có thể gặp tới hơn 20% trường hợp .Vì vậy nó thực sự là sai lầm nếu cho rằng sự hiện diện của bất thường nên làm cho một chẩn đoán của VT.
Một lý do khác làm VT có thể không đều vài phút sau khi xuất hiện VT là do điện thế dạo động trước khi nó đạt được trạng thái ổn định
VT thường xảy ra sau rối loạn (cơ tim mấp mô, xơ xẹo). Như vậy VT sẽ gặp nhiều hơn ở bệnh nhân có sẹo MI, đường dẫn truyền dài và quanh co gây trì hoãn dẫn truyền . Nhưng, một khi VT đạt đến tốc độ mong muốn nó sẽ trở nên khá đều.
VT sau uống thuốc: tác dụng của Amiodarone.
Hiệu quả của lớp 1 hoặc 3 thuốc chống loạn nhịp trên VT sẽ giảm tỷ lệ VT, QRS rộng và tần số không đều. đặc biệt sau tích lũy thuốc amiodarone
VT đa hình
VT đa hình rõ ràng sẽ không đều.xoắn đỉnh là ví dụ điển hình. nhịp nhanh thất đa ổ (MVT)
hiếm khi nhắc trong y văn. tâm thất được bảo vệ chống lại các rối loạn nhịp tim như vậy dư lào? Khi VPDs đa ổ xảy ra thường xuyên tại sao nó không gây MVT? Có thể, VT xuất hiện như 1 máy tạo nhịp và dập tắt tất cả các hoạt động điện xung quanh.
VT có thể chuyển từ tiêu điểm này sang vị trí khác. Vì vậy khi trong thời điểm chuyển đổi hoặc cạnh tranh giữa 2 điểm mà ghi ECG có thể thấy nó không đều
Vì vậy
VT có QRS rộng và nhanh đều trong phần lớn trường hợp. Nhưng chỉ áp dụng quy tắc này ở VT đơn hình 1 ổ. Phần lớn QRS rộng nhanh không đều liên quan tới AF dẫn truyền qua đường phụ ngược chiều
55. SỐ PHẬN CỤC MÁU ĐÔNG Ở TIM
Một trong những bệnh nhân của tôi bị rung nhĩ gần đây đã đột quỵ do tắc động mạch não giữa MCA phải dẫn đến liệt nửa mặt bên trái . Đã dùng warfarin, nhưng đột quỵ nguyên nhân được xác định do cục máu ở tim.
Tại sao các cục máu đông từ tim hay đi lên não? Có không có nơi nào khác cho nó để đi?
đơn giản vì “Đó là số phận của bạn và mong muốn của cục máu đông”. Trong thực tế, cục máu đông có thể di chuyển đi nhiều nơi nhưng phụ thuộc vào 1 số yếu tố
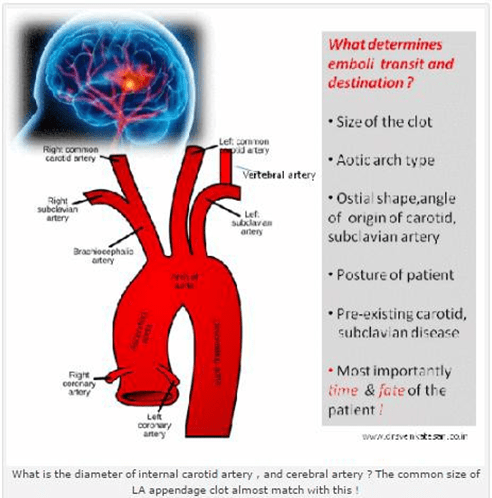
Nó có thể đi thẳng xuống chân, thận, ruột hoặc chi trên .Tất cả đều nguy hiểm. Rất hiếm khi nó có thể chui vào động mạch vành.Nếu cục máu đông đi đến chân bạn có nguy cơ liệt 1 chi cấp thay vì liệt nửa người …
Điều gì quyết định đích đến của cục máu đông khi ra khỏi tim (embolism)?
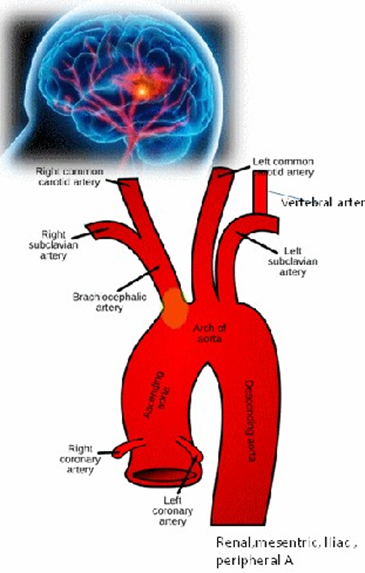
Các yếu tố sau có thể liên quan: Kích thước và hình thái cục máu đông Giải phẫu cung động mạch chủ
Ví dụ thuyên tắc động mạch đốt sống hiếm gặp vì nó là nhánh đánh số 2. Các biến thể trong giải phẫu vòm động mạch chủ
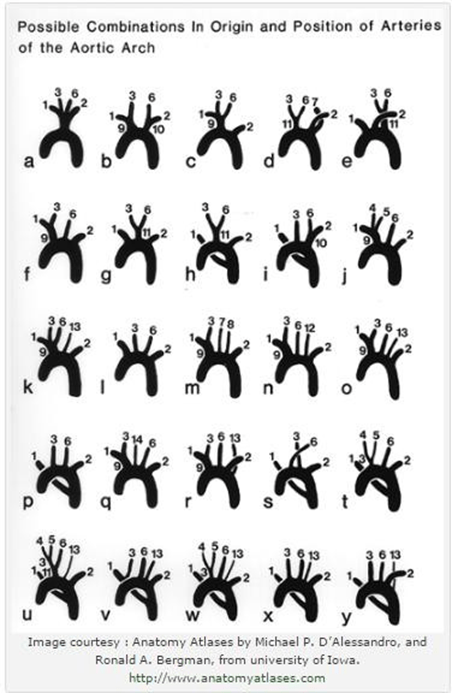
Thật đáng ngạc nhiên, con người có thể có nhiều loại vòm động mạch chủ như bảng chữ cái tiếng Anh. Do đó có vô số cách để các cục máu từ tim gây tắc ở vô số nơi
56. NHĨ THẤT PHÂN LY ÍT XẢY RA KHI NHỊP NHANH THẤT
AV phân ly là dấu hiệu để chẩn đoán VT. ECG phân ly AV có thể gồm: sóng p không liên quan QRS, nhịp kết hợp, nhịp bắt được (capture beat). Thật không may điều này chỉ xảy ra ở khoảng 40% bệnh nhân VT. (Fusion beat ở VT cũng được gọi là Dressler’s beat) Trong sinh lý bình thường, mặc dù tâm nhĩ là thụ động, bất lực về hoạt động cơ học, nhưng nó có chức năng giám sát tâm thất và chi phối điện. Trong thực tế, tâm nhĩ và nút nhĩ thất, ra lệnh cho tâm thất phải hoạt động ở mức nào. Vì vậy, ở người bình thường có nhịp xoang, có sự kết hợp hài hòa mối liên kết AV
Phân ly AV là gì?
Để xảy ra AV phân ly tức mất mối quan hệ sinh lý và liên kết điện giữa nhĩ và thất. xung nhĩ phải được chặn tại ngã ba AV.
block này có thể ở chức năng hoặc do thực thể, một phần hay toàn bộ, liên tục hoặc gián đoạn. Điều này xảy ra chủ yếu ở trong bệnh lý bộ nối AV như CHB …, mà kết quả gây phân ly AV hoàn toàn. Nguyên nhân quan trọng tiếp theo gây AV phân ly, là do sự can thiệp từ máy tạo nhịp tim
tâm nhĩ làm gì khi tâm thất bắt đầu dẫn truyền nhanh chóng và độc lập như trong nhịp nhanh thất?
Khi tâm thất, bắt đầu dẫn truyền độc lập với tốc độ> 200 mỗi xung và cố gắng dẫn truyền ngược qua đoạn giao nhau ở AV. Đồng thời, sự thúc đẩy nhịp xoang khoảng 70 / nhịp cạnh tranh với nhịp từ thất. Đáng buồn thay, tâm thất chủ yếu thành công trong cuộc đua này và hầu hết các xung từ thất ngược lên ngã 3 AV và cấu kết với xung từ nhĩ đến. Khi điều này xảy ra, sẽ xảy ra phân ly AV. Điểm quan trọng ở đây là, nếu AV dẫn truyền ngược nhiều lần tốc độ nhanh và thời gian tối ưu, nó có thể vượt qua nút AV mà không gặp khó khăn và tới tâm nhĩ , sau đó thậm chí còn làm thao túng nút SA và đặt lại nó.
Nếu VT đang liên tục dẫn truyền ngược nó có thể ngăn chặn nút SA phát xung. Điều này làm cho mất hoàn toàn sóng P (Lưu ý thận trọng: Nếu bạn nói VT là một trong những nguyên nhân làm mất sóng P bạn có thể trượt trong hội đồng chuyên môn tim mạch, nhưng điều này vẫn đúng trong thực tế)
Vì vậy, quá trình khử cực và co nhĩ Trong VT là một vấn đề phức tạp. Nó phụ thuộc chủ yếu vào cường độ dẫn truyền xung từ tâm thất. cường độ dẫn truyền từ tâm thất ngược lên quyết định vị trí sóng p:
Sóng P có thể hoàn toàn mất P có thể chạy trước
Trên QRS Trong T
Trong thực tế sóng P nghĩa đen có thể xuất hiện ở bất kỳ nơi nào trên dải của VT
Khi nào nhịp kết hợp (fusion) xảy ra? Khi nào nhịp bắt được (Capture) xảy ra? Điều này một lần nữa được xác định bởi giai đoạn trơ vùng nối AV. Nếu nó cho phép, một xung nhĩ thỉnh thoảng có thể lẻn qua ngã ba AV và tóm được tâm thất. đây gọi là
nhịp bắt giữ ―capture beat‖. Capture beat thường QRS hẹp. Vì vậy, trong một nhịp nhanh QRS rộng nếu chúng ta lưu ý có một QRS hẹp hoặc tương đối hẹp có thể đây chính là VT. Nếu xung nhĩ sau khi vượt qua ngã ba AV va chạm với các xung từ thất sẽ cho ra fusion beat (nhịp kết hợp). capture beat không trọn vẹn chính là fusion beat. Nó là sự kết hợp của hai QRS một kích hoạt từ bên trên, một từ bên dưới (song kiếm hợp bích).cho nên độ rộng QRS có thể rộng, hẹp hoặc trung gian
Vì vậy, các bằng chứng AV phân ly trong ECG rất hiếm khi thể hiện nếu VT thành công đi qua ngã ba AV và chiếm cứ nút xoang.
57. C reactive protein: bình cũ rượu cũ!
Những gì chúng ta biết về CRP. . .
Đó là một chất phản ứng trong giai đoạn cấp tính. Tiết ra chủ yếu ở gan.
là một dấu hiệu cho viêm nhiễm. Hs CRP hơn 1 – 3 mg là đáng để kể
Những gì chúng ta nghĩ rằng, chúng ta đã biết. . .
Đó là một dấu hiệu trực tiếp liên quan tăng nguy cơ của bệnh mạch vành. Giảm nồng độ CRP giảm nguy cơ CAD và ngược lại.
Những gì chúng ta chắc chắn không biết. . .
CRP làm hỏng nội mạc mạch vành? Hoặc là nó tiết ra từ các mảng bám bị viêm? Làm thế nào statin làm giảm CRP?
Làm thế nào bạn có thể phân biệt nguồn gốc tim hay ngoại biên của CRP ? nồng độ fibrinogen có xu hướng tăng trong trường hợp CRP không cao?
Hs CRP đã được đề xuất như là một xét nghiệm để phát hiện CAD có nguy cơ cao, các công ty dược đều quảng cáo như vậy. Đối với các công ty dược, phát triển một loại thuốc liên quan tới chỉ số sinh hóa dễ dàng hơn nhiều, vì nó không liên quan đến an toàn bệnh nhân hoặc các vấn đề đạo đức.
Vì vậy, một trong những nghiên cứu lớn về statin, vai trò Hs CRP xác định nguy cơ cao ở những người có mức LDL bình thường. Nghiên cứu này khiến nhiều chuyên gia cảm thấy
chúng ta nên cẩn thận và có nhận thức của động cơ của nhiều nghiên cứu mang danh cuộc chiến toàn cầu chống lại CAD.
Những gì chúng ta biết được?
C reactive protein có thể coi là ESR (tốc độ máu lắng) thế hệ mới!
Nó có thể không có bất kỳ giá trị cụ thể nào về dự đoán nguy cơ tim mạch
Vai trò của nó chỉ được xác định trong tập hợp con, tức là chỉ ở những người có nguy cơ cao tiến triển CAD
Nhưng phần lớn các bác sĩ bây giờ quá cường điệu, lắm khi gọi là bước ngoặt phân tử để ngăn ngừa sớm CAD- thật khó chấp nhận được
nghiên cứu phân tích trên CRP trong Lancet 2010 đã được công bố. Tôi sợ, nó đã không trả lời câu hỏi khó nắm bắt: giá trị tiện ích của Hs CRP trong lâm sàng tim mạch và phòng ngừa biến chứng tim mạch là gì?
Những gì chúng ta cần biết là,
Tránh ăn vặt,hoạt động thể chất tốt, Bỏ hút thuốc lá, tâm lí thoải mái là cách tốt nhất để ngăn chặn dịch bệnh CAD!
còn phân tử Hs CRP tôi khuyên các bạn đừng ảo tưởng và nên lờ nó đi cho bệnh nhân đỡ khổ.
58. ST CHÊNH Ở AVR CÓ GỢI Ý TẮC NHÁNH ĐỘNG MẠCH VÀNH CHÍNH TRÁI LMCA
Đang có cuộc tranh luận nóng trong group về vấn đề dùng tiêu huyết khối cho bệnh nhân đau thắt ngực nặng có ST chênh lên ở AVR và ST chênh xuống ở V2-V5. Liệu đây có phải có dấu hiệu tắc động mạch nhánh chính trái ở bệnh nhân đau thắt ngực không ổn định!
Tôi đã cố gắng 1 cách hợp lý để phân biệt tăc đm chính trái ở NSTEMI // UA và STEMI
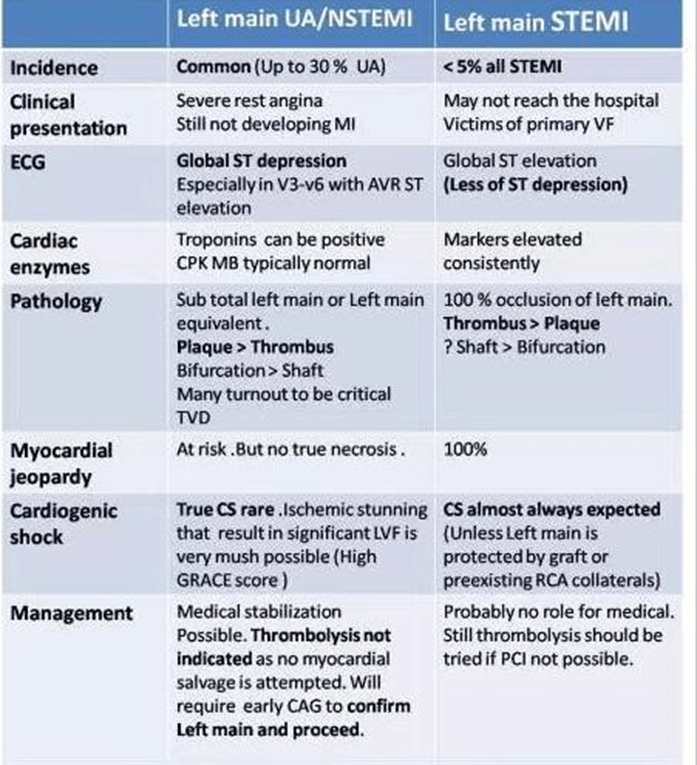
ST chênh lên chỉ ở AVR không đủ tiêu chuẩn để chỉ định tiêu huyết khối.khi dùng tiêu huyết khối cần có huyết khối lớn và tắc hoàn toàn . ST chênh lên chỉ ở AVR không phải là tiêu chuẩn để nghi ngờ tắc động mạch chính trái
59. CÓ NÊN MÀY MÒ TỈ MỈ KHI GẶP QRS RỘNG + NHỊP NHANH?
QRS rộng kèm nhịp nhanh- bản thân nó là 1 cái gì đó gợi trí tưởng tượng và quyến rũ biết bao nhà tim mạch học. Hơn 3 thập kỷ nghiên cứu, tranh luận lâm sàng, các hội nghị, hội thảo vẫn chưa thể giải mã được những bất ổn trong giải mã nhịp nhanh kèm QRS rộng (Cụ thể, VT vs SVT)
Câu hỏi lớn đặt ra là phân biệt QRS rộng + nhịp tim nhanh từ QRS hẹp + nhịp nhanh Điều này xảy ra thường xuyên khi chúng ta nhận ra mình đang xác định nhịp nhanh có QRS rộng 1 cách mơ hồ
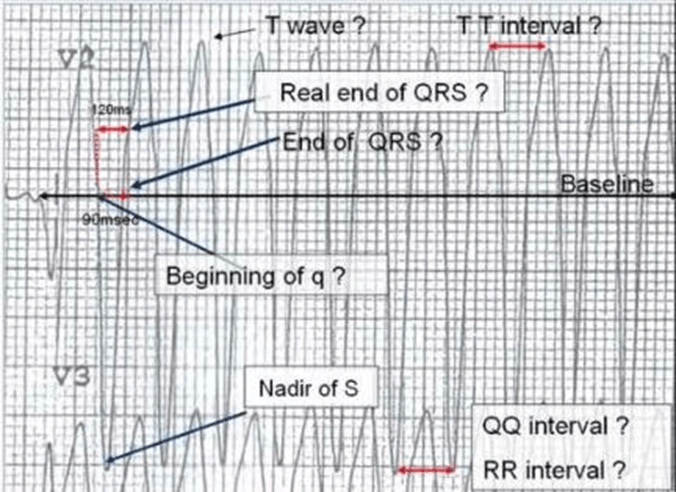
QRS bình thường có thể từ 80 -100ms? QRS hẹp nhịp nhanh 80 ms?
QRS rộng nhịp nhanh > 120ms? QRS chắc chắn rộng> 140msec
* Sự nhầm lẫn chủ yếu vì 20ms khác biệt giữa chuyển đạo chi và chuyển đạo ngực Trong thực tế người ta có thể không phân biệt được nhịp nhanh QRS rộng hay hẹp Có khu vực chồng chéo lớn có lẽ phải để cái tên nhịp nhanh QRS rộng vừa
Nếu chúng ta phân loại thành 3 loại thay vì 2 như hiện tại có thể giúp chúng ta chẩn đoán nhanh và chính xác
Nhịp nhanh QRS hẹp (QRS 80ms)
xoang
Tất cả svtS (avnrt …)
Nhịp nhanh QRS trung bình 90-120ms
Hầu hết các SVT bất thường (Trừ SVTs dẫn truyền lệch hướng thực sự rộng!) VTs vách *
VTs bó *
VT ở bệnh nhân dùng máy tạo nhịp
* Bất kỳ VT nào phát sinh gần hệ dẫn truyền chính của tâm thất gây nhịp nhanh đều có QRS tương đối hẹp.
nhịp nhanh QRS rộng > 120ms
Hầu hết các VT chuẩn (thiếu máu cục bộ, nguồn gốc cơ tim) VTs sau nmct
SVT bất thường đặc biệt là AVRT SVT bất kỳ kèm BBB trước đó rối loạn điện giải
Làm thế nào để đo được độ rộng của QRS?
Chúng ta lấy QRS hẹp hay QRS rộng nhất hay lấy trung bình?
Chúng ta có nên tính xem QRS rộng thêm bao nhiêu sao với QRS nền của bệnh nhân? Vì nếu không QRS rộng với người này lại là bình thường so với người khác Nếu không có đường đẳng điện và đoạn ST lẫn với QRS thì làm sao để xác định vị trí kết thúc của QRS?
Nếu chuyển đạo chi QRS hẹp còn chuyển đạo ngực QRS rộng có ý nghĩa gì? Nếu chuyển đạo trước tim chỉ 1 chuyển đạo có QRS hẹp thì có ý nghĩa gì?
QRS hẹp trong VT có thể rộng khi kèm bất thường gì?
thông điệp cuối cùng
Chúng ta có nên đề xuất phân QRS trong nhịp nhanh thành 3 loại không? 😀
60. YẾU TỐ NÀO BẢO VỆ BỆNH ĐỘNG MẠCH VÀNH CHÍNH TRÁI?
Bệnh động mạch vành nhánh chính bên trái là 1 phân quan trọng của CAD, và nó được sự quan tâm đặc biệt của các nhà can thiệp. Xưa đến giờ vẫn thế, bác sĩ tim mạch rất sợ khi chạm vào tổn thương này, vì họ nghĩ rằng bất ngờ tắc nhánh này sẽ đe dọa tính mạng thậm chí tử vong. Sau khi tiến hành can thiệp chúng tôi mới nhận ra, PCI trong LAD cũng thường thôi, hiện tại chúng ta có công nghệ và chuyên môn để can thiệp PCI thành công cho bất kỳ vị trí nào tắc của LM. Tiếc thay LMD lại trở thành dấu hiệu tôn vinh khi tiến hành PCI.
Các thuật ngữ bảo vệ và không bảo vệ LMD thịnh hành trong nhiều năm. Tiếc là nó không chuyển tải một ý nghĩa thống nhất. tôi sẽ chia sẻ quan điểm của tôi về các sắc thái của LMD được bảo vệ và không được bảo vệ.
Thời gian bảo vệ không đặt ra bởi các nhà sinh lý học tim mạch mà do các nhà can thiệp tim mạch. Do đó nó bao hàm ý nghĩa giải phẫu hơn là sinh lý. Bảo vệ LMD có nghĩa là phải có ít nhất một nhánh nhỏ LAD hoặc nhánh mũ còn chức năng. Khi có yếu tố này sẽ làm tăng mức độ thoải mái của nhà can thiệp.
Bệnh động mạch vành nhánh chính trái được phân loại:
Các tổn thương hay gặp của nhánh chính trái:
Không có triệu chứng, không hạn chế dòng chảy, tổn thương không đáng kể (<50%) Gần miệng nối
Trục: giữa, xa hoặc gần trái chính chổ chia hai
Nhánh chính trái không được bảo vệ
Tất cả các tổn thương trên
Bắc cầu CABG không hiệu quả (ví dụ: LIMA tắc làm LAD không được bảo vệ)
Nhánh chính trái được bảo vệ
CABG với ít nhất một trong những nhánh nhỏ LAD / LCX còn chức năng
Tắc toàn bộ nhánh chính LAD những những nhánh LAD vẫn thông tốt từ RCA / LCX
61. Chúng ta có thể dùng Nitro-glycerine ở một bệnh nhân tụt huyết áp kèm phù phổi cấp tính?
Một người đàn ông tiền sử CAD được chẩn đoán thiếu máu cục bộ LVF và hạ huyết áp . huyết áp 90/60 mmHg và nhịp tim 140. lượng nước tiểu trong giờ qua trước mắt là 50 ml. sp02 95% .rales ẩm khắp 2 trường phổi.
Siêu âm tim thấy rối loạn chức năng LV vừa phải, có giảm vận động thành khu vực LCX, chẩn đoán thiếu máu cục bộ thất trái sau nmct.
Tôi đã đề nghị đồng nghiệp dùng NTG IV cho bệnh nhân rồi ra khỏi phòng. Sau vài giờ tôi đến khám lại, bệnh nhân tình trạng ngày càng xấu đi. Tôi tò mò hỏi sao đồng nghiệp của tôi lại không dùng theo hướng dẫn của tôi. Cậu ta nói cậu không hiểu nguyên tắc dùng NTG ở bệnh nhân bị sốc.
Hãy đọc giải thích bên dưới
Nguyên nhân hạ huyết áp trong thiếu máu cục bộ LVF là gì?
Phổi bị ngập lut do LVEDP (áp lực đổ đầy động mạch vành) rất cao. Máu không chỉ khó vào mà còn khó ra khỏi thất trái do mất thời gian nghỉ vì giảm chức năng bơm.
Tiền tải rất cao thực sự gây choáng tâm thất trái trong kỳ tâm trương. đây là một nghịch lý về huyết động học. Thừa tiền tải nhưng rất ít lượng máu đi qua LV.
Chúng tôi có một số cách làm giảm mức độ rất cao của LVEDP. IV NTG có thể làm giảm đáng kể tiền tải (và giảm LVEDP.) Lợi ích lớn khác là, NTG có thể làm giảm MVO2 bằng cách cải thiện tưới máu mạch vành màng trong tim và giảm áp lực trong tim. Khi LVEDP được hạ xuống, tâm thất sẽ có xu hướng phục hồi và đạt được ít nhất là hệ số đàn hồi ban đầu (định luật frank). Tất nhiên nó sẽ giảm do thiếu máu cục bộ. Thậm chí giảm nhẹ LVEDP (18-25 mmHg có thể có những lợi ích đáng kể
Đây là một tình huống mà NTG có thể làm tăng huyết áp khi huyết động được thay đổi thuận lợi
*Vì vậy để có tác dụng cần dùng liều cao furosemide, nhưng còn phụ thuộc vào tướ máu thận
Các tác dụng có lợi khác của NTG
trào ngược van hai lá là 1 biểu hiên nghiêm trọng của rối loạn chức năng LV.NTG có thể làm giảm phần trào ngược van 2 lá cấp tính rất hiệu quả
Chú ý
NTG có thể làm nặng thêm tình trạng hạ huyết áp của nhồi máu thất phải.
Những gì đã xảy ra với bệnh nhân này?
Ông đã cải thiện triệu chứng khi dùng IV NTG. Bn có dùng Dobutamine đồng thời , huyết áp không tụt hơn và giảm phù phổi. bn phục hồi hoàn toàn sau 48h
Thông điệp cuối cùng
Chúng ta có xu hướng lo lắng nhiều hơn về việc tụt huyết áp khi dùng NTG. . Nó là một loại thuốc tuyệt vời hiệu quả đặc biệt trong bối cảnh thiếu máu và suy tim ngay cả khi huyết áp thấp!
Tụt huyết áp kèm phù phổi cấp hay gặp trong thiếu máu cục bộ thất trái có thể điều trị cực tốt bởi NTG. Tất nhiên các bác sĩ cần can đảm khi dùng NTG ở bệnh nhân có huyết áp tâm thu 80-90mmhg.
Lý tưởng khi theo dõi huyết động xâm lấn và dùng thuốc tăng co bóp đồng thời (Doubtamine / Nor-epinephrine) trong trường hợp áp lực tưới máu xấu đi
62. VÍ SAO NHĨ THẤT PHÂN LY TRÊN ECG PHẦN LỚN ÍT GẶP Ở BỆNH NHÂN NHỊP NHANH THẤT
Khi thất bắt đầu đập không phụ thuộc nhĩ với tần số tầm 200l/p mỗi nhát bóp sẽ cố để truyền ngược lên bội nối AV . cùng lúc đó xung từ xoang vẫn làm công việc thường ngày của nó ở khoảng 70/p phát xung xuống thất, nhưng đối mặt với dẫn truyền không bình thường trên đường xuống của nó bởi các xung bệnh lý từ thất. Điều gì sẽ xảy ra khi cả 2 sóng này gặp nhau. Thất hầu như thành công trong cuộc đua này và hầu hết các xung từ thất dãn ngược lên bộ nối AV và kết hợp với xung nhĩ. Khi điều này xảy ra, phân ly AV được cho là xảy ra. Điểm quan trọng ở đây là , nhiều lần dẫn truyền VA nhanh và tối ưu,nó có thể qua nút AV dễ dàng và tìm dến nhĩ, kết quả khử cực nhĩ và reset lại nhĩ. Nếu VT trường diễn dẫn ngược có thể kiểm soát nhĩ cho đến khi hết cơn VT. nó làm sóng P dường như biến mất hoàn toàn.(chú ý: Nếu bạn nói VT như là một trong các nguyên nhân của sự biến mất sóng P bạn có thể rớt trong kỳ thi tim mạch, nhưng sự thật nó là như thế
63. Mối quan hệ tinh tế giữa D-dimer và bóc tách động mạch chủ!
Vai trò của d dimer trong hội chứng động mạch chủ cấp tính
D -Dimer là sản phẩm của thoái hóa fibrinogen và hủy fibrin nội mạch. Mức hơn 500ng / ml có tính chất gợi ý. trong bóc tách động mạch chủ nồng độ D-Dimer có thể hơn 2000ng / ml.
Nồng độ D-Dimer tăng lên trong 3 trường hợp đau ngực cấp tính
nhồi máu cơ tim cấp tính thuyên tắc phổi
Và bóc tách động mạch chủ.
Nhưng vấn đề không đơn giản như vậy vì bất kỳ quá trình đông máu nội mạch và ly giải, CAD mạn và tổn thương huyết khối trong động mạch vành đều có thể làm tăng d dimer.
Tương tự, huyết khối tĩnh mạch sâu cũng làm tăng D dimer
Vì vậy, tăng D dimer có ích gì trong chẩn đoán bóc tách động mạch chủ?
D Dimer không chỉ giúp chẩn đoán bóc tách động mạch chủ mà còn giúp chúng ta có nên chỉ định phẫu thuật. mức D-Dimer <500 có giá trị tiên lượng âm tính 98%.
Cơ chế sinh học của D dimer trong bóc tách là gì?
D dimer trong bóc tách động mạch chủ chủ yếu tiết ra trong lòng giả ống. Vậy nên khi dòng máu tiếp xúc với khu vực này lớn sẽ kéo theo sự tiếp xúc của các cục máu đông với dòng máu tươi gây đông máu nội mạch rải rác.
Vì vậy, mặc dù các báo cáo ddimer có gần 100% giá trị tiên đoán âm tính. . . nhưng có khi nào có chỉ định phẫu thuật với mức D dimer bình thường?
Có, đã có rất nhiều báo cáo về vấn đề này
Một bóc tách mà không có huyết khối (hiếm… Nhưng vẫn còn có thể!)
Một cục máu đông chỉ giới hạn trong lòng giả ống mà không đi vào tuần hoàn. Phình mạch trong thành
Có thời gian cửa sổ ? Dimer chủ yếu có giá trị với bệnh nhân đến trước 24h kể từ khi khởi phát đau ngực.
Phải mất bao lâu để dimer được bài tiết?
Bóc tách đm vành trong STEMI có làm tăng dimer?
D dimer chủ yếu có tác dụng loại trừ chẩn đoán bóc tách động mạch chủ.
Nếu nồng độ dimer tăng cao và lâm sàng bệnh nhân không có bằng chứng thuyên tắc phổi cấp hoặc nmct cấp tính, đau ngực nghi bóc tách động mạch chủ và cần làm thêm các thăm dò thêm TEE, MRI, MDCT vv
** Không bao giờ cần những thăm dò quá đắt tiền cho đến khi thấy d dimer tăng Mặc dù rất nhạy nhưng không bao giờ nó được sử dụng để chẩn đoán bóc tách động mạch chủ.
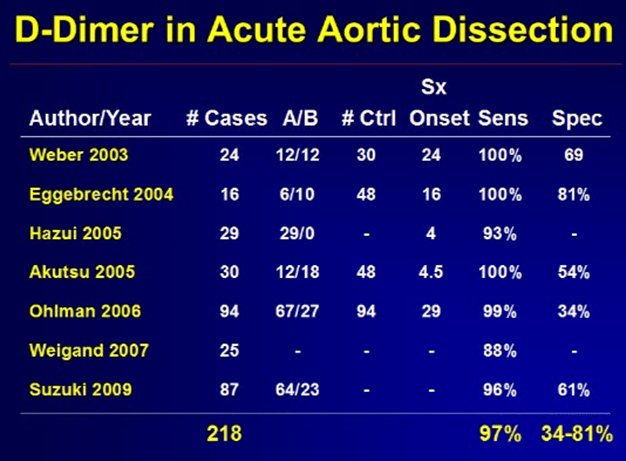
64. Làm thế nào bạn phân biệt block AV Mobitz 1 với block AV Mobitz 2 nếu dẫn truyền 2:1
Block AV wenkebach 1 có kéo dài PR sau đó có sóng P ―Dropped‖ và QRS hẹp. tỷ lệ dẫn truyền trong block AV wenkebach là 3: 2 hay 4: 3.
Block AV mobitz 1 thường phục hồi tự nhiên, không cần máy tạo nhịp hỗ trợ.chỉ có vấn đề tại nut và kể nhĩ thất còn hệ thống dẫn truyền Purkinje còn nguyên vẹn và tiên lượng tốt. Trong block AV 2 mobitz 2 thường tổn thương dưới bó his .Đây là loại block không ổn định và nguy cơ cao block av cấp 3 nên thường phải đặt máy tạo nhịp tim.
Vì vậy, cần phải phân biệt 2 dạng này
Thường thì dễ nhận ra trong hầu hết các tình huống, nhưng khi tỷ lệ dãn truyền là 2: 1 thì sẽ khó khăn để phân biệt.
Dẫn truyền 2:1 hiếm nhưng vẫn có trong các báo cáo
điểm để phân biệt hai loại này là gì?
QRS rộng: QRS bình thường thường là wenkebach . QRS rộng cho thấy block dưới bó his. Khoảng PR bình thường trong mobitz 2. Trong wenkebach khoảng PR thường kéo dài. (du không phải luôn luôn)
Đáp ứng với atropine *: Wenkebach có xu hướng tăng tốc trong khi mobitz 2 có xu hướng giảm.
Đáp ứng với gắng sức: tỷ lệ dẫn truyền Wenkebach cải thiện, mobitz 2 thì không
Đáp ứng với xoa xoang cảnh: Wenkebach nặng hơn, mobitz 2 cải thiện
* những phản ứng khác nhau là do thực tế rằng nút AV do ảnh hưởng của các sợi vagal hơn là hệ thống Purkinje.
** Cần lưu ý tác dụng atropine trên dẫn truyền qua AV .Atropine cải thiện dẫn truyền qua AV, trong khi hiệu quả của nó trên nút xoang làm tăng tần số nhịp tim
65. Sự khác biệt giữa sóng P đẳng điện và mất sóng p là gì?
Sóng P đặc trưng cho quá trình khử cực nhĩ. Chiều cao và chiều rộng của sóng P không chỉ phụ thuộc kích thước của RA và LA mà cũng là đặc trưng cho nguồn gốc phát nhịp từ tâm nhĩ . nút xoang bình thường sẽ tạo ra sóng p bình thường
Chúng ta biết sóng p lạc vị có thể có sự khác biệt lớn về hình thái học bình thường (nhiều hình thái)
Sóng P đẳng điện là gì
Giống như QRS điện áp thấp, sóng p cũng có thể có biên độ rất thấp và hoàn toàn đẳng điện, thâm chí có thể mất sóng p ở 1 vài hoặc tất cả chuyển đạo. tâm nhĩ được kích hoạt nhưng không ghi được sóng p gọi là sóng p đăng điện
Tầm quan trọng của sóng p đẳng điện
Nó có thể xảy ra, cả ở nhịp xoang và nhịp nhĩ lạc vị. mất sóng p cần phân biệt với sóng p dạng đẳng điện. Nó thường được mô tả trong nhịp nhĩ xuất phát từ phía bên phải của vách liên nhĩ gây nhịp nhĩ nhanh bất thường. nhịp xuất phát từ vị trí này sẽ làm xuất hiện sóng p đẳng điện ở hầu hết chuyển đạo, đặc biệt là V1
Các nguyên nhân khác làm mất sóng p
Rung nhĩ
Thực tế ở đây sóng p được thay thế bởi các sóng f ngừng xoang với nhịp bộ nối và dẫn truyền VA ngược không phải tất cả nhịp bộ nối đều mất sóng p
Mất sóng p gặp trong tăng kali / suy thận là do nồng độ cao của kali ức chế hoạt động nhĩ gây liệt điện nhĩ nhưng xung từ nút xoang vẫn qua nhĩ xuống thất.
66. Các yếu tố quyết định độ rộng QRS trong nhịp nhanh thất là gì?
Chúng ta biết VT là nhịp nhanh QRS rộng. 1 số ít người biết VT có thể có QRS bình thường hoặc hẹp. nhưng đa số ít ai biết vì sao VT lại có QRS từ rộng – bình thường – hẹp do cái gì?
Các yếu tố xác định QRS rộng ở VT.
Nguồn gốc của VT: vách ngăn, vách tự do, đỉnh vv Xuất phát từ thượng tâm vị làm cho nó rộng hơn Tần số phụ thuộc dẫn truyền trong tâm thất
Thuốc (liều tích lũy của amiodarone làm VT có QRS rộng) rối loạn chức năng LV liên quan / Bệnh cơ
Điện giải (K + vv)
Block bó nhánh trước đó (Đáng ngạc nhiên là một số BBB có thể chuyển VT từ QRS rộng sang QRS hẹp)
Giải thích hợp lý nhất cho VT có QRS hẹp là nó có nguồn gốc gần vách ngăn và đi xuống sinh lý vào vùng Purkinje và gây khử cực.
67. Tại sao can thiệp mạch vành kịp thời giảm đau thắt ngực nhưng hiếm khi làm giảm khó thở?
PCI giúp cứu nhiều bệnh nhân đau thắt ngực không đáp ứng với điều trị nội khoa.
Trong khi giảm đau thắt ngực là chắc chắn thì khó thở lại không! . Nếu chúng ta tin, giúp thông mạch vành ở bệnh nhân rối loạn chức năng LV sẽ khôi phục lại chức năng LV, thì hiển nhiên đây là điều sai lầm!
Tại sao nó như vậy ?
giảm đau thắt ngực đòi hỏi phục hồi cung cấp oxy và cải thiện thiếu máu cục bộ khu vực. Điều này xảy ra mà không có bất kỳ vấn đề gì khi máu thấm vào tế bào thiếu máu cục bộ và làm dịu các dây thần kinh thiếu máu cục bộ kích hoạt các tín hiệu đau. Trong khi đó, khi chức năng LV cải thiện, lưu lượng máu đã giúp tăng hoạt động của myocyte actin / myosin. Đối với điều này, cần phải có cơ chế co bóp tế bào cònnguyên vẹn. Cấu trúc tế bào cơ phải phù hợp tâm thất .
Và bây giờ, chúng tôi nhận thấy khó thở cực kỳ phụ thuộc vào chức năng tâm trương, hay gặp trong thiếu máu cục. rất ít bằng chứng cho thấy PCI / CABG giải quyết được rối loạn chức năng tâm trương!
68. Case nhồi máu cơ tim thành dưới cũ?
Bn nữ 49 tuổi được 2 bs lâm sàng và 1 bs tim mạch chẩn đoán nmct thành dưới cũ
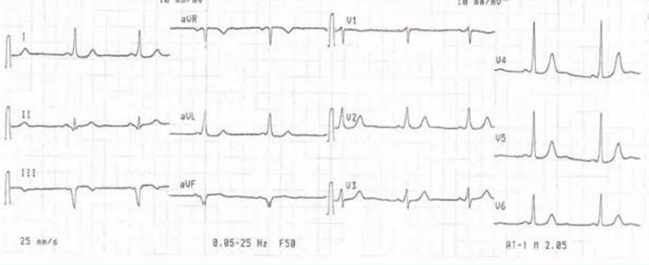
Nên coi chừng với sóng Q không nhồi máu.
Liêu đây có phải là sóng Q của nmct cũ thành dưới không>
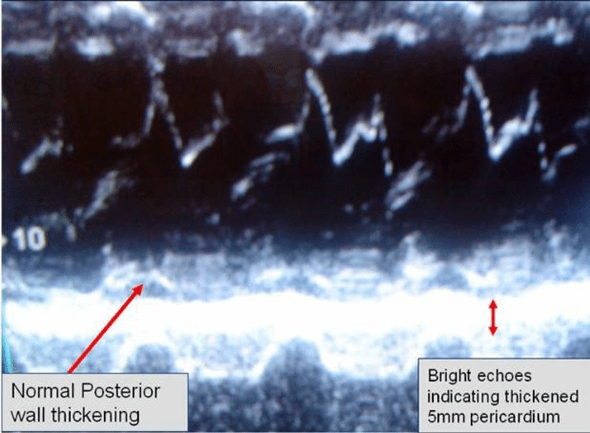
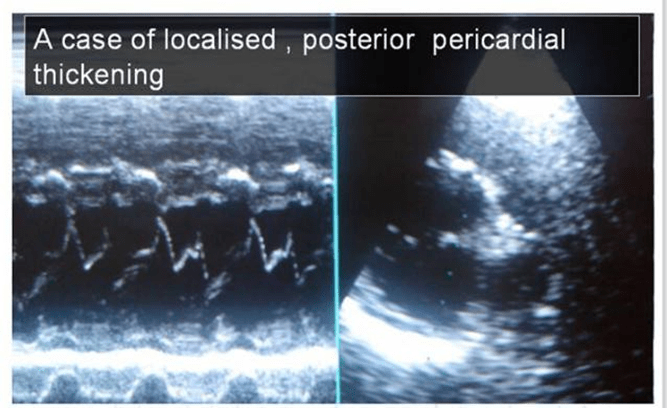
Bạn có tin?
Phụ nữ này có chức năng tâm thu LV bình thường và chức năng tâm trương không có bằng chứng co thắt.
Có dày màng ngoài tim do viêm màng ngoài tim mãn tính .Đây loại dày khu trú ở thành sau thường gặp nhất sau tràn dịch. lao màng ngoài tim rất có khả năng là nguyên nhân gây ra. Sóng Q không phải là sóng đặc hiệu để chẩn đoán nmct. Nó chỉ cho biết hướng dẫn truyền hiện tại có tình trạng ―trơ‖ không cho dẫn truyền.
Các bệnh lý có thể tạo ra sóng Q mà không do nhồi máu?
Xơ nang cơ tim (DCM-Bệnh cơ tim) Sẹo cơ tim
LVH, HCM
Khí, dịch trong màng tim / khoang màng phổi dày màng ngoài tim (Như ở bệnh nhân này) dẫn truyền đường phụ ngắn (WPW syndrome)
Hiếm khi chỉ thiếu máu cơ tim đơn thuần không có hoạit tử lại tạo ra được sóng q
Chốt lại đây là 1 case dày màng ngoài tim gây ra sóng q bệnh lý, bắt chước hình dạng MI

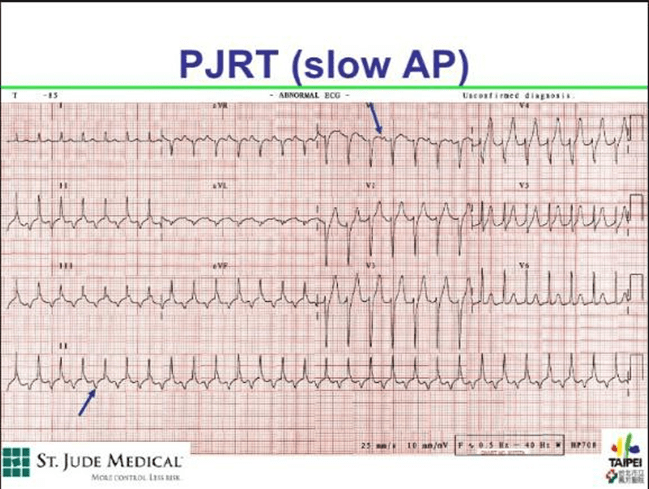
69. Nhịp nhanh bộ nối có ý nghĩa như nào?
Ban đầu, nhịp tim nhanh bất thường được đặt tên theo nguồn gốc của chúng. Sau đó chúng được phân loại thành: nhịp nhanh có QRS hẹp và rộng nhấn mạnh một thực tế rằng, cả SVT & VT có thể là hẹp hoặc rộng !
Người ta thấy hay có nhầm lẫn trong việc phân loại nhịp nhanh QRS hẹp hơn là QRS rộng
Nhịp nhanh bộ nối là gì?
là điểm giải phẫu đặc biệt gọi là nút nhĩ thất AV?
là khu vực lan tỏa trong vùng lân cận của nút nhĩ thất? Là phần đầu của bó his?
Hoặc là nó được hình thành bởi toàn bộ rãnh AV do các fibroskeleton tạo thành một hàng rào điện giữa tâm nhĩ và tâm thất?
Câu trả lời thực tế là chưa rõ
Theo điện sinh lý, bộ nối AV đề cập đến vị trí kết nối dây dẫn đi xuống từ tâm nhĩ và nối với sợi purkinje của tâm thất
nút AV có giải phẫu cấu trúc khác biệt?
không có cấu trúc như vậy, nó là 1 tập hợp các tế bào dẫn truyền khác nhau. Thuật ngữ‖ nút AV‖ nên phế bỏ bởi cộng đồng tim mạch với lý do đơn giản là không hề có cấu trúc thực thể đó
Trong thực tế các tế bào bộ nối AV bây giờ gọi là các tế bào nhĩ ―tinh khiết‖, các tế bào vùng bộ nối, tế bào chuyển tiếp.
chức năng bộ nối AV là gì?
Người ta nhận thấy vị trí ngã ba bộ nối AV làm công việc độc đáo quan trọng tới sự sống còn của con người! Mặc dù nút xoang là máy tạo nhịp tim, ngã ba AV có tác dụng thúc đẩy và trì hoãn khoảng 200 mili giây sau đó mới cho dẫn truyền xuống các tâm thất.
Sự trì hoãn này rất quan trọng với máu trở lại tĩnh mạch khi máu từ tâm nhĩ xuống tâm thất, tâm thất đang được đổ đầy và cung lượng tim giảm.
Số lượng các ion ở ngã ba AV được chi phối kiểm soát bởi các sợi phế vị trong khi tâm thất chi phối nhiều hơn bởi các sợi giao cảm.
Trước đây sinh lý của AVRNT phân tách theo chiều dọc của bộ nối AV. Sắp xếp các tế bào dẫn truyền nhanh và tế bào dẫn truyền chậm phù hợp với vòng vào lại.thành sau tâm nhĩ chủ yếu con đường chậm. phía trước gần bó his là con đường nhanh.
Thi thoảng một số các cụm tế bào bộ nối AV nằm rải rác xung quanh khu vực phía trên vách ngăn làm dẫn truyền chậm xuống thất. các tế bào này có thể gây vòng vào lại hoặc VT fascicular.
Sự chồng chéo của các tế bào này ở bộ nối giải thích sự nhạy cảm verapamil của một số trường hợp VT phát sinh ở vùng lân cận.
Nhịp nhanh bất thường ở bộ nối hoặc vòng vào lại hoặc lạc vị được gọi là JT
AVNRT không bao giờ được gọi là JT mặc dù thực tế rằng, nó được khởi xướng bởi một vòng vào lại bệnh lý ngay giữa khu vực bộ nối AV.
Vì vậy, hiện nay chúng tôi chỉ phân ra vài loại JT. Nhịp nhanh bộ nối không thành cơn (NPJT)
Nhịp nhanh bộ nối dai dẳng (Incessant JT) Nhịp nhanh lặp lại bộ nối kéo dài (PJRT) Nhịp bộ nối tăng tốc
NPJT
Điều này xảy ra trong các tình huống sau đây ngộ độc digoxin (cổ điển)
sau phẫu thuật tim
Đôi khi trong MIR cấp
Có thể gặp trong đốt EP LAB bộ nối
NPJT là nhịp tim nhanh tự động . xuất phát từ mô vùng bộ nối AV. thuật ngữ lý tưởng nên dùng là nhịp nhanh ổ bộ nối (FJT) .tần số 70 -140. Nhịp bộ nối tăng tốc là dạng lành tính của JT, không cần sốc điện
Nhịp nhanh bộ nối dai dẳng
Điều này đã được mô tả đầu tiên ở trẻ nhỏ .có thể do bẩm sinh. Hiện nay cũng gặp ở người lớn, tần sốc 150 -300, hay kèm AV phân ly. Có thể bắt chước rung nhĩ không điển hình hoặc nhịp nhanh nhĩ. High nguy cơ cao ở những bệnh nhân mạch nhanh có bệnh cơ tim. Có thể liên quan amiodaron.Surprisingly, verapamil có thể làm tình trạng nặng lên
.có sự chồng chéo giữa NPJT và nhịp bộ nối dai dẳng, sốc điện không hiệu quả và có thể nặng lên. RF ablatioon đốt ít khi hiệu quả
nhịp bộ nối nhanh bất thường là 1 nhóm duy nhất của nhịp nhanh bất thường QRS hẹp với nhiều cơ chế khác nhau. Chúng được chẩn đoán trong từng trường hợp cụ thể. Chúng thường khó điều trị, là cơ chế lạc vị tự nhiên (Trừ PJRT) . nhịp bộ nối tăng tốc là dạng lành tính của JT. AVNRT cần không bị nhầm lẫn với JT, mặc dù nó có thể coi như là nhịp tim nhanh bộ nối có vòng vào lại
70. Thời gian cửa sổ tiêu huyết khối 12h
Nhưng có thể có cơn đau thắt ngực trước khi nhồi máu hoặc ở bệnh nhân tai biến, nghiện rượu không xác định được thời gian cửa sổ.
Vậy nên nhìn trên ECG: st chênh lên, T âm và sóng Q. Nếu T âm chứng tỏ đã hết thời gian dùng tiêu huyết khối
71. Tại sao chúng ta hiếm khi chẩn đoán nhịp bộ nối lạc vị?
Nhịp lạc vị hay nhịp khử cực sớm là 1 trong những bất thường các bác sĩ hay chẩn đoán trên ECG
Nhịp nhĩ sớm (APDs) nhịp thất sớm (VPDs)
APDs và VPDs hình thành phần lớn tất cả các nhịp lạc vị trên lâm sàng.
Tại sao chỉ có tâm nhĩ và tâm thất tạo nhịp lạc vị còn nút nhĩ thất, bó his và sợi Purkinje hiếm khi sinh ra nhịp lạc vị?
Có phải ngã ba AV tương đối miễn dịch với nhịp lạc chỗ bộ nối JPDs?
Câu trả lời cho câu hỏi này sẽ là “Có thể có”. Tuy nhiên, chúng ta cần phải nhận ra rằng có thể nó không hiếm như chúng ta nghĩ vì có khi chúng ta không nhận ra nó!
Một số nghiên cứu về khử cực bộ nối sớm được thực hiện . ngã ba AV có tính chất độc đáo hơn so với bất kỳ bộ phận khác của tim. Bộ nối AV (nút AV không phải là một từ ưa thích vì giải phẫu không có thực thể này) có tác dụng điều hòa giúp đổ đầy thất phải hoàn toàn. Chúng ta gọi nó là khoảng PR
Vì vậy, khi mục đích cơ bản của bộ nối AV là làm chậm dẫn truyền thì nó sẽ không dễ nhận kích thích một cách dễ dàng nên JPDs hiếm khi xảy ra hơn so với lạc vị nhĩ hay thất
JPDs ít gặp trong khi nhịp thoát bộ nối thể hiện nhịp chậm trên thất nặng. nó xảy ra như nào?
Tế bào bộ nối AV độc đáo ở chỗ nó sẽ cứu tim bất cứ khi nào nút xoang phát nhịp chậm lại. Điều này xảy ra như một phản ứng thụ động Chúng tôi gọi đây là nhịp thoát bộ nối. khác biệt lớn giữa một nhịp JPD và nhịp thoát bộ nối (JEP hoặc JED) là thời gian ban đầu xuấ hiện nhịp. nhịp thoát bộ nối thường đến muộn .nhịp thoát bộ nối thường sẽ đến muốn hơn so với chu kỳ xoang trước. còn nhịp bộ nối lạc vị bao giờ cũng đến sớm hơn so với nhịp dự kiến tiếp theo
Sự khác biệt khác là nhịp thoát bộ nối giúp cứu lại và phục hồi nhịp xoang, thường bằng tần số ngã ba AV 40-50
72. Viêm màng ngoài tim có thể giống như STEMI!
Nguyên nhân hay gặp nhất của ST chênh lên là STEMI.
Các nguyên nhân không nhồi máu có ST chênh lên bao gồm:
viêm màng ngoài của tim hội chứng tái khử cực sớm Tăng kali máu
Hội chứng Brugada
Tổn thương hệ thần kinh trung ương
cơ chế của ST chênh lên trong viêm màng ngoài tim là gì?
Trong viêm màng ngoài tim, chúng tôi không chắc chắn về sự có mặt của tổn thương ở các tế bào màng ngoài tim vì chúng không có khả năng khử cực và tái khử cực .Nhưng, thực tế là thượng tâm mạc và lớp lá tạng màng ngoài tim có giải phẫu gần như nhau.
Làm thế nào để viêm thượng tâm mạc làm ST chênh lên?
Đặc điểm st chênh lên lan tỏa các chuyển đạo và chênh lõm đặc trưng cho viêm màng ngoài tim. Điều này làm chúng tôi tin viêm màng ngoài tim là quá trình lan tỏa và liên quan đến toàn bộ chu vi của quả tim
Độ chênh lên của ST phụ thuộc vào sự lây lan của quá trình viêm dưới thượng tâm mạc. nếu viêm hoạt động mạnh sẽ làm st chênh rõ
ECG của cậu bé 15 tuổi vào viện vì sốt có viêm cơ tim- màng ngoài tim nặng. siêu âm thấy rối loạn chức năng thất trái nặng. cậu bé không đáp ứng với điều trị nội khoa và không qua khỏi sau 48h khởi phát sốc
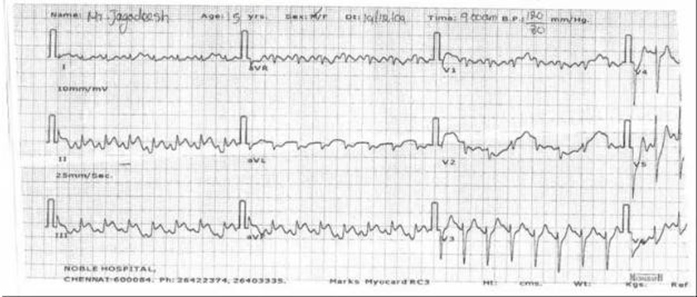
chúng ta có thể khoanh vùng viêm màng ngoài tim với sự giúp đỡ của ECG?
Điều đó là có thể. Nhưng không có mục đích lâm sàng để làm điều đó.
troponin có tăng lên trong viêm màng ngoài tim?
Viêm màng ngoài tim không tăng troponin nhưng nếu ở vùng thượng tâm mạc bị có thể dẫn đến tổn thương viêm cơ và tăng troponin
Chú ý viêm màng ngoài tim ở vùng sau/thượng tâm mạc có thể bắt chước nmct thành dưới hoặc trước. vì vây có thể tránh can thiệp vành không cần thiết
73. Một cách đơn giản và hiệu quả để ngăn chặn một đợt ngất do phản xạ phế vị!
Ngất do phản xạ phế vị Vasovagal là nguyên nhân hay gặp nhất. cơ chế do phản ứng bất thường của phản xạ phế vị đáp ứng với sự gia tăng đột ngột hoạt động sau khi đứng thẳng lên, có liên quan tới cảm xúc hoặc căng thẳng. receptor của phản xạ này nằm ở thất trái Có hai thành phần tham gia
Ức chế tim mạch giảm co mạch
Vấn đề chẩn đoán
Trước khi chẩn đoán ngất do phản xạ phế vị cần loại trừ các nguyên nhân bệnh lý tim mạch

Xử trí ngất vasovagal.
Hỗ trợ tinh thần Dùng thuốc
Một số thuốc có tác dụng như chẹn beta, cortisone Đây là những biện pháp đơn giản, rẻ tiền
DDDR máy tạo nhịp tim được cấy trên toàn thế giới cho hàng ngàn bệnh nhân bị ngất vasovagal.
Nước (H2O!) uống với số lượng thích hợp có thể ngăn hầu hết các trường hợp ngất do phản xạ phế vị. 1 cốc nước mỗi ngày có thể thay thế máy tạo nhịp giá 10.000$
74. Ý nghĩa của sóng T hai pha?
Sóng T là sóng bí ẩn nhất trong điện tâm đồ lâm sàng. Không có gì bất ngờ nếu một sóng T cao rộng và sóng T đảo ngược rõ rệt có thể là bình thường trong ít nhất 6/ 12 chuyển đạo chuẩn (V1 V2 V3, 2, 3 AVF, và tất nhiên là cả AVR)
Các hình dạng chung của sóng T có thể là sinh lý hoặc bệnh lý
Sóng T cao T âm
T có khía hoặc 2 pha sóng T 2 phase
* Sóng T phân cực được xác định bởi vector QRS. Nói chung nó phải cùng hướng với QRS. Khi có rối loạn dẫn truyền hoặc phì đại buồng thất do thay đổi tái khử cực thứ phát.
Điều này phân biệt với sóng T 2 pha nguyên phát
Sóng T hai pha là gì?
Là sóng T được ghi ở 2 bên đường cơ sở còn gọi là sóng T hai pha. 1 số người bình thường có thể có sóng T hai pha.
Sóng T 2 pha có thể có hai loại
Dương ở cuối âm ở cuối
Âm ở cuối gặp nhiều hơn đặc biệt trong CAD.
Âm ở cuối trong chuyển đạo trước tim gợi ý thiếu máu cục bộ liên tục LAD
Điều này xảy ra do sự phân tán của tái khử cực giữa màng trong tim và thượng tâm mạc. Các cơ chế khác có thể là thay đổi gradient thất giữa vector QRS và vector sóng T. Sóng T 2 pha có quan trọng?
Sóng T hai pha là do sự thay đổi trong phân cực. Nó có thể kéo xuống hoặc kéo lên đoạn ST liền kề. khoảng QT kéo dài liên quan chặt chẽ với sóng T hai pha.
1 số sóng U có thể xuất hiện bắt chước sóng T hai pha. Điều này hay gặp trong nhịp tim chậm. LVH là một trong những nguyên nhân xuất hiện sóng T hai pha (Thông thường pha thứ 2 dương)
Sóng T hai pha có thể coi là hình thức biểu hiện của NSTEMI
Mặc dù, ST chênh xuống là biểu hiện của NSTEMI, hiện tại ở bệnh nhân NSTEMI có biểu hiện khác là sóng T hai pha.
75. Test gắng sức dương tính tương đương cơn ngắn của đau thắt ngực không ổn định
Nghiệm pháp gắng sức (EST) là một trong biện pháp đánh giá CAD.
Chẩn đoán ở những bệnh nhân nghi ngờ CAD
đánh giá tiên lượng ở bệnh nhân được chẩn đoán CAD .
Hiện nay có một sự thay đổi lớn trong suy nghĩ của chúng tôi, bệnh nhân bị đau thắt ngực điển hình sẽ chụp mạch vành và test gắng sức dương tính ít nhạy và đặc hiệu với CAD rõ ràng trên lâm sàng
Vì vậy, giá trị chẩn đoán ngày càng bị hạn chế trong việc đánh giá bệnh nhân đau ngực không điển hình.
Như nào là Test gắng sức dương tính?
Đoạn ST chênh xuống > 2-3mm Xảy ra trong 1 lúc
Hạ huyết áp
đau thắt ngực kéo dài và phục hồi
liên quan khi chụp mạch với kết quả EST dương tính?
Bệnh động mạch vành chính trái Đầu gần LAD / LCX
tổn thương nhánh nghiêm trọng
Tương quan hình thái
Những bệnh nhân này thường có tổn thương xa tâm và ở vùng bờ (rìa) tổn thương không ổn định
Ảnh hưởng của gắng sức lên hạn chế dòng tưới máu quan trọng ở điểm nào?
Khi tiến hành test gắng sức và áp lực trong mạch vành có thể ở ngưỡng lý thuyết 60- 90mmhg. Tiến hành gắng sức có thể làm những mảng bám lipid không ổn định, đây là lý do đau thắt ngực không ổn định là chống chỉ định tuyệt đối với EST.
EST dương tính mạnh gợi ý điều gì?
Nó cho thấy bệnh nhân cần chụp mạch cấp và có thể can thiệp ngay lập tức
Thông thường, những bệnh nhân này có cơn đau thắt ngực kéo dài và nhập viện vào đơn vị chăm sóc vành. đã có rất nhiều tỷ lệ mắc ACS ở những bệnh nhân này trong vòng 24 giờ EST. nhiều bệnh nhân tử vong trên đường về hoặc khi về nhà, vì vậy EST là thủ thuật kiểm tra an toàn trước khi cho bệnh nhân ra viện, thường sẽ thực hiện khi bệnh nhân đau ngực có ST chênh xuống
nếu test dương tính, bệnh nhân không bao giờ được cho về nhà ngay lập tức mà phải theo dõi và theo dõi trong 24h. thậm chí chụp đm vành nếu cần
76. Magne chống loạn nhịp như nào?
Magiê là một thuốc ổn định màng tế bào mạnh mẽ. Nó cũng được công nhận tác động nên các tế bào vận động ở vỏ não và ngăn chăn cơn động kinh, đặc biệt là sản giật thai kỳ Mg SO4 vẫn là thuốc được lựa chọn cho cơn động kinh thai kỳ. và chúng tôi đã nhận ra nó là thuốc chống loạn nhịp tuyệt với
Magiê là một đồng yếu tố trong các enzyme Na / K ATPase ở màng tế bào cơ
Tính toàn vẹn của enzyme này là điều cần thiết để duy trì hợp lý lượng kali trong tế bào. Nhiều bệnh nhân hạ kali không thể bù lên được nếu chỉ bù 1 mình K+
Dùng kèm theo magiê làm tăng lượng kali đi vào tê bào và tăng khử cực của các tế bào, làm chúng ít bị kích thích hơn
Hơn nữa, magiê cạnh tranh với ca ++ ion để đi vào các tế bào và do đó nó là một thuốc chặn canxi tự nhiên. Nó cũng giúp xử trí trường hợp loạn nhịp tim kháng canxi.
Chỉ định dùng magiê
Xoắn đỉnh. Lưu ý: Magnesium không làm ngắn được khoảng QT vẫn hiệu quả trong xoắn đỉnh. Bất kỳ VT kháng thuốc đặc biệt sau MI.
Loạn nhịp do Digoxin, hạ kali máu có nhịp nhĩ nhanh bất thường, MAT Nó được dùng liều bolus 1-2mg ( 2-3 liều )
Trường hợp nào chúng ta không nên sử dụng magiê?
Sử dụng thường xuyên magiê trong VT dai dẳng sau MI là không nên http://www.ncbi.nlm.nih.gov/pmc/articles/PMC1368485/
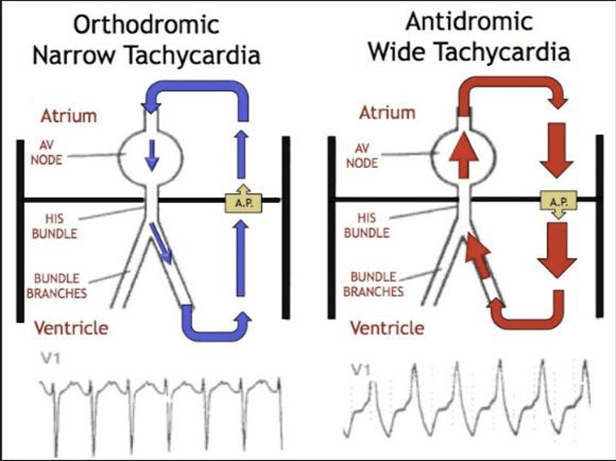
77. Verapamil và beta blockers thực sự chống chỉ định trong AVRT của hội chứng WPW?
Người ta thường nói, suy nghĩ già chết cứng! Một vài báo cáo trường hợp dùng verapamil làm tăng dẫn truyền qua đường phụ,và bất kỳ loại thuốc nào tác dụng trên nút AV đều
Nguy hiểm trong điều trị AVRT
AVRT là nhịp nhanh vào lại nút nhĩ thất, có dẫn truyền đường phụ và nhịp nhanh nhĩ. Có thể chấm dứt bằng cắt đứt đường vào lại. Cách dễ dàng và đơn giản nhất là chặn nút AV (Verapamil, thuốc chẹn beta, thậm chí digoxin!)
Những loại thuốc này đã giải quyết cho hàng ngàn bệnh nhân AVRTs . nhưng chúng tôi thấy rằng, nó không an toàn để chặn nút AV trong WPW vì nó có thể chuyển dẫn truyền sang đường phụ gây dẫn truyền 1:1 có khả năng rung thât VF
Ngay sau khi khái niệm này được báo cáo trên các tạp chí tim mạch trong đầu những năm 1980 bác sĩ tim mạch đã lấy đó làm bài giảng. Đồng thời, rất nhiều các loại thuốc chống loạn nhịp tim mới được phát triển và khái niệm này đặt ra yêu cầu phát triển thêm các thuốc mới nhóm 1 c và nhóm 3 tác động nhiều hơn nữa trên con đường phụ để loại trừ nguy cơ VF .
Tất cả các nhóm thuốc mới chống loạn nhịp nhưng kéo dài khoảng QT dẫn đến loạn nhịp thất nguy hiểm. Vì vậy, các thuốc chẹn canxi và thuốc chẹn beta đã dùng trong điều trị WPW / AVRT
Thực tế là gì?
Verapamil hoặc thuốc chẹn beta có thể gây đột tử ở bệnh nhân WPW là 1 khái niệm quá phóng đại. Block tim hoàn toàn và tỷ lệ xuất hiện RF ở bệnh nhân có hội chứng WPW it gặp do tác dụng phụ của verapamil
78. Làm thế nào để xác định bệnh nhân có nguy cơ tiến triển block AV trong hội chứng WPW?
Yếu tố quyết định chính là con đường dẫn truyền phụ. Nếu nó <250ms khả năng dẫn truyền tăng tốc được coi là cao. nghiên cứu EP cần thiết để đo giai đoạn dẫn truyền đường phụ. Nếu nó> 300ms con đường phụ dường như không tiến triển tăng tốc
Có phương pháp xâm lấn đầu giường để xác đinh giai đoạn trơ của con đường phụ? Tất cả các con đường phụ có che dấu đi khoảng RP, nếu không có dẫn truyền ngược hay bằng chứng của tiền kích thích có thể yên tâm
Những bệnh nhân này có thể tiến triển nhịp nhanh bất thường, những con đường phụ chỉ cho phép dẫn truyền ngược và chẹn nút AV là lý tưởng (không cần amiodarone)
hội chứng WPW liên tục có nguy cơ dẫn truyền ngược lại nhanh, nó sẽ mất sóng delta. Hội chứng wpw sẽ mất khi nhịp tim nhanh
Điều này rõ ràng có thấy sự giảm sút dẫn truyền tại nút AV (phá vỡ điện tự động khí nhịp tim nhanh hơn) và nó là một cơ chế an toàn . Vì vậy, người ta đề xuất ý tưởng co bn wpw
Chạy trên máy bộ đánh giá ảnh hưởng của nó với sóng delta và mức độ tiền kích thích. Thậm chí đánh giá nhịp bình thường hoặc khoảng pr kéo dài cho chúng ta thông tin đánh giá trong những thời điểm AF .
* Cũng nên nhớ một điều rằng nếu có hiện tường WPW che dấu hay wpw chỉ biểu hiện khi gắng sức là nhóm bệnh nhân nguy hiểm nhất mà dùng thuốc chẹn nút AV là chống chỉ định tuyệt đối. cần đốt AF ngay lập tức. hiện tượng trên cho thấy khi gắng sức nút nhĩ thất giảm dẫn truyền trong khi đường phụ thì không
Verapamil và betablockers không phải là loại thuốc chống chỉ định trong WPW. trong thực tế, nó có tác dụng tốt trong điều trị bệnh nhân WPW mạn tính.
Hãy nhớ điều này
Using with caution is not synonymous with contraindication
Sử dụng thận trọng không có nghĩa là chống chỉ định
79. Ecg của các vận động viên
1. ECG có thể nhịp chậm xoang, block AV 1 (AVB), RBBB không hoàn toàn, BER và đủ tiêu chuẩn điện áp của phì đại thất trái (LVH).
2. ECG có thể T âm AT chênh xuống, sóng Q bệnh lý, phì đại nhĩ, phì đại tâm thất phải, block nhánh hoặc ST chênh lên dạng Brugada .
3. bất thường ECG hay gặp ở nam giới hơn nữ giới và vận động viên sức chịu đựng cao như người đi xe đạp.
4. nhịp chậm xoang <30 bpm và ngừng xoang> 2 giây hay gặp ở các vận động viên, đặc biệt là trong khi ngủ.
5. chậm xoang là phản ứng điều hòa khi gắng sức và không rối loạn chức năng nút xoang.
6. hay gặp block AV 1 và mobitz 1, nhưng mobitz 2 hoặc block AV 3 không nên nghĩ là bình thường
7. tái cực sớm ở các vận động viên da trắng hay gặp nhất gồm ST chênh lên lõm và T đỉnh. ở vận động viên da đen thường ST chênh lên lồi và T âm bắt chước dạng brugada
8. khi có tiêu chuẩn điện áp của LVH, LVH bệnh lý nên nghĩ đến nếu kèm phì nhĩ trái, trục trái, BER hoặc sóng Q bệnh lý.
9. sóng T đảo ngược ≥2 mm ≥2 chuyển đạo liền kề nên nghi ngờ bệnh cấu trúc tim
10. test điện sinh lý với vận động viên có tiền kích thích thất
80. Tại sao block nhánh trái trước (LAFB) hay gặp hơn block nhánh trái sau (LPFB)?
Bó his chia thành 2
Bó trước Bó sau
Bó vách giữa Bó giữa
Block nhánh trái trước (LAFB) là một trong những rối loạn dẫn truyền hay gặp. Có thể lành tính hoặc nguy hiểm phụ thuộc vào tình trạng lâm sàng . thường chẩn đoán khi có sự dịch chuyển trục nó gây ra trên QRS.
theo nghĩa hẹp, điều này không hoàn toàn đúng. Lafb gây trục trái đáng kể (> -60 độ). Điều này thực tế đã làm cho việc chẩn đoán LAFB rất hay gặp ở người cao tuổi, tăng huyết áp, vv Trong những tình huống này nó có thể không gợi ý bất cứ điều gì, ngoại trừ việc chậm dẫn truyền ở nhánh trái trước.
Nếu chúng tôi lọc ra tất cả các ECG có thay đổi trục lành tính thì bệnh lý LAFB thật sự không nhiều như vậy
LAFB bệnh lý xảy ra trong các tình huống sau đây.
Block thoái hóa (bệnh Lev & Lenegre) bệnh van động mạch chủ.
Bệnh tim tăng huyết áp
Sau MI (Hoặc một mình hoặc block 2 bó hoặc 3 bó) bệnh giãn cơ tim
Ngay cả trong thoái hóa, thiếu máu cục bộ dẫn đến LAFB hơn LPFB vì sao? Những lời giải thích cổ điển
Nhánh trước liên quan vị trí dưới thượng tâm mạc Nó là một cấu trúc dài và mỏng dễ bị tổn thương
Nằm gần cấu trúc bị ảnh hưởng bởi Tắc nghẽn đường ra thất trái LVOT ** Nhanh trái trước chỉ có 1 nguồn cấp máu duy nhất (LAD)
** theo kinh nghiệm áp lực LV cao > 100mhg và dp / dt lên đến 2000mmhg (Trong khi, nhánh trái sau năm xa phần dòng chảy của LV, tiếp xúc với phần áp suất thấp – cao nhất 10mmhg)
81. Kỹ năng sâu trong y học: chẩn đoán đột quỵ nhờ ecg
Cơ thể con người là mối quan hệ tổng thể của các cơ quan. Thời bây giờ, các bác sĩ thường chỉ chăm chăm nhòm vào 1 cơ quan mà hiếm khi quan tâm tới những gì xảy ra với các cơ quan khác của bệnh nhân hay nói cách khác, anh ta chỉ rành mỗi cái mà anh ta chuyên khoa. Đây là tư tưởng chủ đạo mà các bs bây giờ đang trung thành đi theo
Hồi tưởng lại vào năm 1954. . .
Ba bác sĩ đến từ Michigan, Mỹ công bố một trong những quan sát lớn nhất trong lâm sàng, cụ thể là những thay đổi ECG trong các biểu hiện khác nhau của đột quỵ.
Bây giờ, một bác sĩ thông minh, sẽ nghi ngờ xuất huyết dưới nhện (SAH) bằng cách nhìn vào ECG và tình trạng lâm sàng. Nhưng không phải ai cũng có khả năng như vậy. ở 1 bệnh nhân cao tuổi kèm T âm sâu thường bị đẩy vào khoa tim mạch và đơn vị can thiệp thay vì phải vào đơn vị đột quỵ
Chúng ta cần phải dạy cho đồng nghiệp trẻ của chúng ta. . . Đó là ECG của bệnh nhân với hội chứng thần kinh cấp tính (ANS) có thể bắt chước các hội chứng mạch vành cấp (ACS) (đặc biệt là ở người cao tuổi).
Những thay đổi ECG sau được quan sát thấy ở bệnh nhân đột quỵ
T âm sâu – xuất huyết dưới nhện
Nhồi máu não – kéo dài khoảng QT, sóng U Xuất huyết não – thay đổi đoạn ST / T âm
Những thay đổi điện tâm đồ có xu hướng xảy ra rất sớm sau tổn thương hệ tk trung ương. Có thể kéo dài đến 1 tuần. mặc dù không giúp xác định chính xác loại đột quỵ nhưng T âm sâu gợi ý mạnh mẽ SAH hơn là ICH hay nhồi máu não
Cơ chế của những thay đổi điện tâm đồ là gì?
Đây là một bằng chứng rõ ràng rằng trái tim và não được nối với nhau bằng mạng nơron. Tất cả các thay đổi ghi nhận xảy ra trong quá trình tái khử cực cơ tim (Tức là đoạn ST) . Nó được tác động qua lại bởi hệ adreneergic khi tổn thương CNS truyền tới cơ tim bởi hệ thống giao cảm.
Tại sao SAH làm thay đổi ECG hơn những tổn thương khác?
Mạng lưới adrenegic từ thân não và tủy sống bị tác động mạng hơn trong SAH dẫn truyền toàn bộ hệ thần kinh trung ương thông qua dịch não tủy. Trong khi ICH khu trú hoặc nhồi máu tác động tới adrenergic ít hơn.
Tham khảo thêm tại http://circ.ahajournals.org/cgi/reprint/9/5/719.pdf
82. Nhồi máu cơ tim cấp tính + ảnh hưởng liên quan LVOT:
Một nguyên nhân không được công nhận của tụt huyết áp kháng thuốc
LVOT: đường ra thất trái
Tụt huyết áp là một trong những biến chứng đáng sợ của STEMI cấp tính. Nó có thể do một trong hai biến chứng lực co bóp hoặc thể tích tuần hoàn.
Tụt huyết áp trong nmct thành sau dưới thường làm tăng phản xạ phế vị và dễ dàng điều chỉnh bằng atropine và truyền dịch
RVMI là ví dụ cổ điển của tụt huyết áp có thể cải thiện với hồi sức dịch
Tụt huyết áp, nếu không thể đảo ngược trong vòng 12 giờ, có nhiều khả năng do suy bơm, rách vách liên thất.. vv.
Một cơ chế mới gây tụt huyết áp kéo dài ngày càng được công nhận. Điều này là do
1. Mất hoạt động LVOT.
2. Tăng quá mức LVOT.
Mặc dù đường ra LV có chứa tế bào cơ ít co, công việc chính là của một ống dẫn, nhưng nó cũng có tác dụng đẩy máu vào động mạch chủ. Trong thực tế, nó được cho là nhiều khả năng làm tăng tốc của vận tốc máu xảy ra trong LVOT. Vì vậy, LVOT đóng một vai trò quan trọng trong việc duy trì các chỉ số tim. LVOT quá mạnh sẽ cản trở lưu lượng máu đẩy ra như trong HCOM. Tương tự như vậy giảm hoạt động LVOT có thể làm tốc độ đẩy vào đm chủ kém gây cản trở máu từ LV vào đm chủ
Những yếu tố này được khuếch đại trong NMCT cấp, vì nó là một tình huống rối loạn co bóp và nhịp tim. Vì vậy, bắt buộc LVOT phải hoạt động 1 cách chính xác
STEMI do tắc nghẽn đầu gần LAD có thể liên quan đến các vách ngăn .Nếu nhánh vách bị tổn thương sẽ tác động tới chức năng LVOT.
Nếu hoạt động quá mức sẽ làm mất chức năng LVOT
LVOT có bờ trung gian hình thành bởi IVS, mặt trước và mặt sau .mặt bên liên quan tương đối ít trừ được bảo vệ bởi lá van trước
Nhưng ta nên nhớ lại, AML (anterior mitral leaflet lá van trước ) di chuyển về phía LVOT chỉ ở thì tâm trương. Khi di chuyển cả ở thì tâm thu thì đây là bệnh lý – SAM (Systolic anterior motion -chuyển động trước tâm thu)
Mất hoạt động phối hợp LVOT có thể xảy ra ở cả trước và sau MI. khi tổn thương nhiều nhánh mạch vành có thể xảy ra kèm mất sự phối hợp của thành trước và thành dưới
XỬ TRÍ
Không có xử trí cụ thể nhằm phục hồi chức năng LVOT.
Tái lưu thông mạch cấp cứu sẽ làm giảm bớt rối loạn chức năng cơ học Sử dụng thuốc co mạch mạnh cần cẩn thận tắc nghẽn LOVT
83. Logic vui trong tim mạch: liệu pháp tiêu huyết khối trong đột quỵ thiếu máu cục bộ và STEMI
Điều trị tiêu huyết khối là liệu pháp điều trị cho đột quỵ thiếu máu cục bộ trong vòng 3h (hiện nay là 6h). chỉ có vấn đề là, chúng ta cần loại trừ 100% đột quỵ xuất huyết trên CT / MRI. Cơ chế tác động của thuốc tiêu huyết khối đơn giảm làm tiêu huyết khối và làm cách nào để tưới máu hoặc thâm chí đảo ngược lại tổn thương do thiếu máu cục bộ tới các neuron.
Và bây giờ, chúng ta hãy xem, làm thế nào điều trị với bệnh nhân có tiền sử đột quỵ thiếu máu cục bộ gần đây với STEMI cấp tính.
Ông ta cần cấp cứu bảo vệ cơ tim bằng thuốc tiêu huyết khối hoặc PCI
Việc dùng thuốc tiêu huyết khối hoặc PCI không làm nặng thêm nhồi máu não
liệu pháp tiêu huyết khối chống chỉ định tuyệt đối ở bệnh nhân STEMI và gần đây có thiếu máu cục bộ (<3 tháng)
Vậy có nên cho dùng TPA hoặc Streptokinase?
Lý do chủ yếu chống lại việc dùng tiêu huyết khối trong đột quỵ gần đây là do nguy cơ chuyển từ vùng nhồi máu thành xuất huyết gây chảy máu não
Điều này là rất phỏng đoán, tiền sử đột quỵ thiếu máu cục bộ không làm tăng nguy cơ chảy máu . sự thay đổi từ vùng thiếu máu cục bộ sang xuất huyết chỉ xảy ra ở những giờ rất sớm sau đột quỵ cấp (chứ không phải vài tuần sau đó). Điều này có thể 1 phần do canxi gây ra tái tưới máu tổn thương.
Câu hỏi chưa được trả lời
Vấn đề trở nên phức tạp hơn nữa với suy nghĩ lệch lạc của các bạn
Nếu chống chỉ định dùng tiêu huyết khối ở STEMI, chúng ta sẽ chỉ định ngay lập tức PCI?
Có vẻ như vậy, đối với hầu hết chúng ta!
PCI có an toàn ở một bệnh nhân có tiền sử đột quỵ thiếu máu cục bộ?
PCI cấp cứu ở một bệnh nhân tiền sử đột quỵ rất nguy hiểm.
Thao tác ở cung động mạch chủ và van động mạch chủ có xơ vữa động mạch có thể làm tăng nguy cơ đột quỵ tiếp theo.
Thuốc chúng ta dùng trong PCI không phải là loại vô hại. Aspirin, Heparin, clopidogrel (đôi khi thậm chí 2b 3a!) Sẽ cũng vẫn làm cho vùng nhồi máu thiếu máu cục bộ chuyển thành vùng xuất huyết. Đừng có suy nghĩ PCI sẽ an toàn hơn dùng TPA.
Vì vậy, đừng dễ dàng quyết định PCI ở bệnh nhân cao tuổi có STEMI và CVA gần đây. Vì vậy, ở bệnh nhân đột quỵ thiếu máu cục bộ có thể dùng TPA an toàn không phân biệt thời gian bị đột quỵ. Điều này nghe có vẻ trái với sách vở. Điều chúng ta làm không phải phi đạo đức với các tài liệu khoa học, cũng phải khó khăn những bằng chứng khoa học nhiều khi chỉ là lý thuyết
Theo như tôi đã tìm kiếm các ưu hoặc nhược điểm của TPA và PCI trong CVA thiếu máu cục bộ thấy rằng điều này chưa bao giờ được so sánh 1:1. Thực tế có thể thấy điều này cũng sẽ không bao giờ có trong tương lai. Có vẻ như PCI giành được phần thắng áp đảo so với TPA
Câu hỏi chưa được trả lời
Làm thế nào để giảm tỷ lệ tử vong ở bệnh nhân đột quỵ sau dùng TPA?
Làm thế nào kết hợp an toàn aspirin, heparin và clopidogrel ở bệnh nhân bị đột quỵ gần đây?
Làm thế nào để quyết định sẽ dùng TPA với bn có STEMI và CVA gần đây? Câu trả lời là tùy thuộc vào
Thời gian bị CVA
Vị trí của vùng ổ nhồi máu não Kích thước của vùng nhồi máu Tổn thương thần kinh khu trú
Các ổ nhồi máu lớn tại vị trí quan trọng mới cần sợ biến chứng chuyển từ nhồi máu sang xuất huyết. Tất cả nhồi máu não nhỏ, ở vị trí lành tính không cần lo lắng về biến chứng này
Làm thế nào để đánh giá khả năng phục hồi của ổ nhồi máu não?
Việc phục hồi và phát triển mô đêm phụ thuốc nhiều vào phản ứng cá nhân với hội chứng viêm. Một số lành trong vòng vài tuần,tăng sinh mạch tân tạo trong khu vực hoại tử.nguy cơ chuyển từ vùng hoại tử do thiếu máu cục bộ thành xuất huyết hoại tử dưới 1% . chống chỉ định dùng TPA ở bn CVA là điều độc đoán quá buồn cười
MRI là công cụ tốt nhất dự đoán được vùng nhồi máu an toàn để sử dụng TPA? Hiện tại, chúng ta chưa có công cụ tốt để xác định vùng nhồi máu an toàn có thể chịu được TPA. Nếu có các công cụ chẩn đoán hình ảnh nâng cao, chúng ta có thể dự đoán sự hình thành mô đệm và tân tạo mạch.
Làm thế nào để xử trí 1 bn nam STEMI gần đây có đột quỵ do nhồi máu não?
A. đưa ông đến phòng can thiệp và PCI
B. tiêu huyết khối với TPA hoặc Streptokinase
C. theo dõi và xử trí với Heparin * Trả lời: ý nào bên trên cũng đúng.
• Heparin được coi là lựa chọn trong STEMI có đột quỵ gần đây
Hãy bỏ suy nghĩ kiểu buồn cười như “Nếu TPA chống chỉ định, thì mình phải chọn PCI” đây là điều hoàn toàn sai sự thật!
84. Bài viết quan trọng nhất từng được công bố về nhịp nhanh QRS rộng!
QRS rộng nhịp nhanh thường gợi lên phản ứng OCD (Obsessive compulsive disorder rối loạn ám ảnh) giữa nhiều chuyên gia tim mạch. Bất cứ khi nào chúng ta gặp nhịp nhanh
QRS rộng, chúng ta lại phải tranh luận nó là VT hay SVT. Hàng chục ngàn bài báo, hội thảo, CMES, đã được tiến hành trong hơn 30 năm để giải mã QRS rộng kèm nhịp tim nhanh bất thường. Thực tế là vãn có sự nhầm lẫn phổ biến
Trong khi test gắng sức (EST) nhạy trong chẩn đoán tim mạch lâm sàng tới 75%, 99 % tiêu chuẩn nhạy trong chẩn đoán VT lại không được tôn trọng.
* Tất cả nhịp nhanh QRS rộng ở những bệnh nhân có tiền sử CAD / STEMI sẽ là VT bài viết này được xuất bản vào năm 1988
“Chẩn đoán nên đi trước điều trị bất cứ khi nào có thể”
Nhưng công sức, thời gian, chi phí liên quan chẩn đoán nên có ý nghĩa (hay không cần chính xác quá)
Vấn đề ở đây không phải là khoa học hay không khoa học, nhưng cho dù bạn đúng hay sai. Các bài viết được trích dẫn ở đây có một cái nhìn sâu sắc tuyệt vời đầy triết lý về chẩn đoán VT.
Trong chẩn đoán QRS rộng nhịp nhanh, Nếu chúng ta áp dụng cái gọi là nguyên tắc khoa học sẽ chẩn đoán sai VT tỷ lệ rất cao, trong khi nếu bạn chẩn đoán mù theo logic của bạn thì lại đúng đến 90% mặc dù vô lý nhưng nó hoàn toàn đúng sự thật!
Một bác sĩ trẻ nên nhận ra tầm quan trọng của việc này. chẩn đoán VT không hay gặp trước năm 1980. Nó đã trở thành một hiện tượng mới.
85. Làm thế nào để bạn xác định vị trí tổn thương trong block nhánh phải?
Giống như trong bệnh thần kinh, người ta có thể xác định vị trí block tại các nhánh, mặc dù điều này ít ai nghĩ nó có giá trị lâm sàng (Không giống như các tổn thương mạch vành)
Nói chung, RBBB có thể chia type gần hoặc xa (ngoại vi). Vị trí hay gặp là type xa hơn 100 năm nghiên cứu về ECG, chúng ta đã sử dụng 1 số thuật ngữ không chính xác, thậm chí ngày nay vẫn có người cho rằng ― chậm dẫn truyền với block là 1 và giống nhau‖
Trong thực tế, RBBB vẫn có dẫn truyền không đầy đủ qua các nhánh này Ví dụ về chậm dẫn truyền RV / RVOT
Bất cứ bệnh gì làm RVOT giãn đều có thể gây RBBB thông liên nhĩ
Nhiều trường hợp RVH tăng áp động mạch phổi
dạng rSr’ lành tính ở V1 là gì?
Đây là do quá trình khử cực tương đối muộn của dòng chảy RV
Nhiều người có dạng rSr’ này không có tổn thương ở RBB trong ASD.
Gọi rSr’ là dạng RBBB không hoàn toàn là không nên (Như nhiều sách ECG đề nghị) . bởi vì, mặc dù RBBB hoàn toàn cũng không có nghĩa là hoàn toàn không dẫn truyền . hơn nữa r’ ở V1 hoặc S ở V1 không thể hiện được tính đầy đủ của RBBB.
Block nhánh phải hoàn toàn là block hoàn toàn?
Đúng khi
Nmct thành trước rộng
Một số trường hợp Ebstein bất thường.
86. Tại sao tụt huyết áp hay gặp hơn ở nmct thành sau dưới?
Trái tim con người là một khối cơ nặng khoảng 300-400 gram. Các nguồn cung cấp máu của khối cơ này rất khác nhau. Một số khu vực nhiều mạch máu (ví dụ như -IVS.) Một số khu vực có nguồn cấp máu bởi động mạch đôi (Thường ở vị trí giao nhau LCX và RCA). Một vài khu vực có nguồn cung cấp máu không ổn định. Đó là khu vực dễ bị tổn thương hay tam giác Bermuda của trái tim – khu vực tạo bởi đỉnh LV, thành tự do và mặt trước. Khi nguồn cung cấp máu không đồng nhất, thì hệ thống nội tại của tim cũng có nhiều kiểu . hệ thống thần kinh tự động tim dẫn truyền qua các đám rối thần kinh tim. Thành trước của tim chứa nhiều sợi giao cảm giàu catecholamine, thành sau tim có nhiều sợi phó giao cảm
Vì vậy, nó trở nên dễ hiểu, tại sao thiếu máu cục bộ của vùng sau dưới thường tạo ra phản ứng phó giao cảm và thành trước thiếu máu cục bộ lại gây phản ứng adrenergic. Tuy nhiên, tác động chồng chéo có thể xảy ra trong CAD nhiều nhánh (multivessel) với lưu thông phụ thuộc vòng tuần hoàn phụ
Nmct thành sau dưới, tiên lượng thường tốt vì nó giống như thuốc chẹn beta tự nhiên (giảm nhịp tim, giảm độ tiêu thụ oxy cơ tim- MVO2) và tụt huyết áp là biến chứng đáng lo ngại trong nmct thành sau dưới
Các yếu tố sau đây góp phần gây tụt huyết áp ở STEMI thành sau dưới
Tăng phó giao cảm do phản xạ Bezold jarish
Tổn thương thất phải gặp trong 40% nmct thành sau dưới. mất hoạt động bơm thất phải là giải thích trước đây gây tụt huyết áp
Gần đây công nhận thực tế: nmct thành sau dưới thường có sự tham gia hoạt động điện của tâm nhĩ. Đây là một sự kích hoạt mạnh mẽ gây tiết peptide lợi niệu nhĩ ANP. ANP là hormone gây mất nước và tụt huyết áp trong trường hợp này. Cũng cần lưu ý hoại tử nhĩ không nhất thiết tăng sinh ANP. Căng nhĩ hoặc căng thất phải đều kích thích sinh ANP Cũng có trường hợp kèm tác động tới thất trái trong nmct thành sau dưới. nó ảnh hưởng bất lợi tới chức năng LV, và là yếu tố độc lập gây tụt huyết áp.
An thần quá mức với morphine có thể làm nặng thêm hoặc gây tụt huyết áp. (tác động phó giao cảm của morphine)
Cuối cùng và cũng là nguyên nhân quan trọng nhất là mất thể tích (vã mồ hôi nhiều và nôn nặng có thể mất tới 10 lit nước trong cơ thể)
Làm thế nào để xử trí ?
Bù thể tích tuần hoàn đầy đủ
Bù dịch trong nmct thất phải theo quy tắc nếu 1 lit truyền tĩnh mạch xả nhanh không đáp ứng tốt thì phải bù thêm 5 lit mới có đáp ứng nhưng sẽ gây quá tải dịch và hạ Na máu Atropine (Đây là một trong những tình huống hiếm hoi mà atropin phong tỏa phó giao cảm để gây tăng huyết áp) .Dopamine có thể có tác dụng nhưng chúng ta cần giảm trương lực phó giao cảm và để phục hồi tính tự động. (Tăng trương lực giao cảm trong khi phó giao cảm vẫn tăng mà muốn phục hồi tính tự động của tim là điều không logic)
Tạo nhịp tạm thời có thể cần nếu huyết áp không tăng vì mạch chậm dai dẳng.
Hạ huyết áp trong nmct thành sau dưới thường xem như vô hại. Tuy nhiên, nó có thể nguy hiểm ở một số người, đặc biệt là ở người già và khi kèm theo nmct trước đó. Hiểu được cơ chế gây tụt huyết áp sẽ giúp chúng ta xử trí nhanh chóng và dễ dàng
87. Một “tin xấu” cho những người có hội chứng tái cực sớm lành tính BER
Hội chứng tái cực sớm lành tính ERS –được coi là rối loạn trên ECG lành tính trong nhiều thập kỷ qua. Nhưng hiện tại nó bắt đầu có bằng chứng cho thấy nó sẽ dẫn đến loạn nhịp thất
ERS do những biến đổi phức tạp của các kênh ion trong tái khử cực của tim (cụ thể, đó là do tăng chức năng của các kênh ion K + trong phase 3 của điện thế hoạt động) .đây là quá trình rất lành tính. Nhưng, những gì chúng ta phải quan tâm là nó có thể dẫn đến các rối loạn nhịp thất nếu bệnh nhân đang có thiếu máu cục bộ
Khi tái cực xảy ra sớm nó gián tiếp rút ngắn khoảng QT. QT ngắn hay dài(<320ms,> 460ms) đều có thể nguy hiểm.
ERS là một dấu hiệu báo hiệu nguy cơ VF?
Dạng BER ở chuyển đạo dưới tiềm ẩn nguy cơ tử vong cao sau này ở bệnh nhân trung niên http://www.nejm.org/doi/full/10.1056/NEJMoa0907589?keytype2=tf_ipsecsha&ijkey=05 d042b1253645ccf488e0f42898bfbf01496dec
88. Tại sao LVH tạo ra điện áp QRS cao ở 1 số bệnh nhân, 1 số bệnh nhân QRS điện áp lại thấp hoặc có sóng q?
LVH là một trong những bất thường ECG phổ biến nhất. Chúng ta chẩn đoán LVH khi có tăng điện áp QRS. tăng điện áp QRS khá chính xác trong việc chẩn đoán LVH nhưng không có nó không thể loại trừ LVH.
Tại sao tăng điện áp QRS không hay gặp trong LVH?
Mặc dù chúng tôi nghĩ rằng khối lượng cơ tim là yếu tố quyết định duy nhất của điện áp QRS, trong thực tế nó được xác định bởi nhiều yếu tố khác.
Khoảng cách giữa các đạo trình ECG và cơ tim là một yếu tố quan trọng. khoang LV không được làm rộng ra, thực tế là nó có thể co lại 1 chút do phì đại cơ vào bên trong và chén ép khoang LV. Khối lượng máu trong LV là một nhạc trưởng rất tốt của điện thế.
Thể tích LV lớn sẽ làm tăng điện áp QRS. Điều này có thể thấy ở 1 số bệnh nhân DCM có điện áp QRS cao bắt chước LVH. Nhưng, những gì thực sự quan trọng là sự cân bằng của khối lượng máu và khối lượng cơ tim sẽ xác định tỷ lệ và cường độ của LVH trong ECG.
QRS điện áp như một công cụ để phân biệt bệnh lý từ LVH sinh lý
Chúng ta biết dạng QRS được tạo ra từ bên trong các tế bào cơ .Nếu các tế bào cơ phì đại đồng đều sẽ không làm thay đổi dạng QRS và có hình ảnh điện áp QRS cao cổ điển của LVH
Nếu LVH xảy ra ở các tế bào cơ phì đại vô tổ chức, các sợi cơ xen với bó cơ liền kề, điện áp QRS có thể không tăng hoặc thậm chí có dạng móc hay chữ V như nhiều trường hợp bất thường dẫn truyền trong thất
Các bất thường phì đại cơ tim của HCM gây sóng q bệnh lý.
* Các yếu tố khác xác định LVH bao gồm block nhánh hoặc bó. (Ví dụ: LBBB không hoàn toàn có thể làm tăng điện áp QRS mà không cần phải có LVH)
LVH bị xơ hóa
Xơ hóa không phải là một tiêu chuẩn của LVH. Nó xảy ra ở một số ít người do vấn đề và hệ tuần hoàn quá nhạy cảm với các yếu tố tăng trưởng.
Xơ hóa có thể có tác động rộng trên điện thế cũng như chức năng cơ học của tim.
Xơ hóa tim làm giảm điện áp QRS, thậm chí có thể gây ra sóng q bệnh lý. Có thể dẫn đến các rối loạn nhịp thất, ngăn suy thoái LVH.
Các nguyên nhân khác làm giảm bớt điện áp LVH trong ECG
– Bn tăng huyết áp tiểu đường thường điện áp QRS thấp hơn bn THA đơn độc
– Bệnh nhân suy thận thường không có điện áp QRS cao dù có LVH Chẩn đoán LVH bởi ECG đơn giản nhưng các cơ chế quá phức tạp
Một câu hỏi đơn giản, Tại sao có LVH lại không làm tăng điện áp QRS? . . . câu hỏi quá khó, nhưng có một điều rõ ràng, LVH sinh lý (Có nghĩa là LVH, hoàn toàn là do SHT / Hẹp động mạch chủ) thường có điện áp cao, trong khi ở LVH bệnh lý (bị nhiễm khuẩn với xơ hóa) lại làm tăng điện áp không phù hợp.
89. Cơ chế tím tái trong tăng áp động mạch phổi nguyên phát
Làm thế nào xuất hiện tím trung ương trong tăng áp động mạch phổi nguyên phát?
Trong khi, tím tái ngoại vi giải thích dễ dàng trong tăng áp động mạch phổi nguyên phát (PPH) thì tím trung ương lại không dễ như vậy.
Những lời giải thích sau đây được chấp nhận
Lỗ bầu dục (PFOS) bị mở do áp lực nhĩ phải cao
Thay đổi QP / QS . 1 số shunt không có máu oxy hóa (shunt phải sang trái trong phổi) bệnh lý phổi như viêm phổi dẫn đến shunt phải- trái qua tuần hoàn phế nang
* Tím tái ngoại vi có thể xảy ra trong PPH – suy tim
** PFOS là cấu trúc giải phẫu gặp ở 20% dân số, thông khi áp lực nhĩ phải cao
Tím tái – mô tả ngắn gọn.
Tím tái xảy ra khi bão hòa oxy động mạch dưới 85%. Tím tái thể hiện bằng hai cách. Trung ương và ngoại vi. Tím ngoại vi là ý nói tuần hoàn ngoại vi chứ không phải ngoại vi cơ thể. Cơ chế tím ngoại vi hơi khác so với tím trung ương. Nó thường do giảm lưu thông máu, sử dụng nhiều oxy gây màu xanh tím
tím tái ngoại vi hay gặp ở đầu ngón tay, môi… tím ngoại vi có thể không gặp những khu vực ấm áp của cơ thể do vùng này giãn mạch. Tưới máu mô tốt hơn, ngăn tình trạng ứ trệ máu đã khử oxy thiếu oxy trung ương đơn độc không thể dẫn tới tím trung ương .
tím trung ương xảy ra phải cần có hiện tượng pha trộn máu đã khử oxy và mang oxy (shunt phải sang trái trong tim hoặc phổi)
Vì thiếu oxy trung ương nên nó tím cả vùng niêm mạc ấm cũng như chi lạnh
90. Khi nào chẩn đoán thiểu sản động mạch chủ
Thiểu sản động mạch chủ hay gặp trong các bệnh lý tim bẩm sinh, đặc biệt là hypoplasia động mạch chủ là một quan sát phổ biến ở nhiều bệnh tim bẩm sinh đặc biệt những bệnh bẩm sinh không tím tái.
Thiểu sản động mạch chủ được cho là do 2 cơ chế
1. giảm lượng máu tới tử cung (tim thai) dẫn đến thiểu sản
2. sự xâm lấn của mô tuyến lân cận tới quai đmc khi ống động mạch đóng lại
Ở trẻ sơ sinh, khi nào bạn nghi ngờ có thiểu sản động mạch chủ?
Thiểu sản đmc được chẩn đoán khi,
Eo dmc <40% đường kính đoạn lên của động mạch chủ
Đoạn vòm đầu gần<60% đường kính động mạch chủ đoạn lên Đoạn vòm đầu xa <50% đường kính động mạch chủ đoạn lên Tại sao lại đi so với đoạn lên của động mạch chủ?
Bới nó ít có khả năng bị ảnh hưởng co lại bởi mô tuyến xâm lấn. dmc đoạn xuống cũng có thể dùng để so sánh nhưng nó nằm ở xa hơn và khó nhìn để so sánh
91. Đừng thổi phồng và nên hiểu bản chất. Nhiều người đã tử vong vì đặt stent trong hẹp động mạch thận
Đối với khoa học ngày nay, nhiều thứ suy luận logic chưa chắc đã tuyệt vời. Giống như khẳng định ―bệnh tiểu đường là yếu tố nguy cơ chính gây bệnh tim mạch, nhưng kiểm soát được bệnh tiểu đường cũng không thể loại bỏ yếu tố nguy cơ này‖. Tương tự vậy, bệnh lý tổn thương nhiều động mạch vành cũng không nhất thiết phải có rối loạn chức năng thất trái. Theo bản năng của con người, cứ có cái gì cản trở họ sẽ có xu hướng muốn giải phóng nó.
Ví dụ, 1 quả thận giãn tối đa do sỏi, nhu mô thận mỏng dính rồi nhưng bác sĩ vẫn động viên mổ phanh lấy sỏi dù lấy xong quả thận cũng không hồi cũng như có tác dụng gì.
Các bác sĩ can thiệp CDHA hay tim mạch hiện nay bất chợt có suy nghĩ đặt stent nong động mạch thận hẹp do nhiều nguyên nhân (THA, xơ vữa….) và đáng ngạc nhiên khi nó không có lợi ích gì với việc giảm huyết áp hay hồi phục chức năng thận.
Can thiệp mạch thận nổi tiếng nhiều biến chứng và đa số không được báo cáo http://www.nejm.org/doi/pdf/10.1056/NEJMoa0905368 http://www.nejm.org/doi/full/10.1056/NEJMoa0905368#t=article
Vào thời đại này, làm 1 bác sĩ thông minh phải biết chọn lọc thông tin để thực hành lâm sàng.
92. Bạn đã gặp nmct cấp xuất hiện với VT ổn định?
NMCT cấp và VT có liên quan chặt chẽ với nhau. Trong thực tế, phản ứng đầu tiên với thiếu máu có thể là một VT Nhưng điều đặc biệt là nó hầu như luôn thoái triển thành VF trong vòng 1 phút hoặc lâu hơn (Không giống như VTs vô căn / RVOT / LVOT VTs). rối loạn nhịp tim trong trường hợp này có thể gọi là ― VT nguyên phát‖ là nguyên nhân gây ―VF nguyên phát
Người ta tin chắc rằng VF không thể xảy ra mà không cơn VT ngắn trước nó Mặc dù có mối quan hệ mật thiết giữa VT và STEMI, nhưng hiếm khi có bệnh nhân STEMI vào cấp cứu kèm theo VT ổn định. Trong khi nhiều trường VTs có huyết động ổn định thường ít khí thoái triển thành VF
* Lưu ý: theo kinh nghiệm, VT ổn định trong STEMI sẽ chuyển thành VF trong vòng 60 giây. Nếu không, nó là hiện tượng rất bất thường
“Nhưng trong y học luôn có cái gọi là bất ngờ “
Báo cáo 1 trường hợp, một bệnh nhân vào cấp cứu vì VT dai dẳng (tương đối ổn định) với dạng LBBB. Chúng tôi nghĩ nó là VT không thiếu máu cục bộ (bệnh cơ tim, RVOT vv) . Khi thăm khám, bệnh nhân không ổn định, được sốc điện 50J hai pha. Đáng ngạc nhiên sau sốc điện lộ ra STEMI và ngay lập tức được dùng tiêu huyết khối
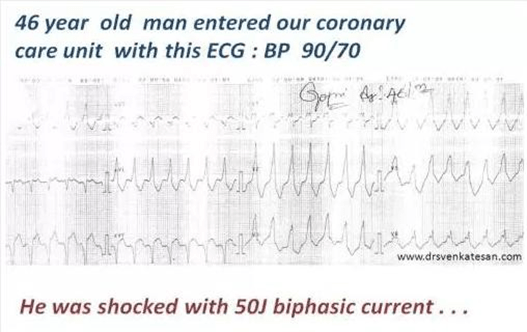
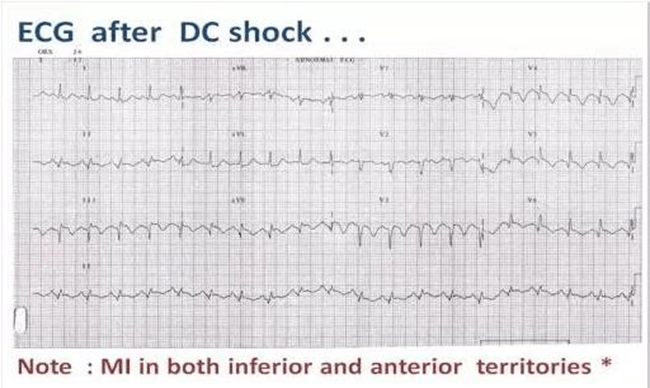
* Có thể, bệnh nhân đã có MI cũ mà nhồi máu lại xuất hiện VT.
Nhưng trường hợp này vẫn ít gặp vì nó không thoái triển thành VF trong STEMI
Gần như tất cả các trường hợp nhịp nhanh thất, xảy ra vào những phút đầu sau STEMI sẽ chuyển sang VF sau vài phút/h
Vô cùng hiếm hoi cho 1 VT thiếu máu cục bộ cấp do STEMI lại có thể đi lại trong bệnh viện được
Chúng ta đặt ra 2 câu hỏi:
Điều gì quyết định chuyển VT thành VF?
Tại sao vòng vào lại lớn, sẹo do VTs thường tiên lượng tốt? (Mặc dù rối loạn chức năng LV!)
Block nhánh trái – câu hỏi ít gặp
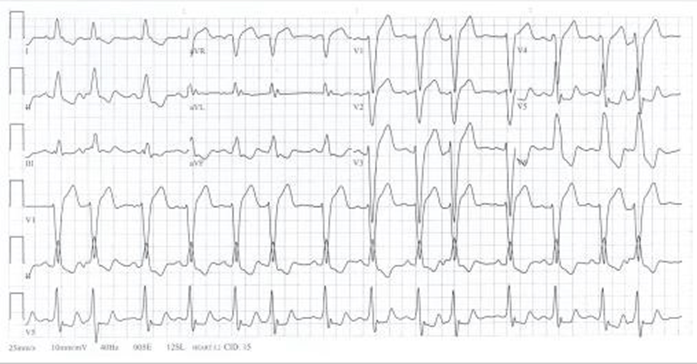
Tại sao QRS cao và rộng hơn trong LBBB?
QRS rộng, do dẫn truyền chậm hơn sợi không liên quan .QRS cao do thời gian co của RV và LV không cùng nhau (phân ly)
Mặc dù block hoàn toàn nhưng vẫn có sự dẫn truyền. Nó phụ thuộc vào mức độ của LBBB.
cơ chế và ý nghĩa lâm sàng của trục trái trong LBBB đơn thuần?
đáng ngạc nhiên là trục QRS trung bình không thay đổi lớn trong LBBB. Nếu trục chuyển trái gợi ý bệnh lý liên quan LV hoặc liên quan nhánh trước trái tác động của việc co IVS và thời gian LBBB?
Trong LBBB đơn thuần, chuyển động vách bất thường làm thay đổi thời gian kích hoạt vách ngăn. Điều này dẫn đến sự xuất hiện bất thường về chuyển động vách ngăn. Trong thực tế, giảm chuyển động bất thường này gợi ý chức năng LV tốt.
Tại sao chuyển động bất thường của vách trong LBBB, không xảy ra đồng thời trong LV bình thường?
CRT là điều trị trong tưởng tượng ở những bệnh nhân với LBBB và suy tim. ở trường hợp tâm thất bình thường, LBBB không làm mất ổn định chức nhưng LV mặc dù chuyển động vách không đồng thời với LV co. Đây vẫn là một bí ẩn những bất lợi của LBBB là gì co vách ngăn không đồng thời trào ngược van hai lá
LBBBs mãn tính đơn thuần không dẫn đến bất kỳ bất lợi nào về huyết động học của LV- tại sao?
LBBBs nguy hiểm trên ECG, nhưng với hầu hết các bệnh nhân thì nó lành tính trong trường hợp không có bệnh cấu trúc tim, van tim, cơ tim hay thiếu máu cục bộ. Có thể có sóng r nhỏ ở V1 và V2 trong LBBB?
Đúng vậy . Mặc dù chúng ta mong đợi sự đảo chiều của quá trình khử cực vách làm mất sóng r ở v1 – v3. Do đó xuất hiện của r nhỏ trong v1 -v3 không loại trừ LBBB.
Lời giải thích được chấp nhận là lực co của vách RV được che đậy bởi lực co của LV sớm hơn.
Một khả năng khác là do sự chuyển động tự do của vách thất trong trạng thái bệnh lý.
Khả năng thứ ba là “r” có thể thực sự đại diện cho những sóng q vách ngăn như trong LVH hay AWMI cũ. (y hệt q nhỏ chuyển đạo bên)
Làm thế nào giải thích hình dạng QRS phù hợp “concordant” ở V1-V6 trong LBBB?
Chúng ta hy vọng QRS chuyển từ QS sang RS, ít nhất cũng phải có ở v5 / v6 . nhiều trường hợp ta thấy V6 có dạng RS. Đây thường do lỗi vị trí hoặc do LV rất lớn. Nếu chúng ta ghi tại V7 hoặc V8 sẽ có hình dạng hoàn chỉnh
Điều gì sẽ dẫn đến VPD phức bộ thất đến sớm bắt nguồn từ LV trong trường hợp LBBB?
Nhịp ngoại tâm thu thất là 1 dạng block lành tính! VPD thường vẫn dẫn truyền xung điện bình thường và QRS bình thường. Vì vậy, khi một bệnh nhân LBBB đột nhiên xuất hiện dạng QRS bình thường hoặc nhịp nhanh QRS bình thường ta nên nghĩ đến VT phát sinh từ tâm thất trái. Điều này được khẳng định qua các nghiên cứu điện sinh lý
Hình thái VPD nếu nó phát sinh từ RV và vách ngăn trong trường hợp LBBB?
Cần trả lời câu hỏi
ảnh hưởng của LBBB trên S1 và S2 là gì?
Mô tả trước đây trong LBBB là S2 tách đôi bất thường
S1 rộng chia đôi
Bạn phải nghe 4 thành phần trong LBBB. trong thực tế điều này không xảy ra. Tốt nhất bạn có thể nghe thấy S2 tách đôi.
Một lý do khác khiến cho ta khó nghe những tiếng tách đôi là yếu tố gây nhiều như rối loạn chức năng LV, MR, khoảng PR….
ở bệnh nhân LBBB, có tăng nguy cơ tiến triển thành block AV hoàn toàn khi dùng chẹn beta hay chẹn kênh canxi ?
Thông thường sẽ nói là có. Còn về ý nghĩa khoa học không có câu trả lời. Chúng ta biết, tâm thất chi phối bởi 2 bó .Khi chỉ có một có chức năng, thì 50% cung cấp dẫn truyền cho thất bị gián đoạn. Trong CAD, chỉ còn 1 mạch cấp máu được như nguy hiểm nhưng xung dẫn truyền thì không như vậy! Mặc dù thực tế là tâm thất có nhiều tế bào dẫn truyền xung điện nhưng tốt hơn nên thận trọng dùng thuốc chẹn beta, thuốc chẹn calci và digoxin ở bệnh nhân LBBB. Nếu dùng
phải theo dõi sát. (khoảng HV (thời gian dẫn truyền qua bó sợi his- purkinje trong LBBB hơi dài). Không bao giờ dùng thuốc ―block nhịp‖ ở bệnh nhân mới khởi phát LBBB và ACS
http://bilagi.org/blog/2012/07/17/diagnosing-level-of-av-block-pa-interval-ah- interval-and-hv-interval/
94. Phân loại tứ chứng Fallot
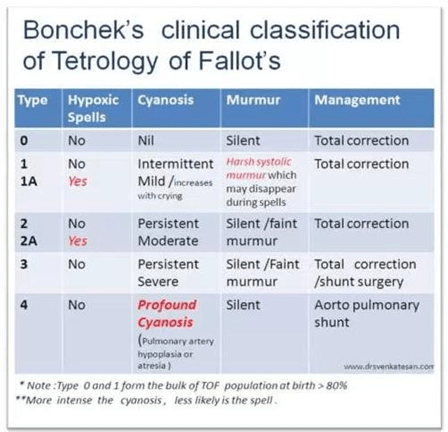
95. Một số ý kiến về viêm màng ngoài tim trong hội chứng tăng ure huyết
Màng ngoài tim là một màng sinh học rất nhạy. nó bị ảnh hưởng khi thận có vấn đề. Chúng tôi gọi đây là tiếng cọ màng tim do tăng ure huyết, nhưng đây là hiện tương ít gặp ở bệnh nhân suy thận. Xảy ra ở khoảng 10% bệnh nhân suy thận.
Cơ chế
viêm màng ngoài tim liên quan chất hóa học : ure?
Lọc máu có thể viêm màng ngoài tim nhiễm trùng l
Hai cái này đều có thể xảy ra.
Viêm màng ngoài tim không tràn dịch.
Tràn dịch màng ngoài tim mà không viêm màng ngoài tim Cái sau hay gặp hơn.
Nó là dịch tiết hay dịch thấm?
Thông thường là dịch thấm do tích tụ protein.
Tràn dịch xuất huyết hay không xuất huyết?
Một lần nữa cả hai đều có thể xảy ra. rối loạn chức năng tiểu cầu gặp trong suy thận . chảy máu vào khoang màng ngoài tim chỉ vài cc máu là đủ để làm dịch màng ngoài tim chuyển màu đỏ
ECG của viêm màng ngoài tim tăng urê huyết, có gì khác?
Viêm màng ngoài tim ure huyết ít khi dẫn đến ST chênh lên mà có hình ảnh tăng kali máu chiếm ưu thế- nếu có
Lý do ít khi ST chênh lên cao do dịch màng ngoài tim nhiều phân tử ure tích điện trái dấu nên trung hòa về điện tích
Mối quan hệ với lọc máu
Sự xuất hiện tiếng cọ màng ngoài tim là dấu hiệu cần chạy thận
Điều trị
Indomethacin / NSAID khác steroids
chọc hút dịch màng ngoài tim
Phẫu thuật có thể cần thiết nếu viêm màng ngoài tim tái phát Tài liệu tham khảo http://emedicine.medscape.com/article/244810-overview http://circ.ahajournals.org/cgi/content/short/53/5/896
điều trị phẫu thuật http://ats.ctsnetjournals.org/cgi/content/abstract/22/6/588
96.Đừng bỏ qua cơn đau lưng ở phòng cấp cứu…bạn sẽ có thể phải trả giá!
Đau ngực có thể là 1 triệu chứng của MI cấp làm bệnh nhân phải vào cấp cứu.tim nằm trong lồng ngực và rộng ra phía sau khoảng 15cm. Vị trí tim bên trong thành ngực tạo thành cấu trúc ba chiều. Về mặt lý thuyết, đau có thể bắt đầu tập trung ở một điểm và lan ra theo bất kỳ hướng nào. Theo cổ điển, khi chúng ta nói đau ngực, chúng ta thường chỉ nói đến thành ngực 2 bên. Về mặt kỹ thuật, ngực có thành sau. Mặt sau của ngực nhiều khi đơn giản chỉ gọi là lưng
Chúng ta biết, đau ngực có thể lan ra nhiều nơi, thường lan ra vai và cánh tay trái.
Chúng ta thường nghĩ rằng cơn đau của MI chỉ đến từ cơ tim, nhưng có nhiều nguồn liên quan như:
Màng ngoài tim liền kề Động mạch vành
Đau thần kinh do các dây thần kinh thiếu máu cục bộ Cuối cùng là đau tham chiếu qua da
Một số người tin rằng khi nhồi máu hoàn toàn cả nơi nuôi các đầu tận thần kinh sẽ không xuất hiện tín hiệu đau và bệnh nhân không đau, trong khi cơ chết sẽ làm đau tối đa. Hệ thống thần kinh soma, phản chiếu đau nội tạng tới da làm bệnh nhân tưởng đau bắt nguồn từ những vị trí này. tim là một cấu trúc phản ánh cơn đau chủ yếu ra thành ngực trước, không có gì ngạc nhiên nếu nó chệch hướng cơn đau ra phía sau. Tất nhiên, xương và thành sau ngực dày có khuynh hướng ngăn chặn sự lan ra này
Tuy nhiên, trong nhiều trường hợp, bệnh nhân vào CCU hoặc ACS chỉ vì đau lưng sau ngực. Những điều sau đây đã được quan sát.
Đau lưng nghiêm trọng ở bệnh nhân STEMI lớn thường chỉ ra tình trạng rách cơ tim. Tắc động mạch mạc treo và tạng
Bóc tách động mạch chủ đau lưng chỉ do STEMI
Tất cả các nhà tim mạch sẽ thấy ít nhất vài trường hợp STEMI chỉ có đau lưng. Vấn đề đau lưng sẽ có thể vào 1 số khoa khác nhau.
Đau lưng như là dấu hiệu của sự nứt vỡ sắp xảy ra
Đau lưng nghiêm trọng trong STEMI là dấu hiệu đáng lo ngại vì nó thường là điểm đánh dấu nguy cơ vỡ sắp xảy ra. Ở đây bệnh nhân đang trong tình trạng căng thẳng trầm trọng, và có thể trở nên kích động và bồn chồn (thiếu oxy)
Có phải MI thành sau hay gây đau lưng (sau ngực)?
Chưa được chứng minh nhưng rõ ràng là có thể. (MI thành sau). Chúng tôi nhấn mạnh kết quả chuyển đạo V7 đến V10 ở MI thành sau
Vì vậy, với bệnh nhân đau ngực đặc biệt phần sau ngực cần làm ECG kiểm tra. Đây là lời khuyên cực kỳ quan trọng mà các bs vừa ra nghề cần nhớ
97. Có thể tăng JVP và phù chân ở bệnh nhân suy tim tâm trương đơn độc?
Trên thực tế, hai dấu hiệu này là tiêu chuẩn chẩn đoán suy tim theo tiêu chuẩn suy tim của Framingham. Khi các tiêu chuẩn này được xây dựng, khái niệm suy tim tâm trương không phải như hiện này. Vì vậy, chúng ta không biết liệu điều này có áp dụng cho suy tim tâm trương?
Không thể áp dụng, nhưng tại sao không ?
Chúng ta biết thì tâm trương thất trái ít có khả năng làm tăng áp lực tĩnh mạch hệ thống gây phù và tăng JVP. Tuy nhiên, những rối loạn chức năng tâm trương có thể làm tăng PCWP, PAP và RVP. Cần nhớ rối loạn chức năng tâm trương có liên quan giãn thất phải. Chúng ta cũng nên nhận ra, áp lực tĩnh mạch tăng lên không phải là cơ chế duy nhất gây phù chân. Rối loạn chức năng tâm trương có thể kích hoạt gen ACE, kích hoạt thận giữ Na. Kích thích hoạt động thần kinh nội tiết là cơ chế gây phù ở 1 số bệnh nhân, tác động nhiều đến áp lực thủy tính. Do đó phù có thể dẫn đến rối loạn tâm trương đơn độc
Vì sao rối loan chức năng tâm trương thất phải là nguyên nhân gây suy tim phải?
Cơ chế chưa rõ, hình thái và phát triển LV và RV có chung 1 nguồn cơ, chức năng tâm trương LV có thể ảnh hưởng tới RV.
Phù chân và tăng JVP là dấu hiệu của suy tim tâm thu đơn độc hoặc kết hợp suy tim tâm trương.
98. Tại sao bệnh nhân giãn cơ tim có QRS điện thế cao ở chuyển đạo trước tim và QRS điện thế thấp ở chuyển đạo chi?
Sự kết hợp của qrs điện áp thấp và qrs điện áp cao là dấu hiệu nổi tiếng của bệnh lý giãn cơ tim. Các bệnh nhân có bệnh lý cơ tim nặng thường có qrs điện áp ở v1-v6, điện áp qrs thấp ở chuyển đạo chi.
Tại sao điều này xảy ra?
Điều này xảy ra do hai lý do.
1. Chúng ta biết, chuyển đạo ngực đơn cực và cho thấy hoạt động điện ngay dưới điện cực. Trong bệnh cơ tim giãn, tim giãn ra (thường hơn 6 cm trong tâm trương, có thể lên đến 9cm) làm cho cơ tim gần ngực hơn. Điều này làm tăng hoạt động điện dưới điện cực.
2. thất trái giãn thì tâm trương và cuối tâm thu, lượng máu tăng lên làm tăng tính dẫn điện và ghi lại phức qrs điện áp cao.
Đây được gọi là hiệu ứng Brody. Hiện tượng tương tự xảy ra trong các điều kiện sinh lý như trong test gắng sức làm điện áp qrs tăng
Tại sao chuyển đạo chi không có tăng điện áp?
Chuyển đạo chi là chuyển đạo lưỡng cực, chúng ghi nhận điện áp thấp hơn chuyển đạo ngực. ở bệnh nhân giãn cơ tim, tế bào cơ bị thay bởi mô sợi làm giảm năng lượng điện dẫn truyền ra từ tế bào tim
Lưu ý: Mặc dù vậy, LV giãn vẫn ghi lại điện áp cao ở chuyển đạo ngực như giải thích ở trên
Khi nào chuyển đạo chi có thể ghi được điện áp cao trong bệnh cơ tim?
Cần phải nhận ra những khiếm khuyết dẫn truyền có thể làm tăng điện áp qrs ngoài bệnh lý của cơ tim. Điều này xảy ra do LAFB, LBBB, IVCD không đặc hiệu. Bởi vì, các bất thường dẫn truyền này rất phổ biến ở bệnh cơ tim, ít liên quan tới thể tích LV gây QRS điện áp cao.
Sự tương quan của điện áp thấp với khối lượng cơ trong LV?
Với điện áp rất thấp <5mm (qrs max) ở chuyển đạo chi dự đoán tiên lượng tồi (sẹo LV)
99. Tam giác Becmuda của thất trái
Trái tim con người là một bó cơ nặng khoảng 300-400 gram. Cung cấp máu của khối cơ này rất khác nhau. Một số khu vực được tưới máu dồi dào (ví dụ -IVS.) Một số khu vực có cấp máu cân bằng hoặc cung cấp máu kép (thường là LCX và RCA trong vùng giao nhau của tim). Một số khu vực có nguồn cung cấp máu bấp bênh. Đôi khi chúng được gọi là vùng tam giác Bermuda, dễ bị tổn thương, tạo bởi đỉnh LV, thành tự do LV và mặt trước. Đây thường là vùng đất không người ở, mỗi nhánh mạch lớn đều bỏ qua khu vực này và chối bỏ trách nhiệm của chúng.
Đây là lý do tại sao vỡ thành tự do thất và vỡ ICS là biến chứng cơ học gây tử vong hàng đầu trong STEMI
Tương tự như vậy, ngay cả trong số những người sống sót, khu vực này dễ bị giãn nở phình ra và thay đổi bất lợi. Điều này liên quan nhiều đến sự phân bố áp lực của LV (định luật Laplace).
100. Tim mạch lâm sàng: hấp hối hay đã chết?
Có thể đây là câu hỏi quan trọng nhất cho một bác sĩ tim mạch hiện đại.
Hỏi: Tim mạch lâm sàng là một chuyên khoa. . .
A. khỏe mạnh và phát triển
B. vẫn sống nhưng đang yếu
C. hấp hối
D. chết cách đây nhiều năm
Nếu câu trả lời của bạn là A, nó sẽ là một lời nói dối trắng trợn! Nếu câu trả lời là D, bạn là một người bi quan.
Câu trả lời thực sự có thể ở đâu đó giữa C và D, nhiều hơn về phía D “
Tại sao khoa tim mạch lâm sàng rơi vào tình trạng như vậy?
Tại sao nó lại trở thành vấn đề đáng lo ngại của các nhà tim mạch hiện nay? Bạn đổ lỗi cho nó về bất cứ điều gì, nhưng thủ phạm thực sự là do sự tấn công của thương mại và suy nghĩ đầy mơ mộng của nhiều bác sĩ tim mạch. trong cuộc sống này, văn hoá và di sản của quá khứ được duy trì ngoại trừ trong y học.
Bây giờ, tim mạch như là một chuyên khoa đang ở trong trạng thái đau thương. Gần như đồng nghĩa với việc đặt stent qua động mạch vành tắc nghẽn. những bs trẻ coi tim mạch như mục tiêu khi chọn nghề
Nhiều người cho rằng bệnh tim mạch nghĩa là chỉ đo HA, nhìn JVP, nhìn mạch mỏm, S1, S2…chứ không khám, sờ và đếm mạch.
Định nghĩa thế nào về tim mạch lâm sàng trong thời đại hiện tại?
Đó là quá trình áp dụng chất xám chúng ta vào triệu chứng của bệnh nhân, ảnh hưởng tới sức khỏe tổng thể và mối liên quan đặc biệt với hệ thống tim mạch. nói đơn giản hơn là lâm sàng, tính hợp lý và đạo đức
Ví dụ, một bệnh nhân sau nmct có chức năng LV bình thường, bạn nên cho về nhà và theo dõi sau này(nếu và chỉ khi có triệu chứng bất thường). Đây mới là cách điều trị đúng đắn.
Nếu bệnh nhân đó được gửi trực tiếp đến phòng can thiệp mạch, thì bạn đã đi sai đường!
Tương tự, một bệnh nhân bị rung nhĩ với đáp ứng thất nhanh, bạn nên cho dùng digoxin, chẹn beta hoặc chẹn kênh canxi để kiểm soát tần số như biện pháp đầu tiên. Nếu bạn gợi ý bệnh nhân nên đến phòng điện sinh lý EP thì bạn lại sai lầm! Nếu bệnh nhân có ASD với shunt dưới 2: 1 lại khuyên nên đặt vật liệu tốn tiền thì bạn lại sai lầm rồi.
Nếu một bệnh nhân bị hẹp động mạch thận lại xui bệnh nhân đặt stent mù quáng thì tim mạch lâm sàng sắp đến hồi tử vong
Nếu bạn chỉ định một loại sartan thế hệ mới nhất cho bệnh nhân tăng huyết áp thay vì tư vấn về chế độ tập luyện, chế độ ăn uống và thay đổi lối sống, điều đó có nghĩa là tim mạch lâm sàng đáng bị treo cổ công khai
Cuối cùng, sự nhạo báng cuối cùng của các nhà tim mạch lâm sàng, khi một bác sĩ chẩn đoán suy tim bởi BNP và CVP, ngay cả khi phổi của bệnh nhân đang rale ầm ĩ kèm theo tĩnh mạch cổ đập mạnh dữ dội.
Tệ hơn nữa, bệnh nhân này cũng có thể bị bs loại trừ chẩn đoán suy tim nếu BNP ở mức bình thường!
Khi bạn gặp một trong những tình huống trên, quá thường xuyên, thì bạn có thể dự đoán tương lai của tim mạch lâm sàng như thế nào rồi đấy.
101. Mạch sẽ thay đổi như nào ở bệnh nhân NTT thất nhịp đôi (bigeminy)?
Mạch sẽ là bao nhiêu nếu trên ECG bệnh nhân có tần số 90 (45 xoang, 45 VPDS/minute) ?
A. Chính xác như HR, nghĩa là 90l / p
B. bằng 1 nửa HR, tức là 45l/p
C. Có thể từ 45 đến 90l / p
D. Một trong những điều trên có thể đúng
Câu trả lời là D.
Lưu ý, câu hỏi đơn giản này đã gây nên nỗi lo lắng vô cùng ở các bạn sinh viên khi thi lâm sàng tim mạch
Tại sao khó trả lời câu hỏi dễ dàng này?
Trước đây, nhịp lạc vị thất gọi là ngoại tâm thu, gợi ý mỗi nhịp tim sẽ tạo ra 1 mạch ngoại vi. chúng ta gọi chúng là VPD (khử cực thất có thể có hoặc không có hoạt động cơ học) Vì vậy, ở bệnh nhân có nhịp luân phiên là VPD, mọi thứ trở nên ít phức tạp.
Điều gì quyết định VPD có khả năng gây co tâm thất hay đơn giản là sự xuất hiện của 1 hoạt động điện?
Thời điểm của VPD *.
Thể tích thất trái cuối tâm trương (LVEDV) khi bắt đầu VPD
Lực co bóp của LV (Tất nhiên, nó liên quan trực tiếp đến LVEDV) Mối quan hệ thời gian với việc mở van động mạch chủ **
Nếu VPD quá sớm hoặc quá muộn thì không thể có hoạt động cơ học. Nó nên xuất hiện giữa 2 nhịp xoang để xuất hiện hoạt động cơ học.vì vậy, ở bệnh nhân có NTT nhịp đôi thường mạch sẽ giảm 1/2. Hoặc có thể bằng tần số tim khi khoảng cách để xuất hiện hoạt động cơ học là tối ưu, cũng có thể không đều (1 số có hoạt động cơ học, 1 số thì không)
* Trong bốn yếu tố trên, thời điểm của VPDS là điều quan trọng nhất vì nó có thể ảnh hưởng đến tất cả ba yếu tố khác.
** Bất cứ điều gì ảnh hưởng đến thời gian hoặc lực co của van động mạch chủ để mở ra tạo ra mạch. Nếu vì lý do nào đó làm điều này không xảy ra có thể có hoạt động cơ học liên tục chúng ta vẫn gọi là mạch hụt
102. Khám mỏm tim
Trái tim là một trong những cơ quan độc nhất mà bác sĩ có thể chạm vào và cảm nhận trước khi chẩn đoán bệnh. Thực tế, tim nằm ở bề ngoài của khoang ngực giúp kiểm tra xúc giác. Các bác sĩ tim mạch thế hệ hiện tại nên biết sờ mỏm tim là 1 cách khám khoa học ý nghĩa rất lớn thế kỷ trước. Leannc và Dressler đã dạy hàng giờ cho sinh viên về cách khám và sờ mỏm tim.
Thật là châm biếm, khi chúng ta có thể nhìn thấy và cảm nhận nhiều vùng trong tim trực tiếp (thất phải gần xương ức, xung động mạch phổi, độ co bóp LV) thì chúng ta lại quá nghiện các thăm dò và chẩn đoán hình ảnh hiện nay
Nhìn thấy mỏm tim đập có thể không thấy ở 1/3 dân số. 2 bất thường hay gặp ở mỏm tim là tăng hoạt động và mỏm tim đập mạnh
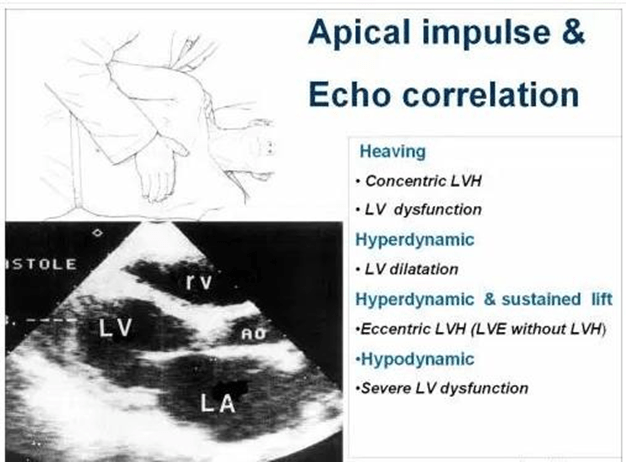
Diện đập mỏm tim tăng hoạt động
Diện đập mỏm tim lan tỏa (ít nhất 2 khoang liên sườn> 3 giây) và đập tần số nhanh có thể thấy bằng mắt thường. Điều này có nghĩa là tâm thất trái phì đại đáng kể và thành không dày nhiều. Đây là sự phì đại LV lệch tâm. Nó cũng cho chúng ta thấy chức năng LV được bảo tồn tốt vì thuật ngữ ―tăng hoạt động – hyperdynamic‖ cho thấy tình trạng LV hoạt động rất cao. Rõ ràng, LV giảm chức năng không thể hoạt động quá mức. diện đập mỏm tim tăng hoạt động ở bệnh nhân AR hoặc MR cho thấy kết quả phẫu thuật tiên lượng tốt vì lý do đơn giản chức năng LV của họ được bảo tồn. Trong cùng một logic như vậy, bệnh nhân có diện đập mỏm tim mạnh thường là dấu hiệu chức năng LV còn tốt
Lưu ý: Một bệnh nhân với diện đập mỏm tim mạnh hiếm khi thấy hồi hộp, đánh trống ngực.
Tăng hoạt động xảy ra ở tâm thu hay tâm trương?
Logic có thể nói rằng thấy rõ trong thì tâm thu. Nhưng ở giai đoạn tâm trương cũng có khi thấy được (dấu hiệu S3 kèm theo tăng hoạt động)
Mạch mỏm đập mạnh
cho thấy có nhịp LV kéo dài ít nhất 50% thì tâm thu.
– Hẹp động mạch chủ có chức năng LV bình thường
– rối loạn chức năng và giãn LV làm tăng tải sau Mạch mỏm tim không thể sờ thấy khi suy tim.
Mối quan hệ giữa mạch mỏm tim và LVH?
Hiếm khi diện đập mỏm tim tăng hoạt động lại kèm theo LVH. Ngoại trừ ở HOCM, thì tâm thu LV bị gián đoạn rất sớm trong giai đoạn tống máu.
Mỏm đập mạnh có thể là dấu hiệu của LVH.
Có thể xảy ra đồng thời tăng hoạt động và mỏm đập mạnh ở diện đập mỏm tim? Có thể xảy ra ở phình mỏm thất trái.
Thông điệp cuối cùng
Việc khám và sờ mỏm tim thời nay có thể bị coi là công việc ngu ngốc Ngày nay là hỏi tiền sử, làm ECG, siêu âm tim và đẩy lên cathlab sớm nhất. Nhưng hãy nhớ, có những cái kì diệu vẫn còn hiện hữu đến ngày nay
103. Tại sao thông liên thất (VSD), 1 số đóng lại còn 1 số thì không?
Thông liên thất (VSD) là một trong những bệnh tim bẩm sinh hay gặp nhất.. 60% tất cả các VSDs nhỏ sẽ đóng vào năm 10 tuổi.
Vì vậy, chúng ta nên làm gì khi trẻ được chẩn đoán VSD? Chúng ta nên đóng hay nên chờ đợi?
Chỉ định đóng VSD được bàn ở bài khác Các yếu tố quyết định đóng VSD là gì? Kích thước
Vị trí
Tuổi của trẻ Hình thái của bờ
Tổn thương liên quan * Huyết động
Các yếu tố mô liên kết Nhiễm trùng **
* Các bất thường kèm theo như PDA, tắc nghẽn RVOT làm ngăn đóng VSD tự phát
Các quy tắc chung về đóng VSD Kích thước
VSD <5mm có cơ hội tự đóng, VSD> 1cm hiếm khi tự đóng.
VSD nằm bên dưới động mạch không thể đóng tự phát dù kích thước nhỏ
Vị trí
VSDs nằm trong lớp vách màng hiếm khi tự đóng. Lớp cơ VSD nếu lớn không thể tự đóng
Hình dáng bờ VSD
Các cơ VSDs nhỏ có khả năng đóng lại
Quá trình tăng trưởng mô khi đứa trẻ lớn lên, người ta mong đợi tim sẽ lớn hơn tổn thương. Đây được coi là phương thức phổ biến nhất của việc đóng lại VSD.
** Vai trò của nhiễm khuẩn
Viêm nội tâm mạc nhiễm khuẩn gần VSD đẩy nhanh quá trình làm phẳng mô và liền VSD
Mối quan hệ với tăng ápđộng mạch phổi (PAH)?
Một khi có PAH thì VSD không bao giờ đóng. Điều này do VSD là hậu quả PAH đặt vào VSD không bao giờ được đóng tự phát, Điều này có thể là do tất cả các VSDs làm tăng PAH đáng kể
Tại sao một số VSDs không bao giờ đóng lại?
Rõ ràng, kích thước và vị trí VSD là quan trọng nhất, nhưng có một vài vấn đề khác có thể tác động tới quá trình đóng VSD
104. Điều gì sẽ xảy ra với cường độ tiếng S1 của tim ở bệnh nhân rung nhĩ?
Đây là một dấu hiệu cảnh báo nổi tiếng trong tim mạch, S 1 trở nên biến đổi về cường độ khi bắt đầu rung nhĩ.
Trong sinh lý học, cường độ của S 1 được xác định bởi nhiều yếu tố.
1. Hình thái van (Độ dày, vôi hóa, Độ cứng)
2. Độ di động của van
3. Khoảng PR
4. Lực co LV
5. Khoảng RR (4 và 5 liên quan đến nhau)
6. Các yếu tố ảnh hưởng đến nghe tim (thành ngực dày …)
Làm thế nào rung nhĩ gây thay đổi cường độ của S1?
Cần lưu ý, rung nhĩ làm thay đổi chỉ một trong những yếu tố trên, tức là khoảng thời gian RR trở nên không đều.
Sự kết hợp giữa các khoảng RR ngắn và dài xảy ra ngẫu nhiên. Khoảng cách RR ngắn, làm tiếng S1 tương đối nhẹ và ngược lại. Cơ chế này có liên quan trực tiếp đến mức độ co của LV và sự thay đổi lực co LV
Nếu khoảng RR quá dài, có thể có mối quan hệ nghịch với cường độ s1. Vì khi đó van 2 lá đã đóng 1 phần hoặc hoàn toàn, làm lực co LV không liên quan tới sự hình thành S1, thậm chí không nghe thấy tiếng S1
105. Lí do mất khoảng PR trong rung nhĩ?
Không quá khó hiểu vì nếu không có sóng P thì PR cũng không thể xuất hiện Nếu không có khoảng PR, có thể không ảnh hưởng đối với tiếng tim đầu tiên. 2 type biến đổi cường độ tiếng S1?
Kinh nghiệm cho thấy có 2 loại *.
Trình tự 1: Thay đổi theo dạng: to- to hơn- to nhất Trình tự 2: Thay đổi theo dạng: to- bình thường- nhỏ
* Chỉ áp dụng đối với những người nghe tim tốt
Cường độ S1 có liên quan tới bệnh lý nên: rung nhĩ có bệnh van tim và không có bệnh van tim
Rõ ràng sự thay đổi khoảng RR với thay đổi cường độ S1 sẽ trực tiếp phụ thuộc vào bệnh lý nền. Cường độ của S1 trong AF không tổn thương van động mạch (như AF đơn thuần, nhiễm độc tuyến giáp + AF, giảm oxy máu +AF, thiếu máu cục bộ + AF …) dễ bị thay đổi khoảng RR hơn.
Trong bệnh thấp tim, ảnh hưởng của hình thái van, độ cứng, vôi hóa và sự có mặt của MR thường chiếm ưu thế hơn so với việc ảnh hưởng của thay đổi khoảng RR. Vì vậy, trong trường hợp hẹp ha lá và AF hay gặp thay đổi cường độ S1 theo type 1
Trong AF hoặc AF đơn thuần do CAD, type 2 có nhiều khả năng hơn * kết hợp rối loạn chức năng LV và thiếu máu cục bộ có thể làm giảm cường độ tiếng S1
Ý nghĩa lâm sàng
Nghe thấy tiếng S1 lớn ở bệnh nhân AF là dấu hiệu gián tiếp cho thấy chức năng LV cơ bản còn rất tốt vì nó cho thấy lực co LV còn mạnh
106. Clopidogrel – Sự vinh danh bịp bợm
Điều buồn cười trong y học là, câu hỏi càng đơn giản thì càng khó trả lời! Clopidogrel là một thuốc chống ngưng tập tiểu cầu không thể đảo ngược. Có lẽ nó là một trong những loại thuốc tim mạch hàng đầu được sử dụng hiện nay, nó đã trở thành cứu tinh của loài người và cũng chính nó đã muốn giết aspirin và thất bại thảm hại. Hiện nay nó đóng gói cùng aspirin- khái niệm kháng tiểu cầu kép là ví dụ điển hình. Thực tế, Clopidogrel hiếm khi sử dụng thành công trong vai trò tác nhân chống ngưng tập tiểu cầu trong khi Aspirin lại có thể thực hiện xuất sắc vai trò này.
Bạn có biết, loại thuốc này được coi là một loại thuốc chống ngưng tập tiểu cầu tuyệt vời, thậm chí nó không thể vượt qua thử nghiệm cơ bản để kéo dài thời gian chảy máu?
Tuy nhiên, không rõ tại sao nó lại không làm tăng thời gian chảy máu khi quan sát trên bệnh nhân – chúng tôi đã xác nhận điều này bằng các test bên cạnh giường bệnh nhân (rút ra những kết luận có tính thuyết phục hơn những nghiên cứu mù đôi). Ở nhiều bệnh nhân dùng 300 mg clopidogrel không kéo dài thời gian chảy máu thậm chí chỉ vài giây!
Nếu clopidgorel không thể kéo dài thời gian chảy máu, dùng nó có nguy hiểm không? Đối với hàng triệu bệnh nhân DES (đặt stent phủ thuốc – drug eluting stents), tỷ lệ sống sót ở những người này thay đổi thất thường
Cộng đồng tim mạch không bao giờ bị sốc, ngay cả trong thời đại y học thực chứng, 1 loại thuốc được sử dụng hơn 17 năm nay lại không có chiến lược giám sát cơ bản nào về hiệu quả của nó
Không có gì đáng ngạc nhiên khi thấy một lượng lớn bệnh nhân DES vào cấp cứu vì huyết khối cấp do dùng clopidogrel thất bại hoặc kháng clopidogrel.
Đọc nghiên cứu dưới đây được xuất bản bởi 1 trong những tạp chí tim mạch có uy tín và hiểu tranh cãi về clopidogrel https://www.ncbi.nlm.nih.gov/pubmed/15019671

Thông điệp cuối cùng
Việc sử dụng và tung hô Clopidogrel đang làm tăng chi phí điều trị tim mạch cho dân số nói chung. Quá tốn kém và không chắc đã tốt tương đương với Aspirin đã cho thấy những vấn đề khó tả của nền y học hiện đại.
Không có gì nghi ngờ khi nó sẽ phải đối mặt với số phận tương tự như Ticlopidine, Prasugrel!
“The easiest job to do in this wold is to fooling around the public and it is an irony medical professionals and their patients are often the victims”
107. Digoxin có biết, tâm thất nào cho nó hoạt động ở bệnh tim do phổi (cor-pulmonale)?
Digoxin là một loại thuốc tim mạch kỳ lạ được sử dụng trong hơn một thế kỷ qua.
Cơ chế tác dụng
Tác dụng có lợi của Digoxin là do
Co cơ dương tính Tác dụng phế vị
Digoxin chặn kênh Na-K-ATPase ở màng tế bào cơ
Điều này gây ra tích tụ các ion Na + bên trong các tế bào. Sự vượt quá nồng độ Na, tạo thuận lợi cho trao đổi Na-Ca.
Nó sẽ giúp bơm nhiều canxi hơn vào tế bào cơ.
Tăng canxi có nghĩa là sự co thắt mạnh mẽ hơn và đó là tính co cơ tích cực (dương tính) Đây là mô hình đơn giản hóa tác dụng của digoxin. Nên nhớ sự dư thừa canxi đơn thuần không thể đảm bảo sự co bóp vì nó đòi hỏi các thụ thể cũng phải đầy đủ
Digoxin được sử dụng trong loại suy tim nào?
Digoxin được sử dụng cho cả suy thất trái và suy 2 thất
Digoxin vẫn thường dùng cho suy thất phải vì bất kỳ nguyên nhân nào (bệnh tim do phổi, PPH, Eisenmenger vv)
Rối loạn digoxin và RV?
Digoxin có khuynh hướng tác động lên cơ tâm nhĩ gây ra các vòng vào lại nhỏ để quay về nhịp nút xoang sau các rối loạn nhịp nhĩ phức tạp như MAT.
Nó có gây co cơ RV?
RV là một máy bơm thụ động. Nhưng không có nghĩa là co cơ là đặc tính đặc trưng chỉ của LV.
RV phải tạo ra áp lực khoảng 30mmhg để bơm máu vào phổi.
Trong bệnh tim do phổi, RV phải hoạt động chống lại hậu tải khoảng 50-70 mmhg, làm cho khái niệm co cơ RV quan trọng hơn nhiều. Kiểm soát tần số ở bệnh nhân rung nhĩ, Digoxin làm giảm tần số tim bằng tác động phế vị, chủ yếu ở nút AV và ở mức độ nào đó với nút SA. Giảm tần số thất là mục tiêu chính trong điều trị rung nhĩ và vinh quang này vẫn thuộc về Digoxin
Mặc dù thuốc chẹn beta và verapamil có thể được sử dụng như tác nhân kiểm soát tần số, nhưng có lực co cơ âm làm digoxin chiếm ưu thế, đặc biệt là ở bệnh nhân rối loạn chức năng thất nghiêm trọng.
Tuy nhiên, một trong những bất lợi của Digoxin, ít hiệu quả khi giao cảm bị kích thích như khi gắng sức
Tác dụng của digoxin đối với sự co vách tâm thất?
Digoxin, đơn giản là không biết nó tác dụng ở đâu khi dùng cho bệnh nhân có bệnh tim do phổi! theo logic sẽ rối loạn thất trái.
Một số người tin rằng cải thiện rối loạn chức năng thất trái ở bệnh tim do phổi quan trọng hơn việc làm giảm triệu chứng của bệnh nhân
Các thuốc khác làm co RV là gì?
Doubtamine có gây co cơ RV. Điều này có thể do hiệu ứng từ LV chứ không phải do kích thích RV
Có lẽ cách tốt nhất để cứu RV là làm giảm áp lực động mạch phổi (Nitric Oxide, Epo prostenol vv)
Thông điệp cuối cùng
Digoxin, thực sự có vai trò hữu ích trong bệnh tim do phổi.
Tuy nhiên, lợi ích rõ ràng hơn trong suy thất phải RV giai đoạn cuối
Vì có khuynh hướng gây loạn nhịp tim phức tạp, nên thận trọng khi điều trị rung nhĩ do bệnh tim do phổi (hơn ở các dạng AF khác)
108. Cơ chế gây tím tái ở bệnh nhân có tăng áp động mạch phổi nguyên phát?
Tím trung ương xảy ra ở bệnh nhân tăng áp động mạch phổi nguyên phát (PPH) như nào?
Trong khi, chứng tím tái ngoại biên giải thích dễ dàng trong PPH *, thì cơ chế của tím trung ương không phải dễ dàng.
Những giải thích sau đây được chấp nhận
1. PFO ** mở ra do áp lực RA trung bình cao
2. Kênh tĩnh mạch- động mạch phổi (tân tạo hoặc các kênh không hoạt động được kích hoạt)
3. Thay đổi QP / QS. Điều này có nghĩa là shunt ở phổi chứa 1 số máu không được oxy hóa (shunt từ phải sang trái trong phổi)
4. Bệnh liên quan đến bệnh lý phổi – như viêm phổi dẫn đến shunt phổi phải-trái qua tuần hoàn phế nang.
*Tím ngoại vi có thể xảy ra trong PPH với suy tim
** PFOs gặp ở 20% dân số, hoạt động khi áp lực RV cao
Tím tái – mô tả thoáng qua
Tím tái xảy ra khi độ bão hòa oxy máu động mạch xuống dưới 85%. Tím tái biểu hiện theo hai cách. Trung ương và ngoại vi. Thuật ngữ ngoại vi gợi ý các bộ phận ngoại vi của cơ thể chứ không phải là tuần hoàn ngoại biên. Cơ chế tím ngoại vi có khác với tím trung tâm. Nói chung là do lưu thông chậm chạp, dùng oxy nhiều hơn và gây tím tái
tím ở ngoại vi thấy ở đầu ngón tay, môi, vv tím ngoại vi không thể xảy ra ở khu vực nhiều nhiệt của cơ thể vì vùng này gây giãn mạch, lưu thông mô tốt hơn để ngăn ứ trệ máu bị oxy hóa
Thiếu oxy máu trung ương không thể dẫn đến tím trung ương
Đối với tím trung ương, phải trộn máu khử oxy và oxy hóa ở nơi nào đó trong hệ tuần hoàn (shunt phải-trái trong tim hoặc phải)
Vì nó là bất thường trong quá trình oxy hóa trung ương nên nó gây tím niêm mạc cũng như gây đầu chi lạnh
109. Các câu hỏi về LBBB
Tại sao phức hợp qrs rộng và cao trong LBBB?
QRS rộng do chậm dẫn truyền ở các sợi không đặc hiệu. QRS cao do phân ly thời gian RV và LV, mà lực co LV không bị cản trở nên QRS cao, không có tác dụng đối lập của lực co RV
Đặc trưng của LBBB?
Mặc dù bó trái bị chặn, nhưng phần lớn dẫn truyền vẫn xảy ra qua các sợi đặc hiệu. Nó phụ thuộc vào mức độ LBBB.
Cơ chế và ý nghĩa lâm sàng của trục trái trong LBBB đơn thuần là gì?
Trục qrs đáng ngạc nhiên là không thay đổi nhiều trong LBBB. Nếu có xu hướng trái gợi ý cho ta bệnh liên quan LV hoặc Lafb
Tác động của thời gian và lực co IVS với LBBB?
Trong LBBB đơn thuần, người ta mong đợi sẽ có chuyển động bất thường của vách liên thất. nếu có chuyển động rõ ràng chứng tỏ chức năng LV còn tốt. không thấy hình ảnh này cho thấy LBBB do bệnh tim cấu trúc
Tại sao chuyển động bất thường của vách liên thất lại không gặp trong LV bình thường?
CRT là cách điều trị thú vị ở bệnh nhân bị LBBB và suy tim. ở bệnh nhân có chức năng LV bình thường, LBBB không làm mất ổn định chức năng LV mặc dù mất đồng bộ chuyển động của vách liên thất.
Những bất lợi cơ học của LBBB
Sự co lại của vách liên thất không đúng thời điểm Trào ngược van 2 lá
Hầu hết các LBBBs mạn tính không ảnh hưởng tới huyết động với LV- tại sao?
LBBB nguy hiểm trên ECG, nhưng đa số với các bệnh nhân nó đều lành tính trừ khi có kèm bệnh cấu trúc tim như thiếu máu cục bộ, bệnh cơ tim hoặc bệnh van tim
Có thể có sóng r nhỏ ở V1 và V2 trong LBBB?
Có thể . Mặc dù chúng tôi hy vọng sự khử cực vách sẽ làm mất r ở V1 đến V3. Do đó sự hiện diện của r nhỏ ở v1 đến v3 không loại trừ LBBB.
Giải thích hay gặp nhất là do lực co RV bị che lấp bởi lực co LV đến sớm
Một khả năng khác là sự di động của vách liên thất trong các trường hợp bệnh lý
Khả năng thứ ba là “r” có thể thực sự đặc trưng cho sự xuất hiện sóng q như trong LVH hoặc AWMI cũ (sóng q nhỏ ở chuyển đạo bên)
Làm thế nào giải thích dạng QRS phù hợp (concordant) ở V1 đến V6 trong LBBB?
Chúng ta hy vọng qrs chuyển từ dạng QS sang RS, ít nhất ở v5 / v6. Một số trường hợp thậm chí V6 có dạng RS. Điều này thường là do vị trí bị thay đổi hoặc LV tăng rõ rệt, nếu ta ghi V7 hoặc V8 sẽ có thể lại thấy dạng QS
Hình thái học của ECG có VPD phát sinh từ LV khi có LBBB?
Xuất hiện nhịp ngoại tâm thu từ thất ở bệnh nhân có block nhánh đúng là hạnh phúc trời cho. VPD thường xuyên làm mất block nhánh và giúp dẫn truyền gần như bình thường và khi đó ecg ghi nhận được QRS như bình thường. Vì vậy, khi một bệnh nhân có LBBB bất ngờ tiến triển thành QRs bình thường hoặc nhịp nhanh có QRS bình thường thì phải nghĩ tới VT nguồn gốc từ thất trái
Và nghiên cứu điện sinh lý đã trả lời các câu hỏi dưới đây!
Hình thái ECG có VPD nếu nó phát sinh từ RV và vách liên thất trong trường hợp có LBBB?
Kindwall đã cố gắngtrả lời câu hỏi này Tác động của LBBB trên S1 và S2? Mô tả cổ điển trong LBBB là
S2 chia đôi S1 rộng
Bạn sẽ nghe thấy 4 thành phần trong LBBB hoàn toàn! Trong thực tế điều này không xảy ra. Tốt nhất bạn có thể nghe thấy tiếng S2 tách đôi nhưng hơi bị khó
Một lý do khác cho việc không nghe thấy 4 thành phần do nhiều yếu tố nhiễu như rối loạn chức năng LV, MR, khoảng PR vv (mỗi yếu tố này có xu hướng kéo hoặc đẩy S1 S2 theo các hướng khác nhau)
Bệnh nhân có LBBB, có nguy cơ tiến triển thành block tim hoàn toàn khi dùng Beta blockers, thuốc chẹn kênh canxi?
Có thể có nhưng hiện chưa có câu trả lời.
Chúng ta biết, tâm thất được dẫn truyền bởi 2 bó. Khi chỉ 1 bó có chức năng, nó có nghĩa là các tâm thất đang bị tắt nguồn 50%. Trong CAD, chỉ 1 mạch máu cấp máu do CTO được coi là nguy hiểm nhưng với dẫn truyền điện thế thì không phải vậy. Mặc dù thực tế là tâm thất có nhiều tế bào dẫn truyền điện thế nhưng nên luôn cẩn thận khi dùng các thuốc chẹn beta, chẹn kênh canxi và digoxin ở bệnh nhân LBBB. không bao giờ được sử dụng thuốc chẹn beta ở bệnh nhân mới khởi phát LBBB và ACS
110. Thử nghiệm SHIFT: Ivabradine vẫn tỏa sáng trong thời kỳ huy hoàng của beta blocker?
Bây giờ chúng ta hiểu, giảm nhịp tim có thể là yếu tố quan trọng nhất trong việc điều trị suy tim. Các thuốc chẹn beta đã chứng minh được điều này. Chúng ta biết rằng nhịp tim có mối quan hệ tuyến tính với sự sống còn.
Thử nghiệm SHIFT đã chứng minh rằng Ivabradine có vai trò chính trong việc điều trị chứng suy tim mạn tính. Không có phản ứng phụ về huyết động học.
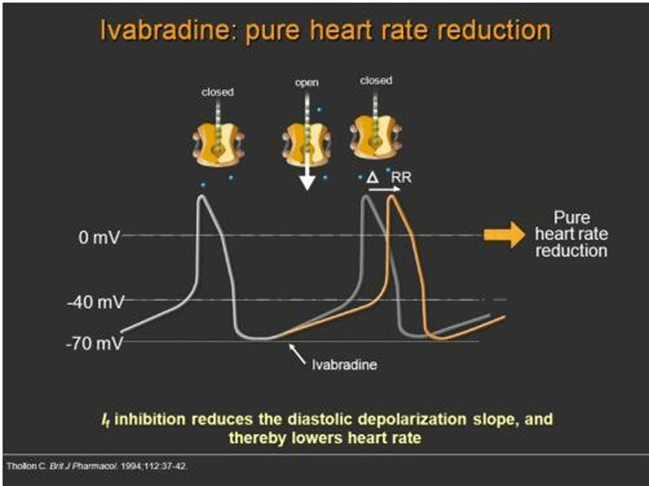
Ivabradine hoạt động như thế nào?
Nó hoạt động ở giai đoạn 4 quá trình khử cực tâm trương ở nút SA
http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(10)61198- 1/fulltext#article_upsell
http://www.shift-study.com/?
Trong thử nghiệm này, việc sử dụng thuốc chẹn beta tối ưu chỉ ở mức 25%. Bệnh nhân đã được điều trị beta blocker cho thấy có nhiều lợi ích khi dùng với Ivabradine. Hơn nữa, việc sử dụng digoxin chỉ khoảng 20% số bệnh nhân
Chúng ta cần một nghiên cứu như thế này.
So sánh một lần giữa beta blocker và Ivabradine trong điều trị suy tim. Một nghiên cứu như vậy sẽ bao giờ xảy ra? Tôi đoán là không thể!
Hiệu quả tuyệt vời của Ivabradine ở những bệnh nhân suy thất độ 4, khi không thể dùng beta blocker
Ivabradine, một thuốc điều nhịp thế hệ mới là một loại thuốc tuyệt vời. Nhưng, hào quang của thuốc này bị beta blocker làm lu mờ vì người ta chứng minh thuốc dung nạp tốt là thuốc chẹn beta để làm giảm nhịp tim. Tuy nhiên, nếu đáp ứng kém với thuốc chẹn beta, thì có thể dùng thử ivabradine. Đó là loại thuốc duy nhất có tính chất co cơ dương tính kết hợp với hoạt động điều nhịp âm tính. Cả hai lợi ích này rất cần với bệnh nhân CHF. Nó kì diệu hơn bất kỳ loại thuốc nào khác (thử nghiệm DIG là sự hiểu nhầm đáng tiếc nhất của các bác sĩ tim mạch!) ‘
111. Làm thế nào xử trí block AV hoàn toàn khi mang thai?
Đối với người dân, thuật ngữ block tim hoàn toàn (CHB) thường truyền tải một thông điệp nguy hiểm. Khi gặp trong thời kỳ mang thai, nó cũng đáng sợ đối với các bác sĩ. Không cần phải nói. . các bác sĩ sản khoa sẽ lo lắng như thế nào!
Block tim hoàn toàn bẩm sinh thường là nguyên nhân hay gặp, dù có nhiều nguyên nhân có thể gây CHB nhưng hiếm khi thiếu máu cục bộ hay block ở bệnh nhân ở độ tuổi sinh đẻ
CHB xuất hiện như nào?
– Triệu chứng CHB phát hiện lần đầu tiên trong quá trình sàng lọc trước sinh
– CHB không triệu chứng được phát hiện bất ngờ trên monitor khi sinh
– CHB lần đầu tiên được phát hiện trong thời gian chuyển dạ. Hoặc là có triệu chứng / Không triệu chứng
Một tình huống quen thuộc hơn là CHB được chẩn đoán từ hồi còn nhỏ.
* Sự thành công của y học hiện đại nằm trong thần chú “chẩn đoán sớm”. Ngay lập tức, phát hiện sớm CHB trong thai kỳ làm tăng thêm lo lắng cho mẹ, gia đình và bác sĩ điều trị. 99/100 trường hợp CHB sẽ không cần bất kỳ can thiệp nào trong thời gian mang thai. Chúng tôi đã từng chứng kiến CHB ở sản phụ sinh thường ở phòng cấp cứu với nhịp tim tần số 45
Trường hợp block AV hoàn toàn bẩm sinh nào là bệnh lý?
Nó thường là do sự gián đoạn giải phẫu của nút AV và bó His. Điều may mắn nhất ở đây là, những bệnh nhân này sẽ xuất hiện nhịp thoát bộ nối khoẳng 40-45l/p. Điều này là đủ cho hầu hết các hoạt động cơ bản. Hơn nữa, tần số này có thể tăng lên đến 100 ở nhiều người, thậm chi lên tới 120l/p khi căng thẳng. có thể tăng lên đến 100 ở nhiều người, thậm chí lên tới 120 lần khi căng thẳng (nhịp điệu liên kết gia tăng) * Một ECG có phức hợp qrs hẹp gần 100% đặc trưng cho nhịp thoát bộ nối ổn định.
Stress huyết động trong thai kỳ là gì? Liệu nhịp tim 50 / p có đủ để hỗ trợ cho chuyển dạ hay mổ lấy thai?
Tự nhiên có tính cân bằng tuyệt vời. Điều mà người mẹ mang thai đòi hỏi là cung lượng tim tốt để nuối dưỡng em bé cũng như bản thân mình. Tần số 50 thường có thể duy trì và hỗ trợ toàn bộ quá trình thai kỳ 1 cách dễ dàng
Nó sẽ thực hiện chức năng như nào?
Trong thai kỳ, có ít phản ứng mạch máu do các nguyên nhân khác nhau (sự tuần hoàn nhau thai trở kháng thấp, giảm nhạy cảm với Angiotensin 2). Trái tim luôn có thể tăng cung lượng tim bằng cách tăng nhịp tim hoặc thể tích nhát bóp. Ở bệnh nhân CHB, vì tần số không thể tăng nhiều, trái tim chấp nhận lựa chọn thay thế thứ 2. Tỷ lệ SVR thấp cũng giúp tăng thể tích nhát bóp. Đây là lý do khiến việc mang thai thường phát triển tốt thậm chí với nhịp tim <50 /p.
Dấu hiệu và triệu chứng đáng lo ngại của CHB trong thai kỳ là gì?
Sau khi thảo luận rất nhiều về bản chất lành tính của CHB bẩm sinh, người ta cần phải nhận ra nó cũng là rối loạn nhịp tim nguy hiểm tiềm ẩn. Ngất xỉu, hạ huyết áp (BP <90) và một số dấu hiệu PIH, tất cả đều có thể chỉ ra cần phải đặt máy tạo nhịp hỗ trợ
Chúng ta có thể làm test gắng sức đánh giá khả năng điều nhịp trong thai kỳ?
Nói chung không nên làm trong thai kỳ. Nếu nhịp tim tăng lên 100-120 thì đó là phản ứng tốt
Nên mắc holter?
có thể chấp nhận theo dõi 24h để đánh giá tần số thấp và cao nhất. nếu có khoảng nghỉ kéo dài > 5s thì cần đặt tạo nhịp vĩnh viễn.
Test atropine?
Đây là một test đơn giản, nó sẽ đo khả năng điều nhịp.
Một bệnh nhân CHB bẩm sinh không nên khuyên không được mang thai
Chỉ có vấn đề là chúng ta phải chắc chắn rằng, phải có chiến lược dự phòng huyết động đầy đủ. Điều này có thể dễ dàng thực hiện bằng cách hỏi một số câu hỏi cơ bản về năng lực vận động. Hoặc, có thể cho test gắng sức (hoặc test atropine). Nếu nhịp tim lên tới 100l/p thì không cần đặt máy tạo nhịp vĩnh viễn
Các vấn đề đặc biệt ở phụ nữ mang thai có máy tạo nhịp tim vĩnh viễn
Nghịch lý của y học hiện đại thấy rõ nhất là ở đây!
Chúng ta nghĩ rằng, chúng ta đặt máy điều hòa nhịp trong CHB để hỗ trợ huyết động tốt trong thời kỳ mang thai. Lý do đặt máy tạo nhịp chủ yếu là tránh nguy cơ nhịp chậm trong quá trình chuyển dạ
Do đó, bệnh nhân có CHB có stress trong thời gian chuyển dạ khi máy tạo nhịp cố định ở tần số 70 và nhịp của bệnh nhân không vượt quá tần số máy tạo nhịp là 70l/p. Nghịch lý là nếu bệnh nhân CHB không đặt máy tạo nhịp có thể tăng tần số tim lên 100-120 ở thời điểm gắng sức. Điều này có thể do nút AV của họ vẫn nằm dưới sự kiểm soát của hệ thống tự động trong khi với các máy tạo nhịp thì không phải vậy!
* Một số máy tạo nhịp hiện tại đã khắc phục vấn đề này bằng tốc độ thích nghi.
Vai trò của bác sĩ tim mạch trong phòng sinh?
Vai trò của bác sĩ tim mạch là hỗ trợ bs sản khoa và đặt máy tạo nhịp tạm thời để tần số quay lại ưu tiên 50l/p là lý tưởng.
Vai trò của tạo nhịp qua da tạm thời?
Phương pháp này với hai điện cực dính ở thành ngực và tạo nhịp bên ngoài. Tuy nhiên, đây có thể là sự thay thế tốt trong vài giờ, có thể gây khó chịu cho bệnh nhân
Máy tạo nhịp tạm thời có thể thích ứng bằng tăng tần số không? Các máy tạo nhịp tim tạm thời hiện nay không thích ứng với tần số Các vấn đề về gây tê trong mổ lấy thai ở bệnh nhân CHB?
Các bác sĩ gây mê đang lo lắng điều này. Nên có bác sĩ tim mạch kèm theo máy tạo nhịp tim tạm thời.
Nhiều loại thuốc gây mê có ảnh hưởng bất lợi đến nhịp tim. Thuốc tránh dùng là Fentanyl, suxamethonium, neostigmine, propofol có nguy cơ làm nhịp chậm nặng hơn. Nên gây tê ngoài màng cứng có kiểm soát để đảm bảo gây tê khởi phát chậm và giữ ổn định huyết động, Bupivacaine gây giảm nhịp tim (thậm chí ngay cả trong gây tê ngoài màng cứng)
Mẹ CHB có ảnh hưởng tới huyết động của thai nhi không?
Không hoặc gần như không (quá ngạc nhiên)
Các vấn đề trong giai đoạn sau sinh?
Giai đoạn sau sinh nên để máy tạo nhịp tạm thời trong 48h, hiếm khi cần máy tạo nhịp vĩnh viễn
112. Thuốc vận mạch nào tốt nhất trong sốc? Dopamine hay norepinephrine?
Thuốc vận mạch là thuốc chính trong điều trị sốc. Tất nhiên còn tùy thuộc vào nguyên nhân gây sốc, nhưng các thuốc này có vai trò quan trọng trong cứu sống và phục hồi chức năng các cơ quan
Các bác sĩ trên toàn thế giới, tỷ lệ dùng 2 thuốc này ngang nhau
Đáng ngạc nhiên là không có một thử nghiệm so sánh nào về 2 thuốc này cho đến năm 2010. Nghiên cứu SOAP 2 xuất bản từ Brussels, Bỉ. Nó so sánh việc sử dụng hai loại
thuốc này với nhiều hội chứng sốc. Nó cũng ủng hộ sử dụng Norepinephrine, kể cả trong sốc tim

Những bất lợi của dopamine được lưu ý trong thử nghiệm này là Tăng nguy cơ loạn nhịp tim
Tăng tỷ lệ tử vong do sốc tim
Ý nghĩa của thử nghiệm này có thể buộc các hướng dẫn của ACC / AHA, vốn khuyên rằng dopamine là lựa chọn đầu tiên trong các hội chứng sốc, đặc biệt là nguyên nhân tim mạch cần phải xem lại
113. Albumin bị biến đổi trong thiếu máu cục bộ – khái niệm mới trong chẩn đoán nhanh thiếu máu cục bộ tim?
Trong chẩn đoán ACS, chúng ta có các dấu hiệu sinh học rõ ràng trong nmct cấp tính. Hơn nữa, ECG cũng nhạy cho STEMI. Trong khi dấu hiệu lâm sàng và ECG của thiếu máu cục bộ lại không được vậy. Chất chỉ điểm sinh học cho thiếu máu cục bộ là ước mơ cả các nhà tim mạch và bác sĩ cấp cứu. Trong hoàn cảnh này, Albumin biến thể do thiếu máu cục bộ (IMA) được kỳ vọng rất cao
Thiếu máu cục bộ làm biến đổi albumin như nào?
Bình thường phân tử Albumin có vài vị trí tự do liên kết với kim loại (đồng). Trong lúc thiếu máu, khả năng ràng buộc kim loại này giảm. sử dụng coban bổ sung vào
máu khi có thiếu máu thấy các vị trí liên kết này thừa nhiều liên kết tự do, cobalt sẽ gắn và làm đổi màu mẫu giúp chẩn đoán thiếu máu cục bộ
* Albumin người bình thường có thể chứa 2% albumin biến thể do thiếu máu cục bộ (IMA) và dự kiến sẽ tăng lên đến 6% trong thời gian thiếu máu cục bộ
IMA tăng không chỉ trong thời gian thiếu máu mà nó cũng có thể tăng lên trong đột quỵ, bệnh thận mãn tính, bêṇ h gan, bệnh ác tính
Nó cũng có thể tăng sau chụp mạch vành, PCI, sốc điện, tăng acid lactic
IMA có thể giúp xác định thiếu máu cục bộ sớm. Tuy nhiên, độ nhạy không cao

http://emj.bmj.com/content/23/10/764

http://circ.ahajournals.org/content/107/19/2403.full
114. Loại thuốc bí ẩn mang tên Ranalozine
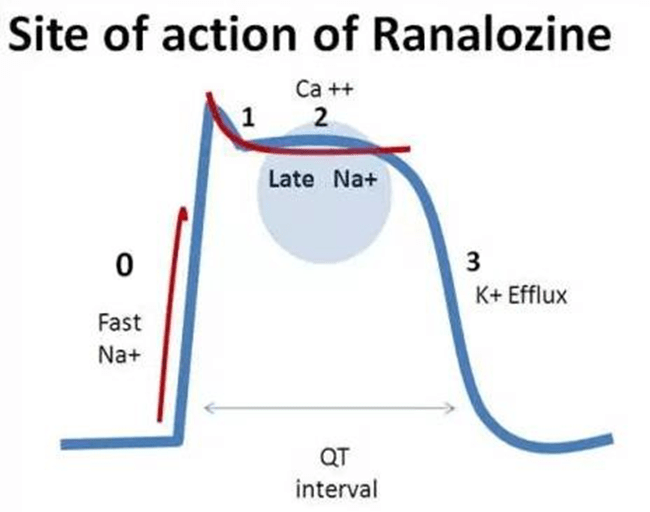
Về cơ bản, khi thế giới đang tìm kiếm một loại thuốc chống đau thắt ngực mà không có nhiều tác động lên huyết động. Trimetazidine đã chiếm ngay vị trí này. Trong khi nó dùng phổ biến ở Châu Âu và Nhật Bản, người Mỹ có nhu cầu về loại thuốc tương tự. do đó Ranalozine được sinh ra
Ranalozine hoạt động như thế nào?
Có ba tác dụng quan trọng của Ranalozine (tác dụng thứ 4 là một bất ngờ)
1. Chống đau ngực
2. Chống loạn nhịp
3. Có thể có hiệu ứng lusiotropic
4. Chống tiểu đường *
* Thật ngạc nhiên khi thấy Ranalozine làm giảm Hb A1c. Điều này là ngẫu nhiên hoặc 1 câu chuyện cổ tích mà chúng ta không biết!
Chống đau thắt ngực
Nó hoạt động trên kênh ion Na cuối phase 2 của điện thế hoạt động
Điều này tạo điều kiện cho Ca dư thừa sẽ được lấy ra khỏi tế bào qua trao đổi Na/Ca Calcium đi ra cải thiện trao đổi chất vùng cơ bị thiếu máu do thiếu máu cục bộ
Điều này làm cho loại thuốc này có hiệu quả chống đau thắt ngực
Chống loạn nhịp
Một loại thuốc, chẹn kênh Na ở phase 2 không có gì đáng ngạc nhiên khi nó có tác dụng chống loạn nhịp
Nó có thể làm giảm vòng vào lại phase 2 như EADS
Tác dụng chống loạn nhịp
Bằng cách chẹn kênh Na kéo dài phase 2 nên QT bị kéo dài
Tác dụng điều nhịp, thư giãn cơ tim (lusitropic)
Bằng cách ngăn ngừa canxi tích lũy từ cytosol nên nó có tác dụng điều nhịp
Lợi thế chính của thuốc Ranalozine so với các loại thuốc khác là gì?
Nó hầu như không ảnh hưởng huyết động
Không giống như các thuốc chống loạn nhịp khác, nó chỉ hoạt động khi có rối loạn hoạt động kênh Na
(Đó là trường hợp trong giai đoạn thiếu máu.) Điều này ngăn ngừa khoảng QT kéo dài ở người bình thường
Mặc dù tác dụng tốt vô cùng và ít phản ứng phụ, nhưng tại sao FDA và các bác sĩ tim mạch vẫn không lựa chọn nó?
Tôi không biết câu trả lời cho câu hỏi này, nhưng tôi chia sẻ cảm giác của tôi về nó cho các bạn.
Trong bối cảnh này, tôi nhớ lại một tuyên bố nổi tiếng của 1 giáo sư “Một loại thuốc có ít tác dụng phụ nhất thì nó cũng sẽ không thể có được tác dụng mong muốn”
Nhưng với thế giới hiện tại, sự thành công của 1 loại thuốc không phụ thuộc vào tác dụng mong muốn mà phụ thuộc vào số lượng bao nhiêu triệu viên được bán ra thị trường. Giống như 1 bộ phim rất dở lại được chiếu ở các rạp phim trong khi 1 bộ phim hay thì lại không được chú ý
115 ACEi chống chỉ định trong bệnh hẹp động mạch thận 2 bên
Lưu lượng máu thận được xác định nghiêm ngặt bởi đường kính lòng mạch của động mạch thận. Trong thực tế, có nhiều yếu tố quan trọng khác cũng ảnh hưởng tới lượng máu chảy tới mao mạch cầu thận. Như ở bất kỳ vị trí nào, các động mạch xác định tính trở kháng và tốc độ dòng chảy
Không giống như các vi tuần hoàn khác, thận có một công việc đặc biệt để làm, tức là lọc những phân tử độc hại. Do đó, đối với máu đi vào thận, chức năng nuôi dưỡng thận dường như ít quan trọng hơn! Các nephrons của thận có lẽ là những tế bào “công nghệ cao” nhất trong cơ thể người (tất nhiên, chỉ bên cạnh các tế bào não) . Máu đi vào qua động mạch hướng tâm, qua mao mạch cầu thận lọc và 1 phần về theo động mạch li tâm.
Dòng máu vào mao mạch cầu thận được điều chỉnh bởi cả động mạch hướng tâm và li tâm thông qua kiểm soát của tín hiệu thần kinh. Sự lưu thông này được điều chỉnh bởi bộ máy cận cầu thận. Nó điều chỉnh lưu lượng máu cầu thận bằng cách tiết ra renin, hoạt động thông qua angiotensin 2 trên động mạch li tâm
Trương lực của động mạch li tâm được cho là yếu tố quan trọng duy nhất trong cơ chế điều khiển dòng máu tới mao mạch cầu thận
Điều gì xảy ra ở hẹp động mạch thận?
Khi có hẹp động mạch thận 2 bên, lưu lượng máu thận tới mao mạch cầu thận giảm không đáng kể nhưng phải tăng co lại động mạch li tâm. Nó giống như một van kiểm tra điểm xả lũ của 1 con đê, đóng 1 phần để duy trì đủ áp lực (ở đây là áp lực để lọc máu ở mao mạch cầu thận)
Điều gì xảy ra khi dùng ACEI?
Một khi chất ức chế ACE được sử dụng, động mạch li tâm mất khả năng co, áp lực trong mao mạch cầu thận giảm, áp lực lọc giảm
Lưu ý: ACEI không làm giảm lưu lượng máu thận trực tiếp nhưng áp lực tưới máu cầu thận giảm nên làm giảm chức năng thận cấp.
Ý kiến của bạn về hiệu quả bảo vệ thận của ACEI là gì?
Các nhà tim mạch và chuyên gia về thận đã luôn tin rằng ACEI không thân thiện với thận. Nhưng, bây giờ chúng ta có bằng chứng, ACEI không phải là một phân tử không thể dùng trong rối loạn chức năng thận.
Điều này dựa trên các quan sát được thực hiện, trong những năm mà Angiotensin 2 phải chịu trách nhiệm cuối cùng cho thận!
AT 2 gây tăng huyết áp nội mạch và các chất ức chế ACEI làm giảm nó. Điều này liên quan tới chế độ lọc của nephron và sự tổn thương cầu thận. Vì vậy, người ta nghĩ ACEi có vai trò rõ ràng trong việc gây tiến triển tổn thương tế bào thận
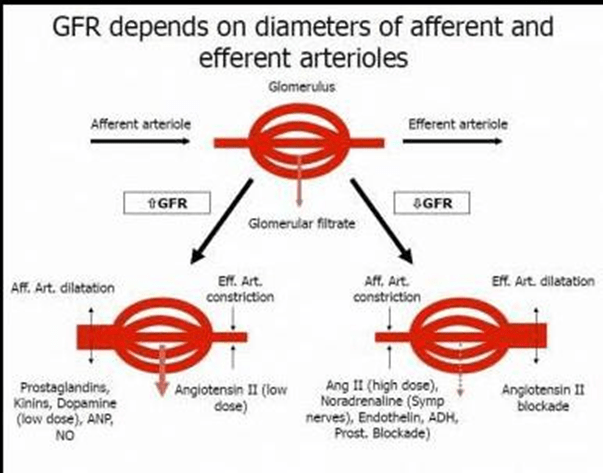
Điều này tương tự như câu chuyện chẹn beta trong CHF ban đầu được chống chỉ định ở CHF sau đó trở thành chỉ định rõ ràng
ACEI có thể được bắt đầu hoặc tiếp tục ở bất kỳ mức độ creatinine nào trong CKD ổn định có hoặc không có lọc máu
Tuy nhiên, ACEIs cần phải được dừng lại trong tất cả các điều sau đây Suy thận cấp
Đợt cấp của suy thận mạn
creatinine tăng nhanh (như hẹp động mạch thận hai bên)
116. Khi nào bạn nghi ngờ THA do hẹp động mạch thận?
Nghi ngờ ở những bệnh nhân THA khởi phát sớm khoảng từ 30-55 tuổi. nhưng có những bệnh nhân có thể khởi phát muộn hơn. Nghi ngờ khi có các điểm sau
Huyết áp tâm trương> 120 Tăng đột ngột huyết áp
Huyết áp kháng với ba hoặc bốn thuốc thông thường bao gồm thuốc lợi tiểu. Suy thất trái
Sự xuất hiện bệnh võng mạc tăng huyết áp Thổi tâm thu cạnh rốn
THA kèm theo CAD LVH trên siêu âm tim
Cuối cùng, điều quan trọng nhất là làm xấu đi chức năng thận với thuốc ức chế ACE là một dấu hiệu cho thấy thận ở trạng thái giảm tưới máu và tuần hoàn máu ở thận phụ thuộc vào tăng AT2.
Http://www.ajronline.org/cgi/content-nw/full/189/3/528/FIG21
117. Nguồn gốc và sự lành tính của LBBB
LBBB là một bất thường về điện tâm đồ. Ít khi chẩn đoán sót nhưng cũng ít người hiểu ý nghĩa của nó
Nguyên nhân của LBBB ở một bệnh nhân quan trọng hơn nhiều so với bản thân nó LBBB!
Mặc dù nguyên nhân thường gặp nhất của LBBB là lành tính (bất thường dẫn truyền mà không có bệnh lý van tim, cơ tim hay thiếu máu cục bộ), nên thận trọng khi loại trừ LBBB có nguyên nhân bệnh cấu trúc tim hoặc thiếu máu cục bộ.
LBBB & STEMI
Để chẩn đoán STEMI trong LBBB, chúng ta đã có tiêu chuẩn Sgarbosa nổi tiếng. Nó quá nổi tiếng đến nỗi người ta đã quên những hạn chế của nó. Áp dụng nó trong trường hợp cấp cứu không phải dễ dàng. Dựa trên lâm sàng và enzyme tim an toàn và có thể chính xác hơn. Nhờ các hướng dẫn của ACC, nó đã đơn giản hóa nhiệm vụ của chúng ta. Bạn được khuyến khích dùng tiêu huyết khối trong tất cả các trường hợp mới xuất hiện LBBB nếu như hình ảnh lâm sàng gợi ý ACS
LBBB & NSTEMI
Không ai biết làm thế nào để nhận ra NSTEMI trong LBBB. Theo logic thì ST chênh xuống có thể xảy ra. Còn độ nhạt như nào và lí do thì chưa ai biết
LBBB trong DCM
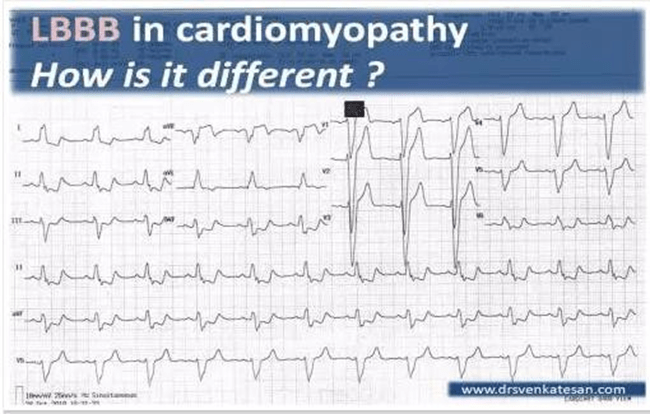
Đây là ECG của một bệnh hoàn toàn không có triệu chứng. Ông được chẩn đoán như là một trường hợp bệnh cơ tim giãn với EF 30% và không có bằng chứng về tình trạng thiếu máu cục bộ đang diễn ra. Nếu không rõ tiền sử dễ chẩn đoán là ACS
Để chẩn đoán bệnh cơ tim trong LBBB chúng ta không có tiêu chí cụ thể. Nhưng chú ý những điều sau đây:
Độ lệch trục trái tối thiểu 45-60 độ / AVR dương tính Điện áp thấp QRS, đặc biệt là chuyển đạo chi
ST chơn so với thay đổi điển hình ST/T thứ phát của LBBB QRS dạng lõm có sóng r hoặc s
bất thường nhĩ, sóng P rộng. kèm VPD
118. Trong xử trí thuyên tắc phổi cấp: khi nào heparin được dùng?
Thuyên tắc mạch phổi cấp là một tình trạng cấp cứu về mạch máu. Thuyên tắc phổi cần dùng tiêu huyết khối hoặc lấy bỏ huyết khối ngay. Tỷ lệ thành công cao nhưng cải thiện triệu chứng chậm
Sterptokinase là thuốc thường dùng để làm tan huyết khối phổi. (Ngoại trừ ở Mỹ, họ thích TPA tốn kém hơn nhiều)
Sterptokinase được dùng theo quy trình sau: 2,5 lakh UNIT bolus trong30 phút
Theo dõi với 1lakh UNIT / giờ trong 48 giờ tiếp theo (Lên đến 72 giờ)
Khi nào bắt đầu truyền Heparin?
Đối với TPA, Heparin phải được bắt đầu ngay sau khi truyền TPA hoàn thành (100mg trong 2 giờ)
Vì streptokinase được dùng trong 48 giờ nên người ta cho rằng heparin không bắt buộc trong giai đoạn này. Tuy nhiên, trong thực tế, chúng ta đang trì hoãn vai trò của loại thuốc chống thrombin tuyệt vời này trong những thời khắc quan trọng đang diễn ra. Do đó, theo logic cần dùng ngay heparin cùng streptokinase
Dùng heparin phải theo dõi APTT cẩn thận (dùng 500 UI/h)
Http://ats.ctsnetjournals.org/cgi/content/abstract/62/3/880?ijkey=cdcd223289bd75ffb49 a8d1cd1c73d35fe76e08d&keytype2=tf_ipsecsha
119. Bạn điều trị và theo dõi thuyên tắc phổi cấp sau dùng tiêu sợi huyết như nào?
Tắc mạch phổi lớn là bệnh lý đe dọa tính mạng. trước đây phẫu thuật là lựa chọn chính. Bây giờ, chúng ta dùng tiêu huyết khối như lựa chọn thay thế nhưng tỷ lệ thanh công chỉ 90%. Điều quan trọng phải đánh giá được dùng tiêu huyết khối đã thành công hay chưa để ra chỉ định phẫu thuật
Câu hỏi đặt ra là chúng ta phải chờ đợi bao lâu để đánh giá liệu pháp tiêu sợi huyết đã thất bại?
Không giống như nhồi máu cơ tim cấp, không có thời gian cửa sổ nghiêm ngặt để theo dõi. Cần đánh giá lâm sàng, VP/VQ, thông khí khoảng chết, MDCT, siêu âm…
Các thông số lâm sàng chính cần theo dõi Nhịp tim
Bão hòa Huyết áp
Có bốn cách xử trí sau dùng tiêu huyết khối không thành công.
1. Lấy cục máu gây tắc cấp cứu ở bệnh nhân không ổn định *
2. ở bệnh nhân ổn định, lên kế hoạch mổ phiên lấy máu cục máu đông gây tắc **
3. Lặp lại tiêu huyết khối ***
4. Tiếp tục Heparin trong 72 giờ và tối đa là một tuần. ****
* kết quả rất tệ
** Lựa chọn tốt nhất
*** có thể liều tPA ban đầu không đủ hoặc không hiệu quả để làm sách huyết khối. nó vẫn an toàn nếu lặp lại liều tPA trong vòng 5 ngày sau liều đầu tiên.
**** Không kém phần quan trọng và được coi là vô ích nhưng đã được chứng minh có hiệu quả ở nhiều người.
Làm thế nào để xử trí 1 bệnh nhân tương đối ổn định, có huyết khối lớn ở động mạch phổi?
Lựa chọn số 3 có thể dùng. Heparin được theo dõi dùng kéo dài Cải thiện lâm sàng là điều đầu tiên nên làm.
ổn định nhịp tim, cải thiện bão hòa oxy (> 90-95%), phục hồi thể tích thất phải là những chú ý chính.
120. Các dấu hiệu rối loạn chức năng thất phải trên siêu âm tim ở bệnh nhân tắc mạch phổi cấp?
Đa số thuyên tắc phổi cấp tính (APE) gần như được chẩn đoán khi giải phẫu tử thi. Chúng ta đang trong thời đại có thể nhận ra hầu hết tắc mạch phổi mà không gặp bất kỳ khó khăn nào
Kinh nghiệm đã dạy chúng ta, khi nghi ngờ hội chứng đáng sợ này, bất cứ biểu hiện không giải thích được như khó thở, nhịp nhanh, thiếu oxy, ngất kèm theo khó chịu trong ngực và có yếu tố nguy cơ (DVT, sau phẫu thuật…) sẽ tiên lượng rất nặng Chúng ta cho chụp CT, MRI, chụp V/P, chụp mạch phổi để chẩn đoán xác định PE. Chúng ta không nhận ra là chúng ta còn có một công cụ tại giường đơn giản gọi là siêu âm để phát hiện nhanh, đánh giá giải phẫu và huyết động tuần hoàn phổi. Trong thực tế, chúng ta có thể hình dung toàn bộ động mạch phổi chính (MPA) và phân chia của nó RPA, LPA. Kỳ lạ là các bác sĩ luôn yêu cầu chụp mạch phổi để chẩn đoán APE (tắc mạch phổi cấp) tỏng khi có siêu âm phổi không xâm lấn tại giường. Nó có thể loại trừ hầu hết các trường hợp thuyên tắc phổi nặng với độ nhạy tuyệt vời
Siêu âm có chẩn đoán sót APE?
Siêu âm có thể không thấy huyết khối nếu nó ở xa (trường hợp nhẹ) nhưng hiếm khi bỏ sót huyết khối trong MPA, RPA và LPA (trường hợp nặng)
Ngay cả khi siêu âm không thấy hình ảnh huyết khối, siêu âm cũng dễ thấy được có hiện tượng tăng áp động mạch phổi lên thành tâm thất phải và trái. thực tế cho thấy, ảnh hưởng của APE lên hình thái và chức năng RV là đặc điểm quan trọng nhất để nghi ngờ APE. Đây cũng được coi là chỉ định dùng tiêu huyết khối
Các đặc điểm siêu âm sau đây cho thấy có APE: có thể khó xem nếu bệnh nhân khó thở + thở nhanh, tuy nhiên trục động mạch phổi ngắn nên có thể xem được thậm chí ngay cả khi bệnh nhân nằm ngửa
– giãn RV (Một tiêu chuẩn hay dùng là đường kính cuối tâm trương thất phải ( End diastolic RV dimension) > đường kính cuối tâm trương thất trái. nên nhớ,
trong trường hợp cấp cứu có thể không cần theo tiêu chuẩn nghiêm ngặt này. Chú ý đường kính thất phải, nếu >3cm nên nghĩ đến APE. Nếu bệnh nhân có tiền sử COPD thì kích thước RV sẽ không phải là tiêu chuẩn chẩn đoán APE
– giảm vận động thành RV (dấu hiệu cấp cứu)
– vận động, di chuyển thành RV bất thường
– vách thất phải hình chữ D là cấp cứu tuyệt đối của RV
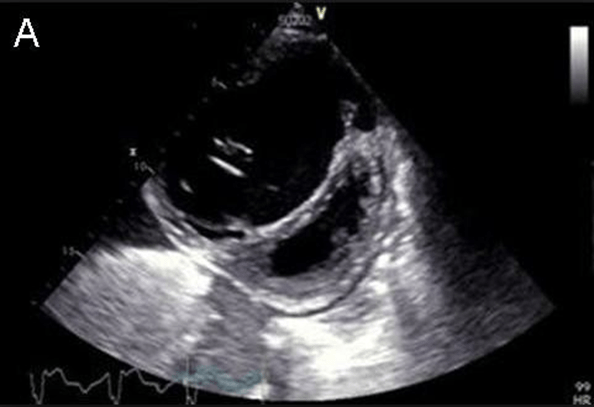
– trào ngược van 3 lá (Điều này phụ thuộc vào chiều dài và hướng của lá, có trường hợp không có mặc dù PAH nặng)
Các biểu hiện ít gặp hơn
– hở van động mạch phổi
– cục máu trong RA, , IVC, RV
– tăng áp thất phải
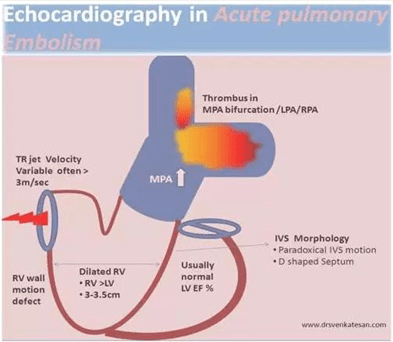
Ở áp suất nào RV bắt đầu giãn?
Điều nàychưa rõ ràng. Trong cơn gia tăng đột ngột áp lực RV, RV có khuynh hướng giãn ra, trong khi đó ở những trường hợp tăng áp phổi thì RV phì đại và giãn từ từ. Người ta tin rằng, các dấu hiệu đầu tiên của giãn RV có thể từ áp lực
PA 30mmHg. Do đó, thậm chí giãn nhẹ cũng có thể quan trọng trong chẩn đoán APE
Có thể chỉ dựa vào giãn RV đơn thuần, để làm bằng chứng cho rối loạn huyết động?
Có, nhưng việc nhận ra trên lâm sàng, sự mất ổn định về huyết động học quan trọng hơn mức độ giãn RV (hạ huyết áp / giảm oxy huyết)
Tụt huyết áp hay gặp ở APE. Mối quan hệ giữa PH và huyết áp hệ thống?
Chúng có mối quan hệ thuận nghịch, thậm chí có thể gây ngất ở những bệnh nhân này do:
– Hiệu ứng Bernhiem
– Suy giảm chức năng ứ máu
121. Trong thuyên tắc phổi cấp tính: heparin có nên bắt đầu sau khi dùng tiêu huyết khối?
Thuyên tắc mạch phổi cấp là cấp cứu về mạch máu, cần dùng tiêu huyết khối hoặc can thiệp lấy máu đông gây tắc ngay lập tức. Tỷ lệ thành công của tiêu huyết khối tốt nhưng cải thiện triệu chứng chậm hơn
Sterptokinase là thuốc thường dùng để tiêu huyết khối phổi. (Ngoại trừ ở Mỹ, họ thích TPA tốn kém hơn nhiều)
Sterptokinase được dùng theo phác đồ sau 2,5 lakh Đơn vị bolus trong30 phút
Theo dõi với liều 1lakh đơn vị / giờ trong 48 giờ tiếp theo (có thể tới 72 giờ)
Khi nào bắt đầu truyền Heparin?
Đối với TPA, Heparin phải được bắt đầu ngay sau khi truyền TPA kết thúc (100mg trong 2 giờ)
với streptokinase. Vì, streptokinase được dùng trong 48 giờ nên người ta cho rằng heparin không bắt buộc phải dùng trong giai đoạn này. Tuy nhiên, trên thực tế, người ta bắt đầu dùng heparin cùng với streptokinase.
Chúng ta tiêm heparin 500units / giờ và theo dõi APTT cẩn thận
122. Phân tử mới đánh giá tổn thương thận cấp tính tốt hơn creatinine!
Các chất chỉ điểm sinh học trong tổn thương hoặc nhồi máu cơ tim được dùng trong nhiều thập kỷ. Hội chứng vành cấp được chẩn đoán từ các xét nghiệm phát hiện ra các protein giải phóng từ cơ tim bị thương.
Các nhà thận học nghiên cứu từ lâu cố gắng tìm dấu hiệu tổn thương thận do thiếu máu cục bộ (dù đã có 2 chỉ số creatinine và BUN)
Neutrophil gelatinase associated Lipocalin (NGAL)
Đây là phân tử 25 Dalton được bài tiết nhiều trong các tế bào vỏ thận để đáp ứng với tổn thương thiếu máu cục bộ. Nó được giải phóng và bài tiết hoàn toàn qua nước tiểu. nồng độ NAL niệu tăng chứng tỏ có tổn thương thận cấp tính. Kinh nghiệm ban đầu cho thấy độ nhạy cao, có khả năng sẽ trở thành xét nghiệm thường quy trong tương lai gần Nồng độ NGAL trong nước tiểu> 250 ng / ml, 2 giờ sau khi phẫu thuật tim gợi ý tình trạng suy thận sắp xảy ra trong 24-48 giờ tới. Ưu điểm là NGAL tăng lên trước khi xuất hiện tăng creatinin huyết thanh. http://cjasn.asnjournals.org/cgi/content/full/3/3/665
123. Phác đồ dùng chống đông ở bệnh nhân có thai đặt van nhân tạo
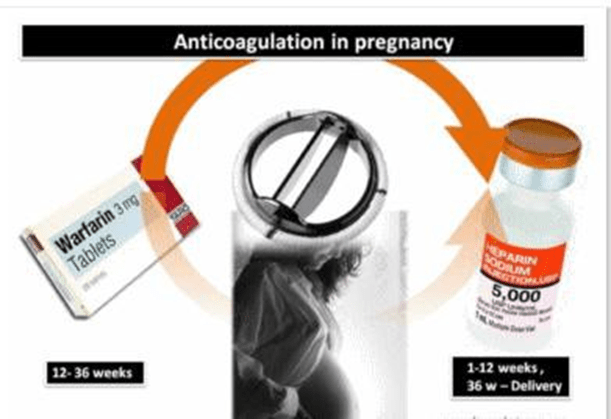
124. Tại sao LVH gây xuất hiện sóng q trên ECG?
LVH được cho là nguyên gây tạo ra sóng R cao. Tuy nhiên, chúng ta cũng biết LVH hay chẩn đoán nhầm là nhồi máu cơ tim, đặc biệt là nmct thành trước (Với sóng q sâu ở v1 đến v3 và đôi khi q ở chuyển đạo dưới)
Mô nhồi máu gồm các tế bào chết trong khi LVH gồm các tế bào sống. làm thế nào ECG xuất hiện những hình ảnh tương tự trong cả 2 trường hợp?
Cần phải nhận ra, ECG không phải là cái máy xác định mô, nó chỉ đơn giản thể hiện sự di chuyển liên quan đến các bản ghi của các điện cực
Nếu nó đi về phía điện cực sẽ ghi được sóng R, nếu đi xa khỏi điện cực sẽ ghi được sóng q
Trong nhồi máu, rõ ràng là các tế bào chết hình thành một cửa sổ điện riêng biệt sẽ ghi được sóng q.
Chúng ta biết, cơ tim bao gồm không chỉ tế bào cơ mà còn các nguyên bào sợi, tế bào kẽ, collagen và các chất ngoại bào khác. Những tế bào không co bóp này có ít năng lượng điện để dẫn truyền. Trong LVH sinh lý học không có tăng khoảng kẽ. Nó đơn giản chỉ phì đại các đơn vị co độc lập. Nó tăng khả năng dẫn truyền và sinh ra sóng R cao trên ECG
Nguyên nhân sinh lý của LVH bao gồm:
– Tim của vận động viên
– bệnh nhân tăng huyết áp
– Giai đoạn đầu của hẹp động mạch chủ
– LVH bệnh lý
Ở đây LVH chủ yếu do sự gia tăng của nguyên bào sợi và các tế bào kẽ. Điều này cản trở sự liên kết của các sợi cơ vân dẫn đến xuất hiện sóng q trong nhiều trường hợp
Các điều kiện gây ra sóng q bệnh lý
– Khoảng 10% LVH do THA có thể có sóng q
– HOCM
– Giai đoạn cuối của hẹp động mạch chủ
– Một số trường hợp kết hợp với bệnh tiểu đường có THA
– THA kèm bệnh thận mạn
* Có một nguyên nhân nữa làm xuất hiện sóng q trong LVH. Đây là kỹ thuật ghi. Khi trái tim quay ngược chiều kim đồng hồ, đáng lẽ ở vách ghi được sóng r lại ghi được sóng s mô phỏng dạng sóng q. Trên thực tế, đây có thể là nguyên nhân phổ biến nhất nhầm LVH với MI
Vì vậy sóng q không phải tiêu chuẩn quá quan trọng để chẩn đoán nmct, nó có thể tạo ra ngay cả ở các tế bào sống
125. Bệnh tim bẩm sinh ảnh hưởng tới tăng trưởng và phát triển ở trẻ như nào?
Tim là cơ quan đầu tiên chuyên môn hóa của thai nhi. Nhịp tim đầu tiên bắt đầu vào ngày thứ 22 của thai kỳ! . Từ khi đó, chức năng của nó hoàn thiện dần theo sự phát triển của bào thai. Nó tiếp tục ở trẻ sơ sinh, trẻ nhỏ và thời thơ ấu.
Không có gì ngạc nhiên, để phát hiện sự chậm phát triển trong bệnh tim bẩm sinh. Có thể đánh giá thích hợp ngay từ lúc ước lượng cân nặng bào thai/cân nặng khi sinh. Các giai đoạn vận động và nhận thức cần được đánh giá tỉ mỉ
Bệnh tim mạch
ASD, VSD, PDA có xu hướng ảnh hưởng đến tăng cân nhưng thường không ảnh hưởng đến chiều cao nhiều. Tuy nhiên, sự xuất hiện của tăng áp phổi sớm cũng sẽ ảnh hưởng nghiêm trọng đến chiều cao.
Bệnh tím tái
CHD ảnh hưởng đến chiều cao và cân nặng tương ứng. Bệnh tim tím tái có tăng lưu lượng máu phổi làm cho tỷ lệ sống còn thấp, suy tim và ảnh hưởng nhiều đến tăng trường và phát triển
Cơ chế phát triển còi cọc.
Thuật ngữ được sử dụng thường xuyên “không lớn”, có thể không phải là do bệnh tim. có nhiều yếu tố liên quan như hoàn cảnh xã hội, thói quen ăn uống, chăm sóc của người mẹ, bệnh tật hiện có, phẫu thuật… các yếu tố này ảnh hưởng nhiều hơn ở trẻ sơ sinh có tăng lưu lượng máu phổi
Ảnh hưởng đến chức năng nhận thức
Trái ngược với những gì mong đợi, ngay cả tình trạng giảm ôxy huyết mạn tính và chứng tím tái cũng không có ảnh hưởng chút nào tới trí thông minh của trẻ. Trừ khi có các dị tật thần kinh kèm theo
Tuy nhiên, bây giờ chúng ta nhận ra rằng, sự phát triển của não bị tổn thương trong môi trường thiếu oxy. Thực tế, tổn thương nhận thức có thể bắt đầu ngay từ khi mang thai.
126. Sóng T 2 pha trong hội chứng vành cấp
NSTEMI là vấn đề lâm sàng thường gặp trong CCU.
Khi chúng tôi nói NSTEMI nó có thể bao gồm bất kỳ trường hợp nào dưới đây: NSTEMI có ST chênh xuống
NSTEMI với sóng T âm NSTEMI có sóng T 2 pha NSTEMI với ECG bình thường
Thật châm biếm khi suy nghĩ STEMI sẽ tiến triển như NSTEMI
Theo mặc định hầu hết chúng ta nghĩ, nếu đó là NSTEMI. . . Phải có ST chênh xuống. Tư duy này không hợp lý nhưng mang tính truyền thống. Tuy nhiên NSTEMI có ST chênh xuống tiên lượng tồi hơn các dạng khác
điện tâm đồ sau của người đàn ông 45 tuổi bị đau ngực trong suốt 48h.
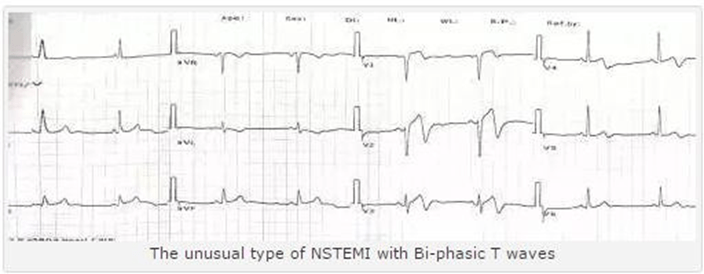
Dạng ít gặp của NSTEMI có sóng T 2 pha
Siêu âm thấy giảm vận động trong vùng cấp máu của LCX. Xác định chẩn đoán NSTEMI. Bất thường chủ yếu là sóng T 2 pha.
** Người ta có thể tự hỏi tại sao chúng ta không thể gọi đây là một trường hợp STEMI cổ điển?
Nếu ST chênh lên 2mm, ta có thể nghĩ ngay là nmct? Tuy nhiên, không có T 2 pha hay T âm trong những giờ đầu của STEMI cổ điển
Điều này chính xác đã xảy ra ở đây. Do đó chúng ta không thể gọi ECG trên là STEMI. Thay vào đó, nó là STEMI tiến triển thành NSTEMI. Vì vậy, có sự kết hợp đặc điểm của STEMI / NSTEMI xảy ra với nhau. Đây là trường hợp điển hình STEMI chuyển sang non q MI
127. Các quan sát mới về sóng T cao “hyper acute” trong STEMI
Sóng T ít gây chú ý hơn trong STEMI trừ khi có sóng T cao thực tế gợi ý pha tăng cấp trong STEMI
Phase cấp là gì?
Vài giây Vài phút Một giờ Vài giờ
Bất kỳ lựa chọn nào ở trên
Câu trả lời là gì?
Không ai biết chính xác nó có thể biến đổi như nào. Vì vậy, đáp án thứ 5 có thể là câu trả lời đúng.
* Điều quan trọng nhất là phase cấp tính không nhất thiết phải xảy ra ở tất cả các bệnh nhân STEMI.
Một số quan sát về biến đổi sóng T trong STEMI
Cơ chế của sóng T cấp “hyper acute T wave”
Liên quan tới động học của kênh kali. Tăng vận chuyển kali vào nội bào được cho là nguyên nhân gây sóng T ―tối cấp‖
Sóng T đặc trưng cho tái tưới máu
Sóng T âm ở chuyển đạo trước tim là dấu hiệu liên quan nhồi máu mạch vành đặc biệt ở LAD
STEMI tiến triển chậm
Đây là khái niệm tương đối mới. STEMI với giai đoạn cấp tính kéo dài, nghĩa là, các sóng T “lăn tăn, không dứt khoát dilly -dally” trong vài giờ hoặc thậm chí vài ngày (vẫn gọi là đau ngực tiền nhồi máu)
Chính đặc điểm này của sóng T làm cho chẩn đoán STEMI trở nên khó khăn. Men tim và các hướng dẫn dùng tiêu huyết khối cũng sẽ phải chờ cho đến khi ST chênh lên.
Điều này thật hên xui. Một giải pháp đơn giản khác là chuyển bệnh nhân đến phòng cath để tìm chính xác điều gì đang xảy ra trong LAD!
Bây giờ, có gì mới về sóng T trong STEMI?
Nó giúp khu trú trong nhồi máu LAD
Sóng T ―hyper acute‖ tăng cao liên tục giúp ta xác định có tổn thương LAD. Bài báo này đã xác nhận rõ ràng sự quan sát này. Nghiên cứu này được thực hiện từ nhóm thuần tập tiến hành ngay PCI, thiết lập hoàn hảo để đánh giá sự tiến triển sóng T trong những phút đầu tiên của STEMI.
Những bí ẩn khác về sóng T trong STEMI
Sóng T “hyper acute” có xảy ra ở sTEMI thành sau dưới?
Tôi tin rằng nó rất hiếm.
Sóng T sẽ thay đổi trong NSTEMI như nào?
Điều này lại không rõ ràng. Hầu hết các trường hợp sóng T tối cấp sẽ tiến triển như STEMI. Nhưng, không có gì ngăn nó tiến triển như NSTEMI. Nói chung, sóng T tối cấp có thể tự hết ở 1 số ít người may mắn (người có khối lượng TPA lớn lưu thông tự
nhiên). Nếu các men ly giải tự nhiên này chỉ thành công một phần, nó có thể tiến triển lần nữa ―De nova‖ thành NSTEMI.
Sóng T 2 pha trong ACS.
Sóng T nhìn có vẻ lành tính với đoạn âm nằm sau ở chuyển đạo trước tim có thể là là dấu hiệu báo hiệu tử vong ở LAD. Đây là những trường hợp nổi tiếng vì gây tử vong ở người đàn ông trẻ liên quan tới quá thời gian cửa sổ ở LAD
STEMI tiến triển chậm là gì?
Giai đoạn sóng T cao kéo dài có thể cho thấy, cơ tim có khả năng chống lại các tổn thương do thiếu oxy máu
Điều kỳ quái nhất trong hiểu biết của chúng ta về sinh lý bệnh ACS là khái niệm về thời gian cửa sổ, dựa trên đó, tất cả các liệu pháp điều trị ACS của chúng ta đều xoay quanh nó!
Có phải tất cả các tế bào cơ tim đều có cùng thời gian sống thiếu máu không? Có thể một số bệnh nhân được ban phước bằng các tế bào cơ tim có khả năng kháng lại khi gặp tình trạng thiếu oxy hoặc thiếu máu không?
o tim, các cơ sẽ hoại tử trong vòng 30 phút thiếu máu, trong khi một số cơ tim không thể nhồi máu ngay cả sau 24 giờ tắc nghẽn. Vì vậy, STEMI đang phát triển chậm là một đặc điểm của chứng thiếu máu cục bộ cơ tim. Không phải là khái niệm thiếu máu cục bộ chúng ta nghiên cứu rộng rãi trước đây.
128. Vôi hóa mạch vành – tốt hay xấu?
Bệnh gây chết người số một của tim là xơ vữa động mạch vành. Xơ vữa động mạch vành đồng nghĩa với làm cứng động mạch. Sự xuất hiện của canxi (vôi hóa) mạch vành với CT scan, đã làm điên đảo các bs tim mạch (Nó đã được thay thế bằng CT 64/128 dãy thu lại lợi nhuận chưa từng có)
Vôi hóa mạch vành có tiên lượng tốt, xấu hoặc trung bình trong CAD không?
Bài viết này trong bài viết của tạp chí của Mỹ năm 2011 cho thấy canxi hóa thành động mạch vành tiên lượng tốt với bệnh nhân
Điều gì làm cho mảng bám dễ bị tổn thương?
Các mảng bám, sự phân bố và đặc tính của nó làm cho nó dễ bị tổn thương. Các điểm tạo thành bởi lipid có thể dẫn đến nứt mảng bám. Tính chất bán rawsnm hỗn hợp, các mảng mềm dễ bị vỡ. cơ chế oxy hóa LDL, dịch hóa LDL… làm các mảng bám có nguy cơ vỡ và bong. Nếu không có các cơ chế trên, mảng bám sẽ rắn và cứng
Mảng bám vôi hóa có khả năng chống lại biến dạng cơ học. canxi hóa mạch vành là hậu quả cuối cùng của xơ vữa động mạch vành.
Ý nghĩa của mảng vôi hóa cứng trong lòng mạch vành?
Như nghiên cứu này đã chỉ ra, vôi hóa trong thành động mạch vành là vô hại. Tất nhiên, vôi hóa không nên dày đặc và cản trở lưu thông máu. Điều này sẽ đòi hỏi phải can thiệp. tổn thương vôi hóa ít có khả năng dẫn đến các biến chứng mạch vành cấp so với tổn thương mềm, không bị tổn thương. Nhưng nó có thể khó khăn khi bạn muốn đặt stent
129. prasugrel cướp lấy vinh quang đáng lí ra phải là của Aspirin?
Tiểu cầu là thủ phạm chính trong việc xuất hiện huyết khối động mạch. Ức chế tiểu cầu là phương thức chính để điều trị / ngăn ngừa các hội chứng động mạch vành cấp tính và mãn tính. Đây là hướng dẫn đã được phê duyệt về phòng ngừa ban đầu và thứ phát của CAD.
Các thuốc kháng tiểu cầu là thị trường thuốc lớn nhất trong số các loại thuốc tim.
Aspirin là thuốc kháng tiểu cầu tốt nhất được biết đến. Nó không chỉ hiệu quả nhất mà giá cả còn quá thấp so với các thuốc khác. Thật không may nó lại là một loại thuốc phổ thông và không có bằng sáng chế. Dù tốt và an toàn, nhưng giá thành thấp là bất lợi lớn nhất của aspirin! Vì vậy, nhiều yếu tố mong muốn thuốc này xuất hiện ít hơn trong các guideline để xuất hiện nhiều thuốc kháng tiểu cầu mới
Sau khi phân tích các tài liệu sẵn có, tôi đã biên soạn các kết luận sau đây (Hầu hết các quan sát chủ quan, nhưng tôi tin chắc rằng nó còn khách quan nhiều hơn với sự thật …)
Tất cả các tuyên bố sau đây có thể được gọi là đúng, đúng, được cho là đúng, có thể đúng, tại một thời điểm nào đó (Giữa thập kỷ trước và hiện tại!)
Aspirin một mình cũng đủ dùng tốt trong cả ACS và CAD mãn tính Clopidogrel có hiệu quả tương đương như aspirin trong ACS. Aspirin dùng một mình nguy hiểm ở ACS.
Clopidogrel đơn độc nguy hiểm hơn aspirin đơn độc trong ACS, Aspirin + Clopidogrel có tác dụng kháng tiểu cầu tốt nhất.
Aspirin + Clopidogrel kết hợp vẫn còn nguy hiểm. Prasugrel có hiệu quả hơn clopidogrel
Prasugrel không bao giờ có thể có hiệu quả như aspirin * Không sử dụng clopidogrel đơn thuần ở bệnh nhân DES. Aspirin có thể an toàn ở hầu hết các bệnh nhân đặt stent
Đối với thuốc prasugrel thực sự có lợi thì cần phải kê toa thêm aspirin. Chỉ dùng Prasugrel có thể gây nguy hiểm cho người bệnh đặt stent.
Nếu bệnh nhân đang dùng heparin đồng thời cũng không thực sự có vấn đề gì quan trọng Trên đây là kết luận của tôi trong tất cả các thử nghiệm trên tiểu cầu trong ba thập kỷ qua Bạn suy luận điều gì?
Có một cơ sở vững chắc cho sự nghi ngờ này vì không ai trong số các nhà nghiên cứu sẵn sàng thực hiện so sánh trực tiếp giữa aspirin và prasugrel hoặc clopidogrel!
130. Làm thế nào Troponin có thể tăng trong viêm màng ngoài tim?
Trái tim có ba lớp Thượng tâm mạc Cơ tim
Nội tâm mạc
Thượng tâm mạc cũng giống như lá tạng của màng ngoài tim, nếu viêm màng ngoài tim nội mạc tử cung. Nếu viêm màng ngoài tim có thể tổn thương màng ngoài tim và vùng bên dưới thượng tâm mạc
Troponins có nằm sâu bên trong cơ tim không?
Không. Nó thậm chí có thể nằm chỉ vài micron bên dưới lớp thượng tâm mạc, do đó viêm màng ngoài tim nặng có thể làm tăng troponin
Liệu troponin có liên quan đến ST chênh lên?
Cơ chế gây ST chênh lên trong viêm màng ngoài tim thực sự là dấu hiệu tổn thương trên cơ tim. Trong thực tế, không có cách nào để phân việt nhồi máu vùng thượng tâm mạc từ viêm màng ngoài tim
Trong viêm màng ngoài tim, sự giải phóng troponin là do viêm hoặc hoại tử?
Cả hai đều có thể xảy ra.
Viêm cơ-màng ngoài tim là gì?
Đó là một thuật ngữ chung được sử dụng để chỉ ra tình huống trên. Trong điều kiện thực tế Viêm màng ngoài tim + Troponin dương tính có thể được gọi là viêm cơ- màng ngoài tim.
Viêm toàn bộ tim là gì?
Đó là viêm tim liên quan đến cả ba lớp của tim, trước gây gặp trong sốt thấp khớp . Bệnh tim mạch kéo dài làm tăng troponin ở mức đáng kể.
Những câu hỏi điên rồ trong bệnh tim mạch
Cấp máu vùng màng ngoài tim? Có thiếu máu cục bộ vùng màng ngoài tim không?
Thông điệp cuối cùng
Đừng bao giờ đánh giá thấp tầm quan trọng của màng ngoài tim bất cứ khi nào bạn gặp phải ST chênh lên mà khó giải thích trên ECG
Dưới đây là một bài báo đã nghiên cứu tỉ mỉ vấn đề này

http://www.onlinejacc.org/content/42/12/2144
131. Chẩn đoán nhầm viêm màng ngoài tim?
Đối với một sĩ quan cảnh sát đến thăm một địa điểm phạm tội, mỗi người đều giống như thủ phạm. Đối với bác sĩ tim mạch ngồi tiếp nhận bệnh nhân, tất cả đau ngực đều phải nghĩ đến 1 cơn nhồi máu.
Điều này giúp hiếm khi xảy ra lỗi nhưng rất tốn kém. Khi 1 bệnh nhân đau ngực nặng kèm theo ST chênh lên trên ECG, thường bạn sẽ không có lí do gì mà không nghĩ đến STEMI
Đây là lỗi về y tế thường xuyên xảy ra
Y khoa là một môn nghệ thuật, và chúng ta là những người nghệ sĩ. Nmct mạn tính vẫn có thể có ECG bình thường và ST chênh lên mà không nhất thiết phải là MI
Đây là Ecg của 1 bệnh nhân đau ngực và đồng nghiệp của chúng tôi đã chẩn đoán chính xác bệnh lý này
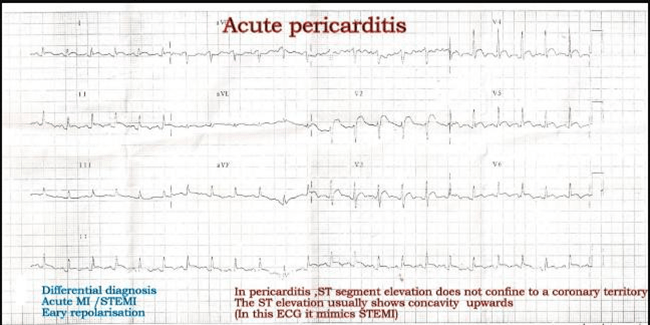
Hầu hết các bác sĩ sẽ dùng tiêu huyết khối cho bệnh nhân này hoặc cho đi can thiệp
Điểm giúp phân biệt
ST chênh lên lan tỏa không giới hạn trong vùng cấp máu của động mạch Không có thay đổi đối xứng
ST chênh lõm ―concave‖
Siêu âm tim và men tim giúp phân biệt
Cơ chế của ST chênh lên trong viêm màng ngoài tim là gì?
Nó thực sự là tổn thương vùng thượng tâm mạc hoặc dưới thượng tâm mạc. Điều gì sẽ xảy ra nếu có STEMI kèm viêm màng ngoài tim sợi “fibrinous”? ST tăng gấp đôi. Mô phỏng dạng nhồi máu.
Nếu dùng thuốc tiêu huyết khối trên bệnh nhân viêm màng ngoài tim lan tỏa có nguy cơ gì?
Nó có thể chảy máu vào vùng màng ngoài tim
ECG sẽ thay đổi thế nào trong viêm màng ngoài tim khu trú?
132. cơ chế của adenosine trong AVNRT?
Adenosine là một chất tương tự purine. Tác dụng bằng cách kích thích kênh K + bên ngoài của nút AV, cụ thể hơn là ở phía sau con đường dẫn truyền chậm nằm gần vùng xoang vành.
Một tác dụng khác của adenosine là ức chế cAMP, tương tự như tác dụng chẹn beta cũng có thể giúp chấm dứt cơn nhịp nhanh.
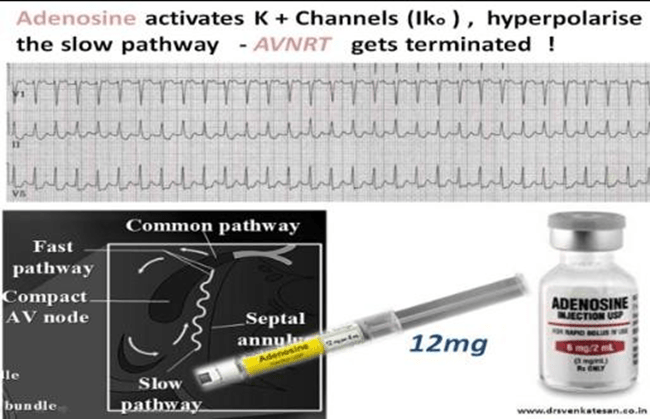
Adenosine: Phép lạ thần kinh chỉ kéo dài 10 giây
12mg bolus nếu có thể nên dùng trong tĩnh mạch trung tâm (Không bắt)
Có thể chấm dứt cơn nhịp nhanh ngay lập tức. có thể xuất hiện VPD thoáng qua trong quá trình chấm dứt cơn nhịp nhanh
Nếu bệnh nhân đang sử dụng thuốc nhóm Aminophylline (Là thuốc đối kháng adenosine), tác dụng ức chế nút AV có thể không hoạt động.
(Có thể ở thời điểm này, Aminophylline được sử dụng trong rối loạn chức năng xoang hoặc block AV để tăng nhịp tim)
http://www.medscape.com/viewarticle/585287_2
133. Đứng trước tiêu chuẩn Sgarbossa
Block nhánh trái (LBBB) kì cục nhưng lại có mối liên quan quan trọng với STEMI. LBBB gây thay đổi đáng kể trong hình thái qrs trái ngược với hoạt động của tâm thất. đoạn ST nâng lên do thay đổi tái cực có tầm quan trọng hàng đầu trong STEMI
LBBB có thể kết hợp với STEMI theo những cách sau
LBBB hoại tử cấp tính có tổn thương lớn ở cơ tim- nguy cơ sốc LBBB mạn tính với STEMI cấp tính
LBBB thiếu máu cục bộ thoáng qua trong STEMI LBBB phụ thuộc tần số (hiếm khi nhịp tim chậm) STEMI trong trường hợp có máy tạo nhịp
Trong mỗi trường hợp trên, có nhiều tiêu chuẩn được đề xuất để chẩn đoán STEMI ở bệnh nhân đau ngực cấp tính kèm theo có sự xuất hiện của LBBB
Các tiêu chí được đề xuất bởi Sgarbosa vào năm 1996 trở thành tiêu chuẩn để chẩn đoán STEMI
Trong 15 năm qua, kinh nghiệm của chúng tôi ở một trong những đơn vị chăm sóc động mạch vành lớn nhất ở Ấn Độ, chúng tôi nhận thấy các tiêu chí này ít có giá trị trong STEMI và LBBB. Hầu hết chẩn đoán chính xác thực hiện đơn giản bằng lâm sàng
Bên cạnh đánh giá lâm sàng, chúng tôi thấy các enzym tim (Troponin và CPK) rất đáng tin cậy trong chẩn đoán STEMI với LBBB.

Điều đáng ngạc nhiên là siêu âm tim không đáng tin cậy như ECG trong chẩn đoán STEMI
Và tiêu chuẩn Sgarbossa độ nhạy rất thấp
134. Sự có mặt của LVH là lợi thế hay bất lợi với bệnh nhân STEMI

LVH được coi là dấu hiệu bất lợi cho cả biến cố mạch vành và suy tim (Framingham). Mặc dù điều này có thể đúng, nhưng chúng tôi cũng có bằng chứng cho thấy những bệnh nhân bị LVH chịu được chứng thiếu máu cục bộ tốt hơn, vùng nmct nhỏ hơn. Trên thực tế, không thể coi LVH như một yếu tố nguy cơ chính cho MI. Nhưng nhiều nghiên cứu khác cho thấy mức độ nguy hiểm nếu có LVH trong ACS.
Tóm tắt
LVH thực sự là một yếu tố tiên lượng bất lợi ở bệnh nhân STEMI. tỷ lệ tử vong ở STEMI 7 ngày ở mức dưới 3% nếu kết hợp với LVH (5-7% ở nhóm không LVH).
* Điều quan trọng là nhận ra không phải tất cả LVH đều giống nhau.
Với nghiên cứu của Framingam, sự có mặt của LVH trong ECG dưới bất kỳ hình thức nào của hội chứng mạch vành cấp tính, dù nó làm tăng nguy cơ tử vong đột ngột ở 1 số người nhưng vẫn có những ưu điểm, chắc chắn tại thời điểm của ACS
Reference
1 Levy D, Garrison RJ, Savage DD, Kannel WB, Castelli WP. Prognostic implications of echocardiographically determined left ventricular mass in the Framingham Heart Study. N Engl J Med 1990;322:1561–1566
2. The Coronary Drug Project Research Group. Left ventricular hypertrophy patterns and prognosis. Experienced post infarction in the Coronary Drug Project.Circulation 1974;49:862–869.
3. Behar S, Reicher-Reiss H, Abinadar E, Agmon J, Barzilai J, Friedman Y, Kaplinsky E, Kauli N, Kishon Y, Palant A. Long-term prognosis after acute myocardial infarction in patients with left ventricular hypertrophy on the
electrocardiogrm. Am J Cardiol 1992;69:985–990.
*Coronary drug project (A old study done in early 1970s has more credibility when LVH was not considered as pharma target !)
135. Bạn có thể đánh giá rối loạn chức năng tâm trương bằng ECG?
Chúng ta thường bỏ qua thực tế, ECG có thể cung cấp dữ liệu về thay đổi huyết động lâu dài của bệnh nhân. Trong khi siêu âm tim cho ta giải phẫu và sinh lý học, ECG cung cấp thông tin về giải phẫu, huyết động học
Trong khi Doppler là một phương thức giá trị để đo huyết đông tại 1 thời điểm hiện tại, nó không cho ta biết được những gì đã xảy ra trong những tháng hoặc năm trước.
Phì đại nhĩ trái LAE có tầm quan trọng rất lớn. Đó là lý do tại sao kích thước nhĩ trái được gọi tắt là HBA1C của rối loạn tâm trương (Một dấu hiệu mạn tính của rối loạn tâm trương)
Trên thực tế, những nếp nhăn và những vết rạn nứt trong sóng P, cho thấy áp suất tâm nhĩ trái và dấu hiệu rõ ràng về chức năng tâm trương cơ tim.
P là sóng duy nhất xảy ra trong thời kỳ tâm trương. Do đó không có gì đáng ngạc nhiên, khi đánh giá nó có thể phát hiện những bất thường về thời kỳ này trong chu kỳ tim.
Kinh nghiệm cho thấy, các hình ảnh ECG sau đây có thể là dấu hiệu của rối loạn chức năng tâm trương đáng kể.
Sóng P Notched (không có khấc) Sóng P rộng
Sóng P 2 pha
* Đáng ngạc nhiên là những bất thường này tương quan với rối loạn tâm trương ít nhất ở độ 1 ngay cả khi không có LAE hoặc LVH trên siêu âm tim.
136. Ảnh hưởng của thuốc, điện giải và chuyển hóa lên ecg
ECG bị ảnh hưởng bởi nhiều yếu tố, bao gồm thuốc, bất thường điện giải và nhiều điều kiện chuyển hóa khác.Thêm vào đó, ECG có thể có vai trò chính, gợi ý các bất thường có thể đe dọa tính mạng, vd như tăng kali máu hoặc ngộ độc thuốc chống trầm cảm 3 vòng (TCA tricyclic antidepressant toxicity)
ẢNH HƯỞNG CỦA THUỐC THUỐC ĐIỀU TRỊ LOẠN NHỊP
Có rất nhiều thuốc, bao gồm thuốc tim mạch và không phải tim mạch có thể ảnh hưởng đến ECG. Sự thay đổi này có thể ảnh hưởng trực tiếp lên hoạt động điện tạo nhịp, hệ thống dẫn truyền, cơ nhĩ và cơ thất. Thuốc còn ảnh hưởng lên hệ thống thần kinh tự động ( giao cảm và đối giao cảm ) nên có ảnh hưởng quan trọng lên tạo nhịp và dẫn truyền.
Dưới đây là phân loại thuốc chống loạn nhịp thường dùng

Nhóm 1 : chẹn kênh Na,nên có thể kèo dài QRS. Chia làm 3 nhóm nhỏ
+ IA : còn có thể chẹn kênh Na dẫn đến kéo dài tái cực thất, nên gây ra hội chứng QT dài, tăng nguy cơ xoắn đỉnh và ngưng tim đột ngột..Bao gồm : Quinidine, Procainamide..
Thuốc tác dụng trên tất cả các tần số tim.
+ IB : chẹn kênh natri trung bình đến nhiều , ít tác dụng khi tần số tim chậm và có hiệu quả khi tần số tim nhanh ,vd như lidocain, mexiletin, phenytoin..
+IC : chẹn kênh natri điện thế , tác dụng trên tần số tim bình thường trên mô bình thường và hiệu quả tối thiểu trên thời gian điện thế hoạt động . Điều trị rung nhĩ và nhịp nhanh trên thất khác, có hình ảnh phức bộ QRS rộng .VD như flecainid, propaferon ( còn có thêm tác dụng chẹn beta).
Tất cả các thuốc chống loạn nhịp nhóm 1 đều có thể gây ra loạn nhịp thất đe dọa tính mạng BN do làm thay đổi điện thế cơ bản của tế bào cơ tim, gọi là ―proarrhythmic drug effects ―.
Kéo dài QT có thể gây xoắn đỉnh, đe dọa tính mạng BN , có thể xảy ra khi dùng nhóm 3, vd như amiodaron, sotalol do chẹn kênh K dẫn đến kéo dài thời gian tái cực.
Chẹn beta ( nhóm 2 ) và chẹn Ca ( nhóm 4) có thể ảnh hưởng lên nút xoang và nút nhĩ thất, dẫn đến nhịp chậm từ trung bình đến nặng.Sự kết hợp thuốc ( vd như metoprolol và diltiazem ) có thể làm nhịp chậm hơn do ức chế nút xoang và kéo dài thời gian trơ của nút nhĩ thất, đặc biệt hay xảy ra ở người già.
Một số thuốc không được phân loại nên được xếp vào nhóm 5, bao gồm digoxin, adenosine..
THUỐC HƯỚNG THẦN
Thuốc hướng thần ( vd như phenothiazin, hay TCA ) có thể làm thay đổi ECG và khi ngộ độc gây ra ngất hoặc ngừng tim do loạn nhịp thất , vô tâm thu. Chúng có thể kéo dài QRS, gây hình ảnh giống block nhánh , hoặc kéo dài tái cực gây xoắn đỉnh . Có nhiều loại thuốc trong tâm thần có thể gây xoắn đỉnh như methadone, khi đó gọi là ― atypical hoặc second generation antipsychotics ― .
Lithium carbonate , dùng để điều trị bệnh lưỡng cực ?? ( bipolar disease ) có thể gây loạn chức năng nút xoang hoặc block đường ra nút xoang hoặc chậm xoang nghiêm trọng.
Donezipil sử dụng để điều trị Alzheimer , gây nhịp chậm, do đối kháng men cholinesterase làm tăng hoạt động của acetylcholine lên nút xoang và nút nhĩ thất.
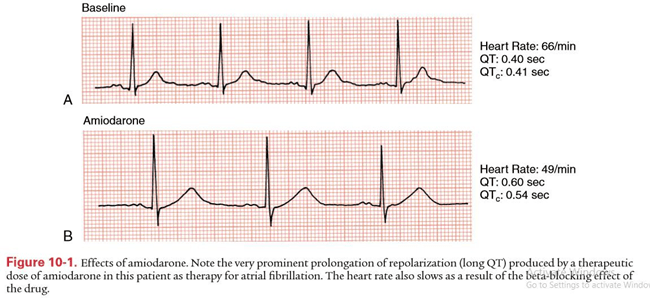
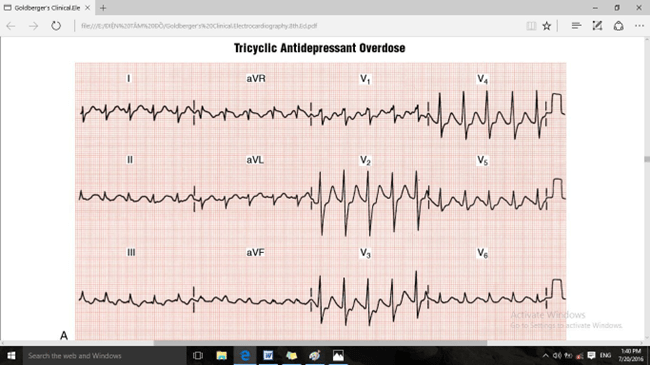
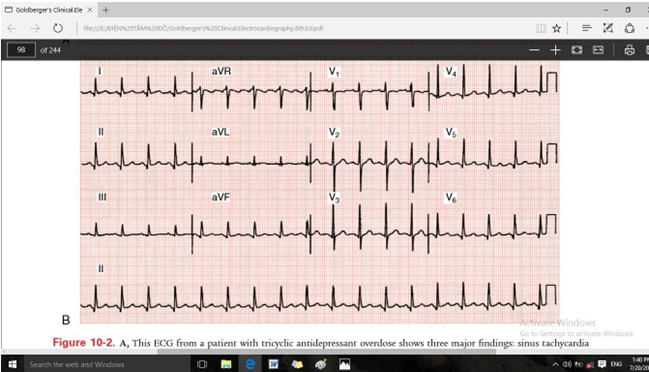
2 hình bên dưới là ECG của BN quá liều thuốc chống trầm cảm 3 vòng, có 3 dấu hiệu chính sau : nhịp nhanh xoang ( do đối kháng hệ cholinergic và đồng vận trên hệ adrenergic ) , kéo dài QRS ( do chậm dẫn truyền nhĩ thất ) , kéo dài QT ( do chậm tái cực
Đo lại ECG của BN sau 4 ngày thì vẫn còn tồn tại nhịp nhanh xoang, tuy nhiên QRS rộng và QT dài đã biến mất..
MẤT CÂN BẰNG ĐIỆN GIẢI
Bất thường nồng độ trong huyets thanh của K và Ca có thể ảnh hưởng đến ECG. Tăng kali máu có thể dẫn đến ngộ độc tim ( cardiac toxicity )
TĂNG KALI MÁU
Tăng kali máu có thể ảnh hưởng lên cả khử cực (QRS) và tái cực (STT) .Nồng độ kali bình thường từ 3,5 đến 5 mmol/ L. Thay đổi đầu tiên khi tăng nồng độ kali huyết tương là song T hẹp và có đỉnh nhọn., với hình dạng ― tented ― và ― pinched‖, và chúng có thể trở nên rất cao. Kali tiếp tục tăng lên thì PR kéo dài và song P nhỏ lại và biến mất. Tăng kali hơn nữa làm chậm dẫn truyền trong thất , với phức bộ QRS rộng. Nồng độ kali tăng rất cao dẫn đến song hình sin , và vô tâm thu , ngừng tim. Vì tăng kali máu có thể gây tử vong, nên dấu hiệu nhận biết sớm nhất là song T nhọn có thể cứu sống BN. Tăng kali máu có thể nhìn thấy ở nhiều tình huống lâm sàng, suy thận là nguyên nhân phổ biến nhất do không thải trừ được kali.
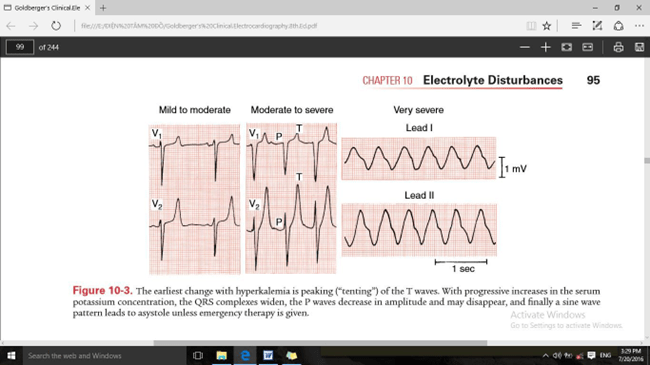
HẠ KALI MÁU
Hạ kali máu có thể thay đổi khoảng STT trên ECG. HÌnh dạng thông thường nhất là ST chênh xuống với sự xuất hiện của song U và kéo dài thời gian tái cực. Sóng U điển hình ngày càng lớn và có thể vượt qua chiều cao của song T nên gây nhầm lẫn. Thay đổi trên ECG không tương xứng với mức độ hạ kali máu
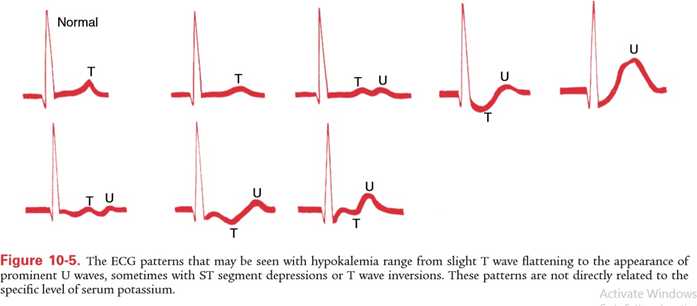
TĂNG CANXI VÀ HẠ CANXI MÁU
Tăng canxi máu gây tái cực thất ngắn , thể hiện trên ECG là QTc ngắn do sự ngắn lại của đoạn ST. Với tăng canxi máu nặng , song T xuất hiện ngay điểm cuối của QRS.Canxi tăng rất cao có thể dẫn đến hôn mê và tử vong. Hạ canxi máu gây QTc dài do kéo dài ST , với hình ảnh ― stretching out ―. Chú ý, tăng canxi và hạ canxi máu có thể có dấu hiệu lâm sàng mà không có thay đổi trên điện tim ,lúc này nên định lượng canxi toàn phần và Ca ion hóa.
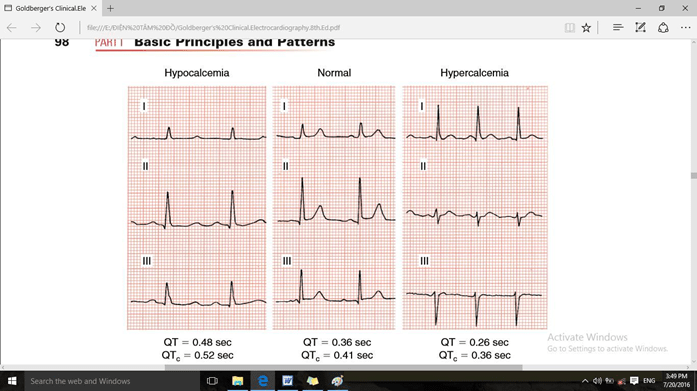
MẤT CÂN BẰNG MAGIE
Tăng và giảm Mg máu quan trọng vì chúng có thể bị bỏ qua và chúng có thể đóng vai trò quan trọng trong cơ chế hình thành loạn nhịp thất và các cân bằng chuyển hóa khác trong cơ thể. Tuy nhiên, chúng thường không có những thay đổi đặc hiệu trên ECG, do đó rất khó chẩn đoán .
Giảm Mg máu do mất qua đường tiêu hóa hoặc thận,vd lợi tiểu có thể đóng vai trò trong cơ chế bệnh sinh làm tăng độ nặng của hạ kali máu. Hạ Mg máu tham gia hình thành loạn nhịp thất sau NMCT cấp và xoắn đỉnh. Thử nghiệm tiêm Mg tĩnh mạch ở BN xoắn đỉnh làm xuất hiện hậu khử cực sớm khởi phát nhịp nhanh thất đa hình. Hạ Mg máu có thể tham gia vào ngộ độc digoxin. Thêm vào đó, hạ Mg máu quan trọng vì nó thường kết hợp với hạ canxi máu do ức chế bài tiết PTH từ tuyến cận giáp.
Tăng Mg máu ( do suy thận hoặc cung cấp quá nhiều ) không làm thay đổi ECG khi tăng nhẹ đến trung bình, có thể PR và QT kéo dài. Tăng Mg máu nặng, 15-20 mmol/L có thể gây ngừng tim. Hạ huyết áp do dãn mạch và thay đổi trạng thái tinh thần có thể gây tăng Mg máu.
CHUYỂN HÓA HẠ THÂN NHIỆT
BN với hạ thân nhiệt toàn thân có thể gây ảnh hưởng lên điện tim với hình ảnh chênh lên ― humplike ―, thường xuất hiện tại điểm J. Sóng J bệnh lý này có tên là song Osborn và
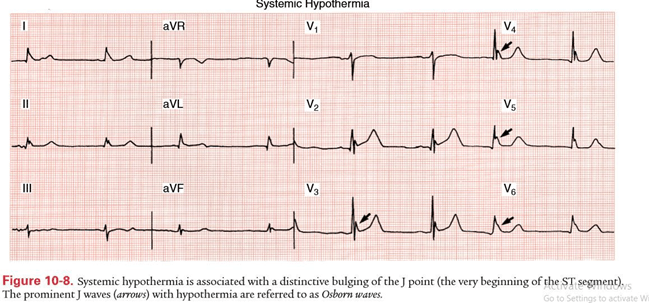
sóng này biến mất khi cơ thể ấm dần trở lại. Cơ chế của song J này là do ảnh hưởng khác nhau của nhiệt độ toàn thân lên
sự tái cực của các lớp khác nhau ở cơ thất.
BẤT THƯỜNG CỦA HỆ NỘI TIẾT
Phần lớn rối loạn nội tiết không có những thay đổi đặc hiệu trên ECG,tuy nhiên ECG đóng 1 vai trò quan trọng trong chẩnđoán và hướng dẫn điều trị bất thường nồng độ hormone. VD như cường giáp hay Grave’s disease thường kết hợp với nhịp nhanh xoang không thích hợp lúc nghỉ. Ngược lại, nhược giáp lại gây ra nhịp chậm xoang lúc nghỉ. Nhược giáp nặng hay phù niêm, có thể dẫn đến tràn dịch màng ngoài tim, biểu hiện điện thế thấp. Điện thế thấp được định nghĩa là tổng biên độ của phức bộ QRS ở chuyển đạo chi nhỏ hơn 5mm, hoặc 10mm ở chuyển đạo trước ngực. Điện thế thấp không đặc hiệu, có thể gây ra bởi không khí ( COPD) , béo phì, tràn dịch màng tim, màng phổi, amyloid, xơ hóa cơ tim…
TOAN VÀ KIỀM
Nhiễm toan hoặc kiềm chuyển hóa, tự bản thân chúng không làm thay đổi ECG, nhiễm toan chuyển hóa điển hình kết hợp với tăng kali máu và nhiễm kiềm chuyển hóa kết hợp với hạ kali máu.
THAY ĐỔI STT : ĐẶC HIỆU VÀ KHÔNG ĐẶC HIỆU
Thuật ngữ thay đổi STT không đặc hiệu được sử dụng phổ biến trong điện tim lâm sàng, nó bao gồm nhiều yếu tố như thuốc, thiếu máu, mất cân bằng điện giải, nhiễm trùng, bệnh phổi…mà có ảnh hưởng đến điện tim. Pha tái cực ( phức hợp STT ) nhạy cảm với nhiều yếu tố và có thể có các thay đổi không đặc hiệu đa dạng do hậu quả của nhiều yếu tố gây nên. Những thay đổi này bao gồm đoạn ST chênh xuống nhẹ, song T dẹt, T đảo nhẹ..
Trái ngược với đó là thay đổi ST đặc hiệu, vd song T cao nhọn trong tăng kali máu, tuy nhiên ngay cả những thay đổi đặc hiệu này vẫn có thể bị nhầm lẫn với nhau, Vd ST chênh lên là đặc điểm của thiếu máu dưới niêm cấp, nhưng chúng cũng có thể bắt gặp ở phình thất, viêm màng ngoài tim và tái cực sớm lành tính BER.
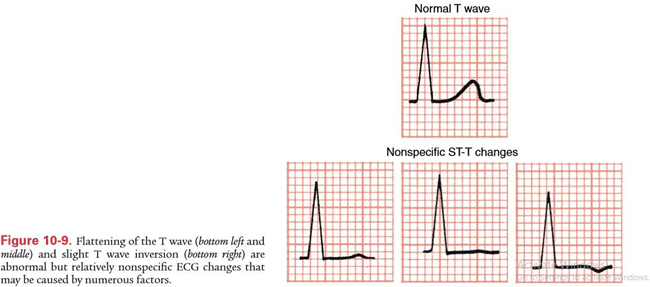
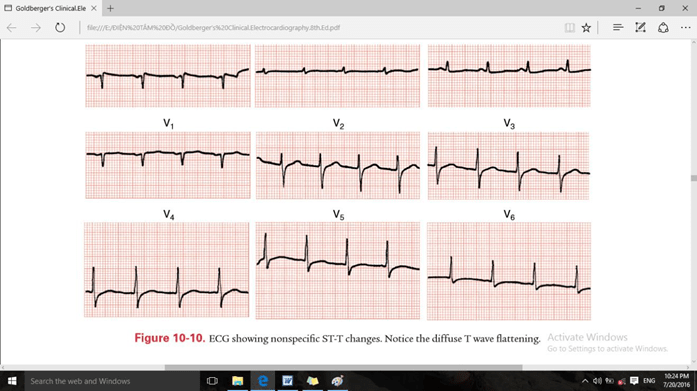
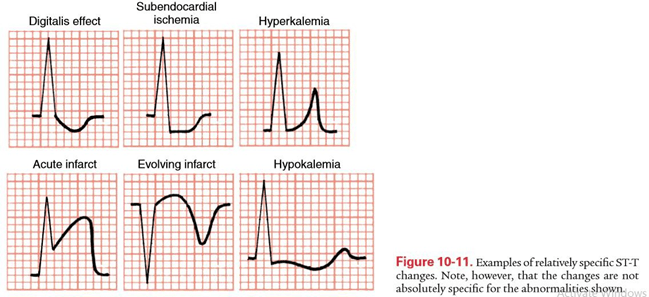
Nguồn : chương 10 Goldberger và chương 13 Harrison tập 3
137. atropine chống chỉ định trong các block 2 II và 3/CHB
Atropine hoạt động bằng cách ức chế các khu vực được chi phối bởi dây thần kinh phế vị. Chúng ta biết các dây thần kinh phế vị chỉ liên kết trực tiếp với nút SA và nút nhĩ thất AV
Lý do atropine được chống chỉ định trong các block 2 II và 3/CHB vì chúng là những block ở dưới nút AV. Block AV1 và 2 1 là block có liên quan nút AV nên có thể hưởng lợi từ việc dùng atropine / phong bế phế vị. 2 mức độ loại II và độ 3 / CHB có liên quan bên dưới nút nhĩ thất.
Hãy tưởng tượng chúng tôi dùng atropine thì nó ức chế phó giao cảm/ phế vị làm tăng SA để tăng AV
o block AV 2 :2 và 3rd/CHB các xung từ nhĩ không xuống thất hoặc hầu hết không xuống thất. đó là lí do vì sao có sóng P mà không gây co tâm thất trong blok AV 2:2 hoặc block AV 3
Nếu chúng ta chỉ tăng tần số nhĩ thì sẽ chẳng có ích lợi gì. Chúng ta cần tăng tần số thất để tăng huyết áp.
Các xung nhĩ không thể đến được tâm thất vì vậy làm nguy cơ tăng nhịp nhĩ làm cho block AV2 dễ chuyển thành độ 3 hoặc độ 3 thành vô tâm thu
138. Cấp cứu bệnh nhân nhịp chậm
Cậu bé 15 tuổi đưa vào phòng cấp cứu bằng xe cứu thương vì ngất. cậu cho biết đang rửa tay ở phòng tắm vào khoảng 04:00 và điều tiếp theo cậu nhớ được là được đưa lên cáng. Trước đây chưa bao giờ bị và có biểu hiện gì bất thường
Gần đây cậu có bị sổ mũi, ho, tức ngực và sốt nhẹ. Được chẩn đoán nhiễm trùng đường hô hấp trên và triệu chứng đã cải thiện.
Lúc vào huyết áp 70/40 mmHg, mạch 36, thở 16 l/ phút, nhiệt độ 37 độ, sp02 98%, glucose 6,6. dấu hiệu sinh tồn của bệnh nhân không thay đổi dù đã truyền dịch. t siêu âm tim thấy suy giảm chức năng tim. Có tăng troponin và bạch cầu. test dương tính với virus Coxsackie.
điện tâm đồ của bệnh nhân (EKG)
Cậu được đặt miếng đệm nhịp qua da và bắt đầu truyền nhỏ giọt dobutamine. Sau đó vào cấp cứu nhi truyền iv immunoglobulin (IVIG) trong 3 ngày. Cậu ra viện sau 1 tuần với chẩn đoán nhịp chậm và suy nút xoang, có thể viêm cơ tim thứ phát do virus.
Bài viết này sẽ đánh giá cách tiếp cận nhịp tim chậm. Trước khi chúng tôi hướng dẫn đánh giá và xử trí bệnh nhân nhịp chậm, cần giới thiệu vài nét cơ bản …
Giới thiệu
Hệ thống dẫn truyền tim bao gồm hệ thống His-Purkinje. xung điện được tạo ra ở nút xoang nhĩ (SA), dẫn truyền xuống nút nhĩ thất (AV) và sau đó xuống tâm thất qua các nhánh bó trái và phải (Hình 1). Nhịp tim bình thường 60-100 bpm. Nhịp chậm khí dưới 60bpm
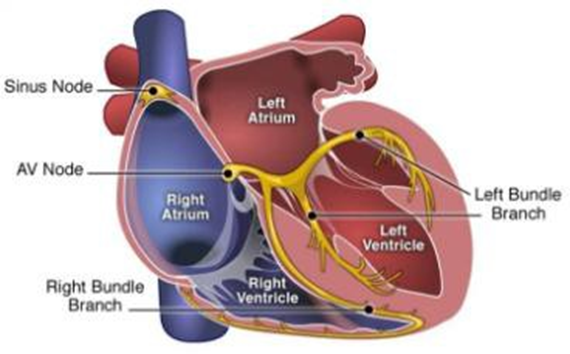
Nhịp tim chậm có thể chai thành hai loại chính: có triệu chứng và không có triệu chứng. Nhịp tim chậm có thể bình thường đặc biệt là ở trẻ em và vận động viên. Một số báo cáo về bệnh nhân không có triệu chứng xuất hiện nhịp chậm được định nghĩa khi mạch <35 bpm. Những bệnh nhân này không cần can thiệp nếu không có triệu chứng
Các dấu hiệu và triệu chứng của nhịp chậm có thể xuất hiện ngất, chóng mặt, đau ngực, khó thở và mệt mỏi. Nhịp chậm có thể dẫn đến suy tim và / hoặc huyết động không ổn định. Khi tiếp cận bệnh nhân nhịp chậm cần tập trung vào tiền sử nếu bệnh nhân có biểu hiện triệu chứng.
Nguyên nhân gây nhịp chậm có rât nhiều: cấu trúc / điện sinh lý, nhiễm khuẩn, nội tiết, ngộ độc /do dùng thuốc và 1 số nguyên nhân khác (Bảng 1).
Table 1 – Etiologies of Bradycardia
|
Category |
Possible Etiologies |
|
Structural/Electrophysiological |
-Sick Sinus Syndrome -AV Block -Ischemia -Congenital Heart Disease -Prior Cardiac Surgery -Cardiomyopathy -Arterial Dissection (Aorta, Coronary, Carotid) |
|
Infectious |
-Myocarditis -Lyme Disease -Bunyavirus -Dengue* -Typhoid Fever* -Legionnaires disease* -Psittacosis* -Leptospirosis* -Malaria* -Babesiosis* -Q fever* -Yellow Fever* -Rocky Mountain Spotted Fever* |
|
Endocrine |
-Hypothyroidism/Myxedema coma -Bamforth syndrome -Hypothalamic dysfunction -Electrolyte Abnormalities/Malnutrition -Hashimoto’s thyroiditis |
|
Toxicology/Iatrogenic |
-Beta blocker** -Calcium channel blocker** -Clonidine** -Guanfacine** -Digoxin** -Lidocaine** -Donepezil** -Organophosphate poisoning -Tacrine -Carbamate insecticide poisoning -Opioid** -Tricyclic Antidepressant Poisoning -Midodrine** -Levetiracetam overdose -Amitraz |
|
Other |
-Heat exhaustion/stroke -Hypothermia -Leukomalacia -Increased Intracranial Pressure – Spinal Cord Injury -Carotid hypersensitivity syndrome -Chromosome 19p duplication syndrome -Fleisher syndrome -Young Simpson syndrome -Asphyxia neonatorum -Pneumothorax -Lupus Carditis -Oculocardiac Reflex -Dexmedetomidine -Prostaglandin |
Tiếp cận nên làm gì?
Điện tâm đồ nên là một trong các xét nghiệm chẩn đoán đầu tiên khi phát hiện nhịp chậm. Ngoài ra, tùy thuộc vào nguyên nhân nghi ngờ, troponin I, BNP, điện giải đồ, tìm nguyên nhân nhiễm khuẩn, X-quang, ct sọ, và siêu âm tim có thể cân nhắc làm.
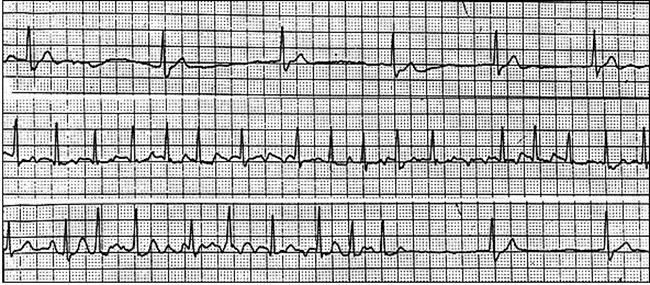 h/c suy nút xoang
h/c suy nút xoang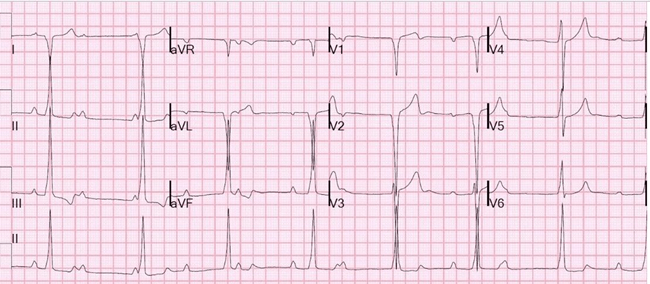
XỬ TRÍ
Như đã đề cập trong phần giới thiệu, không phải tất cả nhịp chậm đều yêu cầu can thiệp, đặc biệt là ở những bệnh nhân khỏe mạnh, không có triệu chứng. Nếu bệnh nhân nhịp chậm có triệu chứng, một trong những điều đầu là vị trí miếng dán qua da. Chuẩn bị để tạo nhịp qua da (cần đặt CVC). Việc xử trí theo ngyên nhân khác nhau được liệt kê trong bảng 1 quá dài và ra khỏi phạm vi của bài viết này. Tham khảo hướng dẫn chung dưới đây
Cấu trúc / điện sinh lý (EP): tìm nguyên nhân bất thường gây cản trở sự dẫn truyền bình thường của tim. Để giải quyết vấn đề này, cần tạo nhịp qua da tạm thời trong khi chờ PCI nếu có STEMI hoặc tạo nhịp vĩnh viễn. siêu âm tim khi nghi ngờ có bất thường về cấu trúc tim
Viêm nhiễm: virus gây viêm cơ tim là một nguyên nhân phổ biến gây nhịp chậm. Viêm cơ tim dẫn đến sự thỏa hiệp về huyết động, đặc biệt trong sốt. Thuốc co mạch, IVIG và ECMO được hướng dẫn điều trị sốc tim thứ phát sau viêm nhiễm (đọc thêm http://www.emdocs.net/pediatric-cardiogenic-shock). Điều trị kháng sinh đặc biệt với những siêu vi như bệnh Lyme.
Nội tiết: rối loạn điện giải và hormon nội tiết cần được xử trí. rối loạn chức năng tuyến giáp cần chú ý khi gặp 1 trường hợp cấp cứu. với bệnh nhân phù niêm có hôn mê (đọc thêm http://www.emdocs.net/myxedema-aka-decompensated-hypothyroidism-an-em- primer). Với các bệnh nhân nhiễm độc giáp và hôn mê có phù niêm cần dùng đường tĩnh mạch t3,t4 dù nó cũng có nguy cơ cao gây rối loạn nhịp tim.
Ngộ độc: xử trí ngộ độc theo từng nguyên nhân không thuộc phạm vi bài viết này. độc tính của thuốc chẹn beta và thuốc chẹn kênh canxi thường được báo cáo. Điều trị bao gồm glucagon, bổ sung canxi, liều cao insulin / glucose và liệu pháp nhũ tương lipid. Đọc thêm http://www.emdocs.net/selected-toxicologic-bradycardias/
Đối với ngộ độc cholinergic và an thần xem thêm tại http://www.emdocs.net/the- approach-to-the-poisoned-patient/
Cần chú ý loạn nhịp tim ở bệnh nhân hạ thân nhiệt.
Đối với nguyên nhân do chấn thương sọ não / thần kinh gây nhịp chậm cần chú ý giảm áp lực nội sọ (ICP) (nằm đầu cao, mannitol, tăng thông khí, 3%NaCl)
Tóm lại
Như đã thấy, xử trí nhịp chậm phụ thuộc vào nguyên nhân nghi ngờ. Không phải tất cả nhịp chậm đều có thể xử trí bằng atropin và tạo nhịp. cần hỏi và khám kỹ để có hướng xử trí phù hợp
Nhìn chung hãy nhớ rằng:
– nhịp chậm khi nhịp tim <60bpm
– nhịp chậm có thể lành tính và không có triệu chứng ECG làm càng sớm càng tốt
– với nhịp tim chậm có triệu chứng, người ta có thể chia nguyên nhân thành 5 loại: cấu trúc / EP, viêm nhiễm, nội tiết, ngộ độc / do thuốc và nguyên nhân khác
biện pháp –trong lúc chờ đợi có thể dùng vận mạch hoặc tạo nhịp. những có thể không hiệu quả ở một số bệnh nhân
139. Cơ chế bệnh sinh một số bệnh kênh ion
GIỚI THIỆU
Bệnh liệt chu kỳ và các rối loạn trương lực cơ là do đột biến gene mã hóa trên các kênh ion sodium, calcium, chloride, gây thay đổi tính kích thích màng tế bào. Hiện nay có 23 loại đột biến trên tiểu đơn vị Alpha kênh Sodium, Calcium cơ xương, gây nên các bệnh kênh ion như: liệt chu kỳ tăng Kali, loạn cứng cơ bẩm sinh, loạn trương lực cơ dao động, loạn trương lực cơ cố định, loạn trương lực cơ đáp ứng vơiù Acetazolamide…Trong nội dung bài này, chúng tôi chỉ trình bày bày một số bệnh đặc biệt.
CHỨC NĂNG VÀ Ý NGHĨA CỔNG ĐIỆN THẾ KÊNH CATION
Màng tế bào gồm 2 thành phần chính là lipid và protein. Protein có nhiều chức năng, trong đó phải kể đến chức năng làm những kênh thụ động đóng mở bằng cách thay đổi cấu hình của phân tử protein. Trong dịch cơ thể các ion ở các ngăn dịch khác nhau có nồng độ khác nhau, thí dụ:
|
Huyết tương mEq/L |
Dịch kẽ mEq/L |
Dịch nội bào mEq/L |
|
|
Na+ |
152 |
143 |
14 |
|
Cl- |
113 |
117 |
|
|
K+ |
5 |
4 |
157 |
|
HCO3 |
27 |
27 |
10 |
|
Protein |
16 |
2 |
7 |
Điện thế màng có được do sự khác biệt số ion dương và âm ở 2 bên màng tạo ra độ sai biệt điện thế, điện thế đo được trong thời điểm này là -90mV đến -65mV tùy theo loại tế bào. Như bảng trên ta đã thấy, nồng độ K+ trong tế bào nhiều hơn ngoài tế bào,
Na+ trong tế bào thấp hơn ngoài tế bào. K+ có khuynh hướng đi ra ngoài tế bào, Na+ đi vào tế bào theo khuynh hướng sai biệt về nồng độ. Sự khuếch tán này vẫn tiếp tục đến khi cân bằng nồng độ nhờ có bơm Na/K-ATPase tại màng có tác dụng bơm Na+ ra ngoại bào và K+ vào trong tế bào. Do đó, bơm Na/K duy trì được sự sai biệt nồng độ Na+ và K+ ở 2 bên màng tế bào, mặc dù sự khuếch tán theo sự sai biệt nồng độ vẫn xảy ra.
Khi bị kích thích, điện thế màng trở nên dương hơn (khử cực), điện thế màng thay đổi rất nhanh đạt đến trị số dương tối đa và sau đó bắt đầu tái cực. Khi tái cực 70%, nhịp tái cực giảm dần, trị số điện thế trở về trị số lúc đầu rất chậm, gọi là giai đoạn khử cực chậm. Khi trở về trị số lúc đầu, điện thế màng còn âm hơn lúc đầu, đó là giai đoạn tăng cực chậm.
Sự thay đổi điện thế khi có kích thích là do sự đóng mở các kênh ion nhạy cảm với điện thế điều hòa dòng Na+ đi vào và dòng K+ đi ra tế bào.
Khi trị số điện thế màng đạt đến ngưỡng, điện thế cho phép mở các kênh ion. Kênh Na+ có 3 trạng thái: trạng thái nghỉ- cửa đóng; trạng thái bị kích hoạt- cửa kích hoạt mở, Na+ vào tế bào cho tới khi kênh bị đóng bởi cửa bất hoạt; trạng thái bị bất hoạt- cửa bất hoạt đóng. Cửa này lệ thuộc thời gian và độc lập với cửa kích hoạt. Sự mở các kênh Na+ càng nhiều, khử cực càng nhanh.
Khi điện thế màng đến ngưỡng, kênh Kali nhạy cảm điện thế cũng mở, K+ ra ngoài tế bào. Kênh K+ đóng không lệ thuộc thời gian mà chỉ lệ thuộc điện thế.
Ơû điện thế động, màng có tính thấm nhiều với Na+ hơn K+. sau đó kênh Na+ bất hoạt và đóng, Na+ không vào tế bào nữa và gây tái cực. Lúc này tính thấm đối với K+ cao hơn đối với Na+. Sự mở kênh K+ gây dòng K+ ra ngoài qúa lâu làm điện thế màng vẫn giữ tăng phân cực trước khi trở về bình thường.
Tín hiệu lan truyền dọc hệ thống ống ngang, hoạt hóa kênh Ca++ Dihydro- pyridine, phóng thích Ca+ + nội bào và cơ co lại do tương tác trực tiếp protein-protein với sự phóng thích Ca++. Đột biến trên những kênh này dẫn tới sự qúa kích thích hay không kích thích phụ thuộc vào sự thiếu sót chức năng nào, kết quả là liệt (không kích thích), hay loạn trương lực cơ (qúa kích thích).
Kênh cation nhạy cảm điện thế ít nhất là 1 mở, 2 đóng. Trong bệnh liệt chu kỳ sự bất hoạt kênh Cation bị xáo trộn, gây nên đóng & mở kênh không hoàn chỉnh.
DẤU HIỆU LÂM SÀNG CỦA LIỆT CHU KỲ TĂNG KALI VÀ HẠ KALI.
Bệnh cơ di truyền, di truyền theo tính trội, xuất độ khoảng 1/100.000 dân, đặc điểm yếu liệt mềm với thời gian, độ trầm trọng & tần xuất khác nhau. Cơn thường xảy ra trong lúc nghỉ sau giai đoạn làm việc nặng. Duy trì hoạt động thể lực nhẹ nhàng có thể trì hoản hay ngăn ngừa cơn. Liệt cơ thường ở gốc chi dưới, và lan dần đến ngọn chi trên. Cơ trục thân, vai cổ, hầu họng, thanh quản, hô hấp, cơ vòng ít bị ảnh hưởng. Dấu hiệu liệt hồi phục sau 1 giờ (loại tăng Kali), đến vài giờ (loại hạ Kali), cùng với bình thường
hóa nồng độ Kali trong máu. Trời lạnh, căng thẳng rối loạn cảm xúc, mang thai có thể gây xuất hiện bệnh hay làm tình trạng bệnh nặng nề hơn. Tuổi khởi phát vào 10-20 tuổi.
Yếu cơ dần dần có thể phát triển thành bệnh cơ, không lệ thuộc vào số cơn, hầu hết khởi phát sau 40 tuổi. Đặc điểm mô học của bệnh cơ này là có các không bào trung tâm trong sợi cơ, lưới bào tương dãn rộng và tăng sản.
Liệt chu kỳ loại tăng và hạ Kali do thay đổi nồng độ Kali trong huyết thanh, còn do các test gây triệu chứng. Uống Kali và đường gây triệu chứng cho bệnh nhân liệt chu kỳ tăng Kali, ngược lại đường (và insulin) gây triệu chứng cho bệnh nhân liệt chu kỳ hạ Kali.
Yếu cơ trong liệt chu kỳ tăng Kali có thể biểu hiện với 2 loại loạn trương lực cứng cơ khác nhau: loạn trương lực cơ (Myotonia), có thể cải thiện khi tập thể dục, và có thể yếu cơ tạm thời trong khi cử động nhanh cơ trong nhiều giây. Co giật cứng cơ (Paramyotonia) nặng hơn khi trời lạnh hay tập thể dục, yếu cơ kéo dài nhiều giờ đến nhiều ngày. Ngược lại không có loạn trương lực cơ trong liệt chu kỳ hạ Kali.
ĐỘT BIẾN GENE TRONG LIỆT CHU KỲ TĂNG VÀ HẠ KALI
Bệnh liệt chu kỳ tăng và hạ Kali do đột biến gene trong tiểu đơn vị Alpha kênh điện thế Cation, gây nên sự thay đổi các Acid amin của Protein. Tiểu đơn vị Alpha gồm 4 khối chức năng (đánh số I-IV), mỗi khối có 6 chuỗi peptid, có cấu hình xoắn Alpha (đánh số S1-S6). Chúng được nối với nhau bởi các quai nội bào và ngoại bào. Tiểu đơn vị Alpha chứa lỗ nối kết ion, xác định tính chất chính của kênh (thí dụ kênh nhạy cảm ion, nhạy cảm điện thế…). Kênh Cation nhạy cảm điện thế đặt ở vị trí peptide S4, protein kênh đơn, di chuyển ra ngoài, xoay và mở kênh. Trong khi đóng kênh không phải tất cả các yếu tố nhạy cảm đều quay trở lại lúc đầu tức khắc. Điều này gây ra sự thay đổi ở tình trạng đóng, giải thích sự đột biến ở vài vị trí gây ra các kiểu hình bệnh khác nhau. Lỗ nối kết ion đặt ở peptide S5-S6 khối IV. Cổng hoạt hóa hầu như đặt ở các lỗ, ngược lại cổng bất hoạt có thể đặt ở vị trí khác trong kênh Na+ và K+( nối khối III- IV).
Liệt chu kỳ hạ Kali type I, chiếm 35% các trường hợp bệnh liệt chu kỳ, do đột biến 1 trong 3 loại ở khối II và IV tiểu đơn vị Alpha kênh Ca++. Sự đột biến gene ở vị trí 1239 DIV/S4, thay thế Arginin bằng Histidine hay Glycin, vị trí 528 DII/S4 thay thế Arginin bằng Histidine.
Liệt chu kỳ hạ Kali type II, chiếm 5% trường hợp, do đột biến khối chức năng DII/S4 của tiểu đơn vị Alpha kênh Na+, vị trí 669, thay thế Arginine bằng Hitidine. sự khác biệt trên lâm sàng 2 loại trên khó phân biệt. Một số bệnh nhân type II không dung nạp thuốc Acetazolamide, trên sinh thiết cơ thấy hiện tượng kết tập khối ống ngang trong một số bệnh nhân. Mặc khác, bệnh nhân liệt chu kỳ tăng Kali có đột biến gần màng dưới của tiểu đơn vị Alpha kênh Na+, phát hiện hơn 50% các trường hợp.
Mặc dù tình trạng bất hoạt của kênh Na+ là kém ổn định trong bệnh LCK tăng Kali, nhưng nó vẫn ổn định trong LCK hạ Kali type 2. Biểu hiện chức năng của đột biến trong LCK hạ Kali type 2 là giảm biên độ, giảm ngưởng điện thế cho cung bất hoạt,
chậm sự hồi phục từ tình trạng bất hoạt nhanh. Tất cả sự thay đổi này làm giảm số lượng kênh Na+ sẵn sàng cho sự lan truyền và phát sinh điện thế hoạt động chuẩn bị cho sự khử cực. Và yếu tố thúc đẩy là do sự giảm dẫn truyền kali, kích thích bơm Na+/K+, dẫn tới bất hoạt kênh Na+ và yếu cơ.
LCK hạ Kali type 1 do đột biến kênh Ca++, làm giảm biên độ dòng điện, giảm nhẹ ngưởng điện thế bất hoạt, chậm tốc độ hoạt hóa. Sự thay đổi dòng Ca++ (giảm phóng thích dòng Ca++) liên quan với hạ Kali dẫn tới yếu cơ có thể do sự giảm hoặc không kích thích thần kinh trong cơn liệt.
LIỆT CHU KỲ: THAY ĐỔI KÊNH K+
Kênh K+ gồm 4 tiểu đơn vị Alpha (và tiểu đơn vị phụ Beta). Tiểu đơn vị Alpha trong kênh K+ bao gồm 1 khối có 6 màng peptide, tương ứng với 1 khối tiểu đơn vị Alpha của kênh Na+ và Ca++. Đột biến R83H trong MiRP2, tiểu đơn vị Beta của kênh Kv3,4, được ghi nhận trong LCK gia đình không phân loại. Có 2 gia đình tìm thấy sự đột biến này. Nồng độ Kali trong máu bình thường trong cơn. Yếu cơ không xảy ra khi truyền insulin/glucose, và uống Kali cũng không cải thiện bệnh. Mặc dù kiểu bệnh đầu tiên tìm ra gần liên quan với LCK hạ Kali hơn là tăng Kali, nhưng xếp loại chính xác vẫn còn đang bàn cải.
HỘI CHỨNG ANDERSEN
HC Andersen được định nghĩa là bệnh liệt chu kỳ nhạy cảm kênh Kali, gồm tam chứng trên lâm sàng:bất thường tim mạch, dấu hiệu biến hình, liệt. Dấu hiệu biến hình có thể thay đổi, gồm dáng người nhỏ, lỗ tai thấp, giảm sản hàm dưới, ngón tay dính, vẹo cột sống. Rối loạn tim mạch như QT kéo dài, nhịp đôi, nhanh thất. Đột tử trong hội chứng này có lẽ do ngưng tim. Tương tự như LCK hạ Kali, loạn trương lực cơ không có trong hội chứng này. Khác với bệnh nhân LCK hạ và tăng Kali, đáp ứng với uống Kali thường thay đổi: cải thiện yếu cơ nếu hạ kali, tuy nhiên vài gia đình cải thiện nhịp tim, nhưng làm trầm trọng yếu cơ. Trong cơn, kali trong huyết thanh có thể thấp, cao, trung bình.
Có vài đột biến trong tiểu đơn vị Alpha nhạy cảm điện thế của kênh Kali trong cơ xương và cả cơ tim. Tiểu đơn vị này gồm protein trong 2 màng peptide (M1 và M2) và nối lỗ dẫn truyền ion. Chức năng là chỉnh lưu nhập bào kali, duy trì điện thế nghỉ. Đột biến trong hội chứng này làm giảm dòng Kali, rối loạn dẫn truyền.
LIỆT CHU KỲ VỚI TĂNG NĂNG TUYẾN GIÁP
Đây là một thể của liệt chu kỳ hạ kali thứ phát. Bệnh xảy ra chủ yếu ở tuổi trưởng thành, phái nam trội hẳn hơn phái nữ. Tại Nhật, Okinaka phát hiện 8,9% nam cường giáp trạng có liệt chu kỳ , nhưng chỉ có 0,4% là nữ. Tại Trung quốc 13% nam, 0,17% nữ.
Bệnh ưu thế những người châu Á,có nguồn gốc Nhật bản, Trung hoa, Singapore. Tuy nhiên xuất độ thấp 1,8-8,8% ở Nhật; 1,9% ở Trung Quốc đối với bệnh nhân cường giáp. Ơû Bắc Mỹ, xuất độ là 0,1- 0,2%. Xuất độ liệt chu kỳ hạ Kali ở bệnh nhân cường giáp ở Nhật năm 1991 so với năm 1957 giảm >40%. Lý do có thể vì sự thay đổi chế độ ăn ít carbohydrate, giàu potassium hơn. Bệnh xảy ra theo mùa: mùa lạnh từ tháng 12- tháng 3 nhiều hơn tháng có khí hậu ấm tháng 5-10. Vào mùa hạ nóng bức, người bệnh khát nước, thường uống lạnh có đường cũng dễ gây ra triệu chứng.
Tình trạng liệt không liên quan với độ trầm trọng của cường giáp. Có thể nói cường giáp không làm tăng tần suất hay độ nặng của bệnh.
Triệu chứng lâm sàng giống liệt chu kỳ hạ kali gia đình , ngoại trừ nguy cơ bất thường về tim mạch cao hơn. Triệu chứng yếu cơ chi, thân từ nhẹ đến nặng, kéo dài vài phút đến vài giờ, hay 1-2 ngày. Triệu chứng thần kinh sọ hiếm xảy ra.
Trong nghiên cứu của Singapore, người ta nhận thấy có 88,5% bệnh nhân xuất hiện liệt giữa 6 giờ chiều và 8 giờ sáng. Liệt mềm cơ ở thân, vai, hông chậu, gốc chi nặng hơn ngọn chi, chi dưới nặng hơn chi trên Bệnh nhân cũng thường đau, cứng cơ. Cảm giác, tâm thần không bị ảnh hưởng.
Trong nghiên cứu củaMCFadzean và Yeung, ông nhận xét thấy biểu hiện cường gíap có trước triệu chứng liệt từ 3 tháng đến 9 năm trong 80% trường hợp, nên triệu chứng cường giáp hầu như rất rõ ràng tại thời điểm bệnh nhân liệt. Tuy nhiên trong nghiên cứu khác, cường giáp chỉ phát hiện qua làm xét nghiệm chức năng tuyến giáp mà thôi.
Trong nhóm bệnh nhân này, hoạt động bơm Na+/K+-ATPase cao hơn người bình thường và bệnh cường giáp nhưng không có triệu chứng liệt chu kỳ.
Không giống như bệnh LCK hạ kali nguyên phát, nó thường không liên quan đến yếu tố gia đình. Nhưng người ta thấy gene HLA-DRw8 đóng vai trò có ý nghĩa trong nhóm bệnh nhân này ở Nhật. Trong 1 cặp sinh đôi một trứng, với 1 người bị viêm tuyến giáp, và 1 người thì bị LCK. Ơû Trung Quốc, người ta tìm thấy kháng nguyên HLA-A2BW22 và AW19B17 trên bệnh nhân LCK tăng năng tuyến giáp, nhưng ngược lại không tìm thấy ở người da đen.
Điều trị cường giáp giúp ngăn ngừa cơn liệt tái phát. Tỉ lệ liệt cơ tái phát cao trong vòng 1 tháng đầu sau điều trị bình giáp. Dùng potassium phòng ngừa dường như không hiệu quả ngừa cơn.
140. Hội chứng tiền kích thích và giải phẫu hệ thống đường phụ ( accessory pathway )
I. Định nghĩa:
Hội chứng tiền kích thích ( pre – excitation syndrome) là tình trạng khử cực quá sớm của tâm thất dẫn đến co bóp một phần của tâm thất)
II. Sinh bệnh học:
Bình thường, tâm nhĩ và tâm thất cách li nhau về điện thế, vách nhĩ thất ngăn cách 2 buồng được xem như vành đai trắng ( vòng xơ nhĩ – thất ), chỉ một đường đi qua vành đai là nút nhĩ thất và bó His rất quan trọng trong dẫn truyền nhĩ thất.
Trong tất cả hội chứng tiền kích thích giữa nhĩ và thất bên cạnh bó His còn tồn tại một đường khác nối nhĩ và thất.
Theo sinh lí, sóng điện thế bình thường bị trì hoãn tại nút nhĩ thất cho phép tâm nhĩ co bóp trước tâm thất. tuy nhiên không có sự trì hoãn như vậy khi điện thế được dẫn truyền qua đường bất thường ( đường phụ ), vì vậy sự dẫn truyền qua đường phụ nhanh hơn qua hệ thống nút nhĩ thất/bó his ( atrioventricular/bundle of His system), vì vậy thất khử cực sớm hơn khi qua hệ thống dẫn truyền bình thường.
III. Phân loại:
Có vài type khác nhau của hội chứng tiền kích thích với các đặc điểm khác nhau được mô tả:
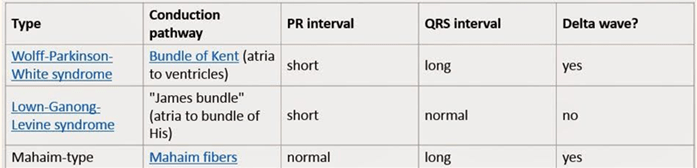
Các đường phụ liên quan hội chứng tiền kích thích:
Giải phẫu đường phụ:
A = atriofascicular B = nodofascicular
C = nodoventricular* D = fasciculoventricular
E = atrioventricular
*first described by Mahaim
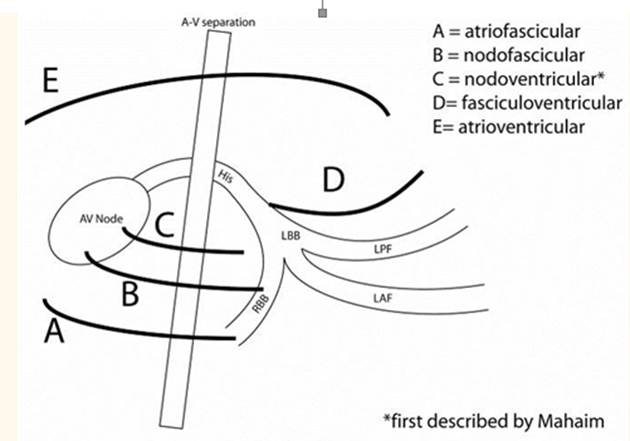
A. Đường phụ nối trực tiếp tâm nhĩ – bó ( ở đây hiểu bó là hệ thống dẫn điện của tâm thất có thể là bó his, phân nhánh phải, phân nhánh trái trước trên hoặc phân nhánh trái sau dưới )
B: Đường phụ nối trực tiếp từ nút nhĩ thất – bó. C: Đường phụ nối trực tiếp từ nút nhĩ thất
D: Đường phụ nối trực tiếp từ bó vào cơ thất. E: Đường phụ nối trực tiếp tâm nhĩ và tâm thất.
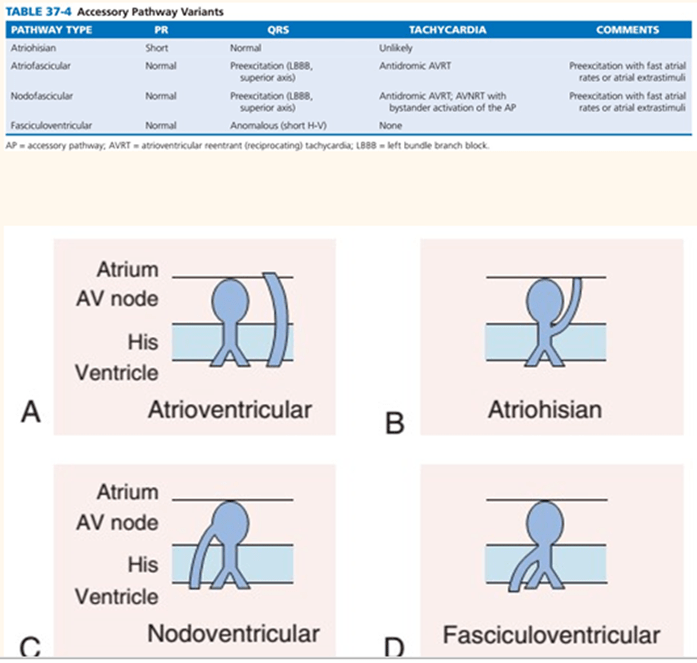
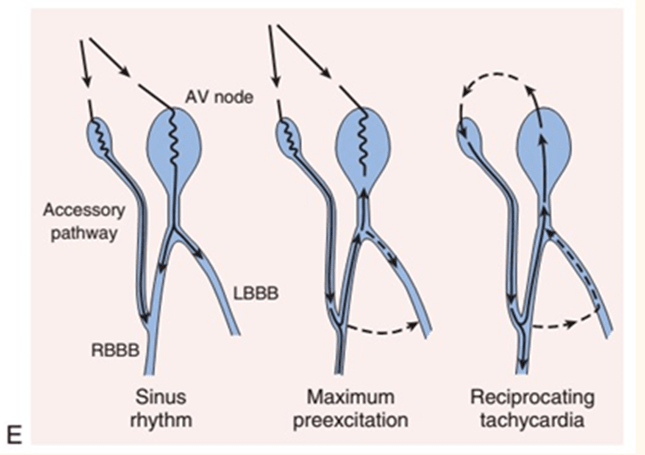
Hình A: là đường phụ nối tâm nhĩ và tâm thất ( AV accessory ) còn gọi là cầu Kent thường biểu hiện lâm sàng của nhịp nhanh liên quan hội chứng Wolff – Parkinson – White.
Hình B: là đường phụ nối tâm nhĩ với bó His ( Atriohisian ) còn gọi là sợi James, thuộc đường phụ kiểu A atriofascicular đã mô tả ở trên biểu hiện lâm sàng là hội chứng Low – Ganong – Levin có đặcđiểm là khoảng PR ngắn trên điện tâm đồ.
Hình C, Hình D: như đã mô tả ở trên, các đường này là các sợi gọi là sợi Mahaim liên quan type Mahaim của hội chứng tiền kích thích.
Hình E: đường phụ nối trực tiếp nút – bó có đặc tính như trong hội chứng WPW ở hình
A. Ngoài ra nó còn liên quan tới nhịp nhanh hỗ tương nhĩ thất hay nhịp nhanh vào lại nhĩ thất( reciprocating/re-entrant tachycardia ) sẽ mô tả ở bài khác.
Một số đường phụ trong các đường phụ đã mô tả có vai trò quan trọng trong tạo ra cơ chế nhịp nhanh trên thất ( supraventricular tachycardia ). Tính chất của đường phụ và nhịp nhanh này sẽ được trình bày trong một bài riêng.
References:
http://en.wikipedia.org/wiki/Pre-excitation_syndrome
Braunwald’s Heart Disease – A Textbook of Cardiovascular Medicine 10th 2015
141. Cơ chế nhịp nhanh vào lại nút nhĩ thất (mechanism of atrioventricular nodal reentrant tachycardia)
Nhịp nhanh vào lại nút nhĩ thất (AVNRT) hầu như là nguyên nhân phổ biến nhất của nhịp nhanh trên thất nhịp đều kịch phát, chiếm khoảng ½ hoặc hơn tổng số ca nhịp nhanh trên thất được chẩn đoán bởi điện sinh lí. Mặc dù nhịp nhanh vào lại nhĩ thất có thể xuất hiện ở bất cứ lứa tuổi nào, hầu hết các bệnh nhân có lần đầu tiên trong độ tuổi 40 và 50. 70 % loạn nhịp này là nữ.
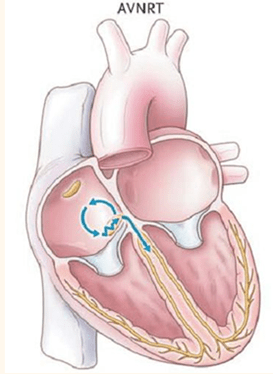
Ở những bệnh nhân với AVNRT có ít nhất hai đường dẫn truyền khác biệt về chức năng. Một đường nhanh đặc trưng bởi tốc độ dẫn truyền nhanh và thời kì trơ kéo dài. Đường thứ hai là đường chậm điển hình với tốc độ dẫn truyền chậm và thời kì trơ ngắn.
Trong suốt nhịp xoang, dẫn truyền qua qua nút nhĩ thất đến thất xảy ra qua đường nhanh Hình 1
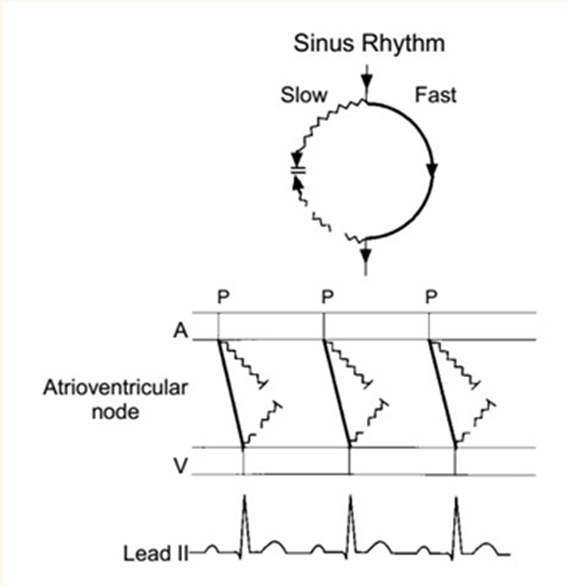
Hình 1
Vào lại nút nhĩ thất điển hình bắt đầu bởi sự khử cực sớm nhĩ trong lúc dẫn truyền xuôi chiều đi xuống của đường nhanh bị block do thời kì trơ kéo dài trong khi đó dẫn truyền trực tiếp xuôi chiều 1 cách chậm qua đường chậm. Nếu dẫn truyền xuôi chiều qua đường chậm đủ chậm để thời kì trơ của của đường nhanh đủ kết thúc. Khi đó xung xuôi chiều qua đường chậm có thể dẫn truyền ngược chiều qua đường nhanh trở lại nhĩ, vì vậy gây ra vòng vào lại. Hình 2
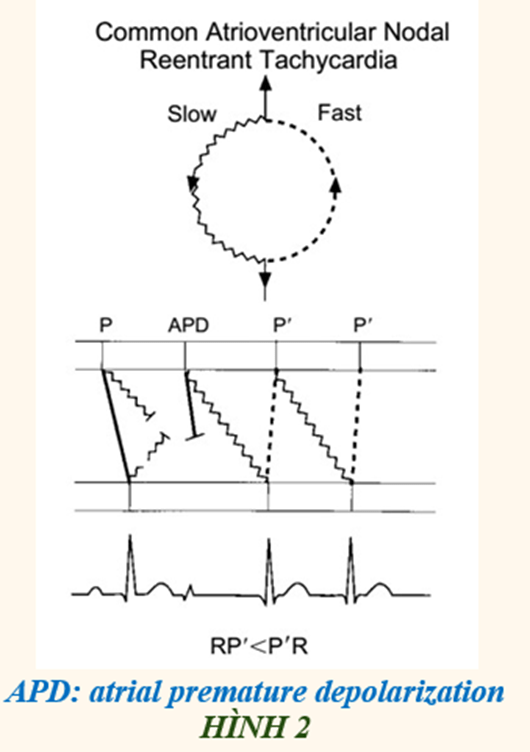
Nhịp nhanh vào lại nút nhĩ thất là phổ biến, như vừa mô tả, là do vòng vào lại trong đó dẫn truyền xuôi dòng qua đường nút nhĩ thất chậm và dẫn truyền ngược
chiều qua đường nhanh. Bời vì dẫn truyền xuôi dòng qua qua bó His và sau đó đến các nhánh bó đến thất xảy ra cùng thời điểm dẫn truyền dẫn truyền ngược chiều qua đường nhanh đến nhĩ, có một sự ghi đồng thời hoặc gần đồng thời của sóng P và phức bộ QRS trên ECG. Hình 2 ECG không thấy sóng P do bị lẫn vào trong sóng QRS do sự ghi đồng thời trên ECG.
Khoảng 10 % nhịp nhanh vào lại nút nhĩ thất không phổ biến, có sự đảo ngược của vòng vào lại, nghĩa là dẫn truyền xuôi dòng đường nhanh và ngược chiều theo đường chậm, đặc trưng bởi nhìn thấy rõ sóng P đảo ngược trên ECG chuyển đạo II, III, aVF do và khoảng RP trong nhịp nhanh kéo dài hơn PR. Loại nhịp nhanh vào lại nút nhĩ thất này thường bắt đầu bởi khử cực sớm thất và hiếm khi duy trì lâu. Hình 3
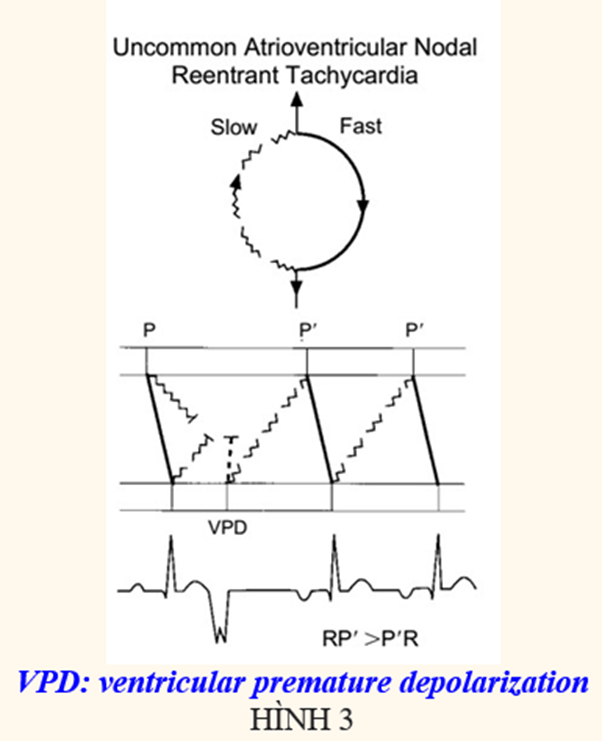
142. Kháng đông đường uống nào dùng cho rung nhĩ ?
Warfarin
Ở bệnh nhân rung nhĩ không do van tim, warfarin làm giảm nguy cơ đột quỵ do thuyên tắc huyết khooisleen đến 60%. Nếu cần thiết, có thể sử dụng vitamin K, prothrombin hoặc huyết tương tươi đông lạnh để làm đảo ngược tác dụng kháng đông của nó. Điều trở ngại của warfarin bao gồm liều không thể dự đoán trước được và hay thay đổi, giới hạn bởi chế độ ăn, tương tác với nhiều thuốc khác, và cần theo dõi chặt chẽ để giữ INR 2 – 3.
Kháng đông trực tiếp đường uống.
Ức chế trực tiếp thrombin: dabigatran etexilate (Pradaxa) và Ức chế trực tiếp yếu tố Xa: apixaban (Eliquis), edoxaban (Savaysa), và rivaroxaban (Xarelto) không yêu cầu theo dõi thường quy thời gian đông máu và tương tác thuốc ít hơn warfarin ( bảng 1).
Điều trở ngại của kháng đông trực tiếp đường uống bao gồm không có phương pháp theo dõi hiệu quả kháng đông của chúng, thời gian bán hủy ngắn làm tăng nguy cơ huyết khối nếu quên uống thuốc, thiếu dữ liệu về cách sử dụng trên bệnh nhân bệnh thận giai đoạn cuối và giá cả cao.
Hiệu quả:
Trong các thử nghiệm then chốt giữa kháng đông trực tiếp đường uống với warfarin để FDA chấp nhận đưa vào sử dụng, tất cả kháng đông trực tiếp đường uống đều có hiệu quả không thấp hơn warfarin trong phòng ngừa đột quỵ hoặc thuyên tắc hệ thống ở bệnh nhân rung nhĩ. Ở bệnh nhân uống warfarin, INR trong khoảng điều trị chỉ đạt 55 – 65% thời gian. Edoxaban ít hiệu quả hơn warrfarin trong phòng ngừa đột quỵ và thuyên tắc hệ thống ở bệnh nhân có độ thanh thải creatinine >95 ml/phút; nó hiệu quả hơn nếu độ thanh thải creatinine 58 – 80 ml/phút.
Chảy máu:
Tất cả kháng đông trực tiếp đường uống có tỉ lệ thấp hơn đáng kể xuất huyết nội sọ và đột quỵ xuất huyết não hơn so với warfarin trong các thử nghiệm lâm sàng then chốt (bảng ). So sánh với warfarin, tỉ lệ xuất huyết nặng với dabigatran và rivaroxaban thì tương tự nhau và tỉ lệ với apixatran và endoxaban thì thấp hơn đáng kể.
Tính đảo ngược hiệu quả kháng đông:
Năm 2015, FDA chấp nhận idarucizumab (Praxbind) để đảo ngược khẩn cấp hiệu quả kháng đông của dabigatran8. Không có antidote nào có sẵn ở Mỹ cho ba thuốc kháng đông trực tiếp yếu tố Xa, nhưng một nghiên cứu ở các tình nguyện viên khỏe mạnh, một sản phẩm tổng hợp được khảo sát (andexanet alfa) đảo ngược hiệu quả kháng đông của apixaban và rivarixaban trong vài phút 9. Kết quả của một vài nghiên cứu chỉ ra rằng hiệu quả kháng đông của tất cả kháng đông trực tiếp đường uống có thể dảo ngược bởi phức hợp prothrombin đậm đặc10.
|
Bảng 1: Kháng đông đường uống dùng cho rung nhĩ |
|||
|
Tên thuốc |
Liều dùng |
Lưu ý |
|
|
Ức chế trực tiếp yếu tố Xa |
|||
|
Apixabanb –Eliquis (BMS) |
5 mg hai lần/ngàyc |
Tương tác chất ức chế và cảm ứng của CYP3A4 và P – gpd |
|
|
Endoxabanb-savaysa (Daiichi Sankyo) |
60 mg một lần/ngàye |
Không nên sử dụng ở bệnh nhân với độ thanh thải creatinine >95ml/phút; tránh sử dụng với rifampin cảm ứng P – gp |
|
|
Rivaroxabanb-Xarelto (Janssen) |
20 mg một lần/ngàyf |
Nên uống với bữa ăn tối; Tương tác chất ức chế và cảm ứng của CYP3A4 và P – gpg |
|
|
Ức chế trực tiếp thrombin |
|||
|
Dabigatran etexilateb- Praxada (Boehringer Ingellheim) |
150 mg hai lần/ngàyh |
Phải được phân phối và bảo quản trong hộp chứa của nhà sản xuất, một khi đã khui sản phẩm, phải sử dụng trong vòng 4 tháng; Tương tác chất ức chế và cảm ứng của CYP3A4 và P – gpi; viên thuốc không nên bẻ nhỏ, nghiền hoặc nhai; rối loạn tiêu hóa thường gặp; reversal agent avalable, có thể thẩm tách được. |
|
|
Kháng Vitamin K |
|||
|
Warfarin – generic |
2 – 10 mg một lần/ngàyj |
Tương tác với nhiều loại thuốc khác, bị giới hạn bởi chế độ ăn uống |
|
|
Coumadin (BMS) |
Theo dõi INR; có thể đảo ngược được tác dụng kháng đông. |
||
|
Viết tắt: INR international normalized ratio; P – gp P – glycoprotein. agiá điều trị trong vòng 30 ngày ở liều thông thường thấp nhất. Giá này được công bố bởi nhà sản xuất đến toàn bộ đơn vị bán thuốc. bFDA chấp nhận sử dụng ở bệnh nhân rung nhĩ không do van. cLiều 2.5 mg 2 lần/ngày cho bệnh nhân có >= 2 yếu tố sau: >=80 tuổi, <=60kg, creatinine huyết thanh >=1.5 mg/dl dỞ bệnh nhân uống thuốc ức chế mạnh cả CYP3A4 và P-gp, giảm liều apixaban 50% xuống còn 2.5 mg 2 lần/ngày. Tránh sử dụng với chất cảm ứng (inducers) cả CYP3A4 và P-gp. eLiều 30 mg một lần/ngày cho bệnh nhân có độ thanh thải creatinine 15 – 50 ml/phút. Không khuyến cáo sử dụng cho bệnh nhân với độ thanh thải creatinine <15ml/phút. |
fLiều 15 mg một lần/ngày cho bệnh nhân có độ thanh thải creatinine 15 – 50 ml/phút. Không khuyến cáo sử dụng cho bệnh nhân có độ thanh thải creatinine <15ml/phút. gTránh sử dụng cới chất ức chế hoặc cảm ứng mạnh CYP3A4 và P-gp. h The American College of Chest Physicians and Health Canada không khuyến cáo sử dụng cho bệnh nhân rung nhĩ với độ thanh thải creatinine <30ml/phút. Nhãn hiệu của Mỹ khuyến cáo liều 75mg 2 lần/ngày ở bệnh nhân với độ thanh thải creatinine 15 – 30 ml/phút; liều này dựa trên mẫu dược lực học và không có nghiên cứu thử nghiệm nào. iTránh sử dụng với chất cảm ứng P-gp. Liều nên giảm còn 75 mg 2 lần/ngày trong quá trình sử dụng chung với dronedarone hoặc ketoconazone toàn thân ở bệnh nhân có độ thanh thải creatinine 30 – 50 ml/phút. Tránh sử dụng với chất ức chế P-gp ở bệnh nhân có độ thanh thải creatinine 15 – 30 ml/phút. Nên sử dụng với kháng đông ngoài đường uống >= 5 ngày và tới khi INR đạt 2 – 3 >=24 giờ. |
||
Kết luận:
Các loại kháng đông trực tiếp đường uống dabigatran (Praxada), apixaban (Eliquis), endoxaban (Savaysa), và rivaroxaban (Xarelto) có hiệu quả ít nhất cũng ngang bằng với warfarin (coumadin và các thuốc khác ) trong phòng ngừa đột quỵ cũng như thuyên tắc hệ thống ở bệnh nhân rung nhĩ không do van, và các thuốc này an toàn hơn. Bệnh nhân kiểm soát tốt với warfarin (INR ổn định ở khoảng điều trị) có thể tốt hơn các loại thuốc này, các trường hợp còn lại thì chọn một thuốc kháng đông trực tiếp đường uống. chưa có thử nghiệm so sánh trực tiếp giữa các thuốc kháng đông trực tiếp đường uống.
REFERENCES
1. Hart RG, Pearce LA, Aguilar MI. Meta-analysis: antithrombotic therapy to prevent stroke in
patients who have nonvalvular atrial fibrillation. Ann Intern Med. 2007;146(12):857- 867.
2. Kcentra: a 4-factor prothrombin complex concentrate for reversal of warfarin anticoagulation. Med Lett Drugs Ther. 2013;55(1420):53-54.
3. Connolly SJ, Ezekowitz MD, Yusuf S, et al;RE-LY Steering Committee and Investigators. Dabigatran versus warfarin in patients with atrial fibrillation.N Engl J Med. 2009;361(12):1139-1151.
4. Patel MR, Mahaffey KW, Garg J, et al; ROCKET AF Investigators. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med. 2011; 365(10):883-891.
5. Granger CB, Alexander JH, McMurray JJ, et al; ARISTOTLE Committees and Investigators. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011;365(11):981-992.
6. Giugliano RP, Ruff CT, Braunwald E, et al; ENGAGE AF-TIMI 48 Investigators. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2013;369(22):2093-2104.
7. US Food and Drug Administration. FDA draft briefing document for the Cardiovascular and Renal Drugs Advisory Committee on October 30, 2014: NDA 206316. http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMate rials/Drugs/CardiovascularandRenalDrgsAdvisoryCommittee
/UCM420704.pdf. Accessed March 31, 2016.
8. Idarucizumab (Praxbind)—an antidote for dabigatran. Med Lett Drugs Ther. 2015;57(1482):
157-158.
9. Siegal DM, Curnutte JT, Connolly SJ, et al. Andexanet alfa for the reversal of factor Xa inhibitor
activity. N Engl J Med. 2015;373(25):2413-2424.
10. Kalus JS. Pharmacologic interventions for reversing the effects of oral anticoagulants. Am J Health Syst Pharm. 2013;70(10)(suppl 1):S12-S21.
143. Thuốc chẹn Beta có tác dụng gì trong ngất do phản xạ phế vị?
Nhiều nghiên cứu cho thấy dùng beta adrenergic blockers có vai trò trong việc kiểm soát tần số và mức độ của ngất do phản xạ phế vị
Người ta có thể tự hỏi làm thế nào một loại thuốc chống adrenergic lại có thể chống lại việc tăng phản xạ phế vị!
Điều này là do trong ngất do cường phế vị, ban đầu có sự kích thích giao cảm. Sự tăng đột ngột của adrenergic sẽ kích thích dây X, gây giãn mạch, hạ huyết áp và mạch chậm.
Làm thế nào mà tăng adrenergic lại kích thích dây X?
Bằng hai cách
Kích thích vùng thân não ảnh hướng đến tủy (trung tâm vận mạch)
Giãn tim do tăng adrenergic. Điều này kích thích phản xạ phế vị từ đáy tim (tương tự như phản xạ của Bazold Zarish). Cơ chế này được cho là quan trọng hơn kích thích vùng thân não nên còn gọi là ngất do thần kinh- tim
Beta blocker tác dụng như nào?
Nó làm dịu trung tâm adrenergic. Nó cũng làm tắc nghẽn dòng giao cảm hướng tâm của chu trình gây ngất.
Tình trạng lo âu và hoảng sợ có mối liên quan chặt chẽ giữa ngất và phản xạ phế vị. Chúng không chỉ được coi là triệu chứng cho ngất mà còn đóng vai trò là yếu tố kích thích quan trọng. Điều này được thuốc chẹn bêta giải quyết hiệu quả.
Cuối cùng, các chất chẹn beta làm dịu các thụ thể áp lực ở tim bằng cach giảm áp lực tâm thất (giảm co bóp và căng thẳng vách) do đó trục thần kinh – tim được bình ổn.
Điều quan trọng cần nhớ là chẹn beta chỉ có tác dụng ngăn ngừa/giảm các cơn ngất do cường phế vị. Nếu dùng sau khi ngất có thể làm tình trạng bệnh nhân năng lên do mạch chậm và tụt áp chiếm ưu thế trong giai đoạn hồi phục.
* Trong giai đoạn ngất do cường phế vị, atropine là thuốc hiệu quả nhất.
Thuốc chẹn beta nào?
Propronolol không có tính chọn lọc và xâm nhập tốt qua hàng rào máu não, đây là nơi thích hợp nhất để ức chế sự vận động của adrenergic.
144. Rung nhĩ kèm nhịp nhanh QRS rộng : Đừng bị ám thị bởi hội chứng WPW.
Nhịp nhanh QRS rộng không đều là vấn đề lâm sàng thường gặp ở bất kì phòng cấp cứu tim mạch nào. Khoảnh khắc đó bạn sẽ tự hỏi nhịp nhanh đó là gì, 9/10 đồng nghiệp chúng ta sẽ nhanh chóng đưa ra câu trả lời, Rung nhĩ kèm theo WPW thậm chí trước khi bạn hoàn thành câu hỏi. Nó không thường gặp nhưng chúng ta vẫn nghĩ. Vấn đề là phương pháp giáo dục truyền thống và định hướng của não bộ về những rối loạn hiếm gặp và kì lạ
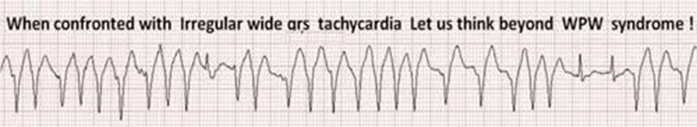
SVT kèm dẫn truyền lệch hướng thường được chẩn đoán trong bối cảnh nhịp nhanh đều.
Chúng ta thường quên rung nhĩ vs dẫn truyền lệch hướng cũng là nguyên nhân thường gặp nếu nhịp nhanh QRS rộng không đều xuất hiện.
Tôi tự hỏi liệu phenomenon đó có thể thành thuật ngữ orthodromic aberrancy không. Ngay lập tức nó là 1 chẩn đoán phân biệt với AF kèm antidromic WPW!
Cũng phải nói rằng Antidromic AF có thể nhịp rất nhanh do con đường phụ không kiểm tra tín hiệu đến, trong khi orthodromic aberrancy thì nhịp thất không thể quá 220 hoặc theo lý thuyết.
Không có dữ liệu chính xác nào được công bố về tỷ lệ AF với orthodromic aberrancy ở dân số chung
Có rất nhiều electrical environments để AF trở thành AF có QRS rộng.
1. AF with Antidromic conduction through accessory WPW pathway.
2. AF with Orthodromic aberrancy ( Non WPW – Similar to any SVT with aberrancy )
3. AF with pre existing LBBB
4. AF with Amiodarone effect. (Especially with DCM and cumulative load of Amiodarone )
5. AF with electrolytic / especially excess intra-cellualr potassium
6. Finally , even Atrial based pacing (DDD) can cause wide qrs irregular tachycardia when modeswitching fails .Here the ventricles may track the atrial irregularity and respond with a wide qrs bizarre tachycardia .
Final message
Có rất nhiều nguyên nhân gây nên nhịp nhanh QRS rộng trong rung nhĩ. Hội chứng WPW với dẫn truyền ngược chiều chỉ là 1 trong số chúng. Chúng ta cần tiếp cận các nguyên nhân với tư duy .Nên nhớ rằng, một khi đã nghĩ tới hội chứng WPW nó có thể block suy nghĩ rất mạnh :v
Chú ý : *chúng ta ko nhắc đến nhịp nhanh thất đa hình ở đây. Nó là tập con rất quan trọng trong nhịp nhanh QRS rộng không đều
** VT có thể tồn tại đồng thời với AF. Không có gì đáng ngạc nhiên cả. Nhiều bệnh lý cơ tim lan rộng cả nhĩ và thất với xơ hóa và sẹo rộng là lẫy cò hoàn hảo dẫn đến rối loạn đồng thời nhịp nhĩ và thất.
145. Tiêm nhầm adrenaline tĩnh mạch
Một vài năm trước, một cô gái trẻ đang lái xe trên đường thì 1 con ong bay qua cửa sổ mở và chích vào đầu gối. cô hoảng hốt vì tiền sử dị ứng với ong và cô lại quên epi-pen ở nhà. Cô vội đỗ xe lề đường và gọi 911. 1 anh cảnh sát đến và thấy cô rất lo lắng nhưng chưa có biểu hiện dị ứng, anh giúp đưa cô lên xe cứu thương và quay trở lại để đưa xe của cô về đồn. khi trở lại xe cứu thương để lấy thông tin thì anh giật mình khi thấy nhân viên cứu thương đang CPR cho cô trên xe và 1h sau đó cô đã tử vong tại viện
Trong trường y, chúng ta được dạy về an toàn thuốc. Cá nhân tôi không nhớ đã được giảng dạy về nó như nào, nhưng tôi nhớ nguyên tắc 5 R. Nếu bạn không biết thì bạn nên nhớ nguyên tắc này 5 R
Right patient : đúng bệnh nhân
Right drug đúng thuốc
Right dose: đúng liều
Right route đúng đường dùng
Right time. Đúng thời điểm
Tôi có thể nói với bạn khi tôi cho bệnh nhân dùng thuốc, tôi sẽ nhìn nhãn, đường dùng, bẻ thuốc và tự tiêm.
Dưới đây là những sai lầm về thuốc mà tôi đã thực hiện qua nhiều năm Tôi đã từng cho nhầm Dramamine (Dimenhydrinate) sang Benadryl
(diphenhydramine). (Hai lọ đều có cùng kích cỡ và màu sắc, và cả hai đều có tên dài bắt đầu bằng D và nằm cạnh nhau trong bộ kit).
Tôi cũng từng nhầm hơn 1 lần epinephrine với atropine và ngược lại. 1 sai lầm vô cùng nguy hiểm khi phải dùng cả 2 loại thuốc với số lượng nhiều trong các vụ ngừng tim
Tôi đã cho ASA cho 1 người dị ứng với Salisylates. Sau khi tiêm cho bệnh nhân, tự nhiên tôi nhớ có liếc qua bệnh án thấy Salisylates trong dòng dị ứng. Đồng thời tôi nhận ra, bệnh nhân bắt đầu ngứa. Opps. Tôi phải cho dùng ngay Benadryl.
Tôi cũng đã có lần dùng phải thuốc hết date cho bệnh nhân. Đây là điều thực sự đáng xấu hổ.
Trong 20 năm hành nghề, tôi mắc nhiều sai lầm nhưng may mắn không có sai lầm nào trầm trọng.
Một trong những lỗi phổ biến nhất và gây chết người là cho epi 1: 1000 IV. Đây thực sự là ―cuộc đời nở hoa hay cuộc sống bế tắc‖. Bạn có thể đổ lỗi tất cả cho thuốc nhưng có 1 số bác sĩ dường như không biết rằng epi 1:1000 có thể gây tử vong khi tiêm tĩnh mạch. Các bác sĩ dường như không biết rằng epi không thể dùng nếu bệnh nhân không có triệu chứng nặng, và liều thuốc được dùng 0,3 mg (SQ) chứ không phải là 1 mg. Có lẽ trong đầu bác sĩ trên xe cứu thương, anh ta nghĩ bệnh nhân dị ứng với ong mà bị ong đốt, không có epi-pen, ta cho epinephrine tĩnh mạch sẽ có tác dụng nhanh hơn tiêm bắp, tại sao lại không tiêm hết luôn 1mg?
Đây là một trường hợp khác:
1 Phụ nữ trẻ bị dị ứng nặng xuất hiện tình trạng quá mẫn, thở khò khè và ngứa. bác sĩ lấy 50mg benadryl và 0.3 mg epi vào các xilanh 1cc riêng. Trong lúc phân tâm nói chuyện với người nhà bệnh nhân, anh ta đã lấy xilanh tiêm benadryl vào tĩnh mạch sau đó tiêm luôn epi vào tĩnh mạch. Bệnh nhân hét toáng lên ―các người làm gì thế này, sau đó xuất hiện VT, may mắn cuối cùng cấp cứu bệnh nhân thoát chết
Một phòng khám địa phương gần đây có một bệnh nhân bị dị ứng với bactrim. Bác sĩ chỉ định 0,3 mg epi tiêm bắp nhưng điều dưỡng cho 0.3 mg epi 1: 1000 IV. Bệnh nhân bị ngưng tim, nhưng may mắn được cấp cứu và xuất hiện sau đó vài ngày
Để tránh sai lầm cực kỳ nguy hiểm này, nhiều bệnh viện đã bỏ epi 1:1000 ra khỏi bệnh viện và thay thế bằng epi-pens. Họ không phải là bệnh viện đầu tiên làm điều này.
146. Tăng huyết áp có thực sự là yếu tố nguy cơ cho bệnh mạch vành? Vâng, chính nó!
Không. . . không phải vậy ! Có lẽ !
Tôi không nghĩ thế!
Trả lời: Bất kỳ câu nào ở trên đều có thể đúng tùy theo mức độ hiểu biết và nhận thức của chúng ta.
THA là một trong những yếu tố nguy cơ đối với CAD, nhưng chắc chắn không phải là một vấn đề lớn, vì nó hiếm khi gây ra STEMI
Trừ khi THA kèm theo có rối loạn lipid máu, hút thuốc hoặc tiểu đường, hiếm khi gây ra ACS.
Tác dụng ngoại ý duy nhất của THA là, nó có thể làm nặng thêm chứng xơ vữa động mạch bằng cách thúc đẩy tổn thương biểu mô và rối loạn chức năng.
Tăng huyết áp là một yếu tố nguy cơ chính, nổi tiếng với bệnh mạch não trong khi lại là yếu tố nguy cơ bé xíu với CAD!
Chúng ta không biết tại sao các mạch máu não không chịu được huyết áp cao trong khi mạch vành lại rất thích nó!
THA không phải là yếu tố nguy cơ chính cho CAD!
Một bằng chứng cho quan sát trên là chúng ta đã phải vật lộn trong hơn một nửa thế kỷ để chứng minh 1 điều khó khăn rằng kiểm soát huyết áp đến mức tối ưu sẽ làm giảm đáng kể các biến cố mạch vành!
Hơn nữa, mối quan hệ của THA với hội chứng mạch vành cấp tính đặc biệt là STEMI rất mơ hồ, hiếm khi những bệnh nhân tăng huyết áp hoặc tăng huyết áp ác tính có STEMI *
Lưu ý ** THA vẫn là yếu tố nguy cơ lớn trong suy ** THA có thể làm tăng cơn đau thắt ngực không ổn định, nhưng rất hiếm khi làm mất ổn định mảng steroid dù THA về mặt lý thuyết có thể là nứt mảng bám
147. LVH điện thế thấp
LVH cổ điển có QRS điện thế cao hoặc trong chuyển đạo chi hoặc trước tim hoặc cả 2
Điện thế cao là một dấu hiệu ECG cụ thể, sự có mặt của nó sẽ gợi ý LVH, nhưng vắng mặt nó không giúp loại trừ LVH thật sự.
LVH với sóng ST dẹt hoặc down sloping, có hoặc không có đảo ngược sóng T, có thể là dấu hiệu duy nhất của LVH. Đây không phải là dấu hiệu của thiếu máu.
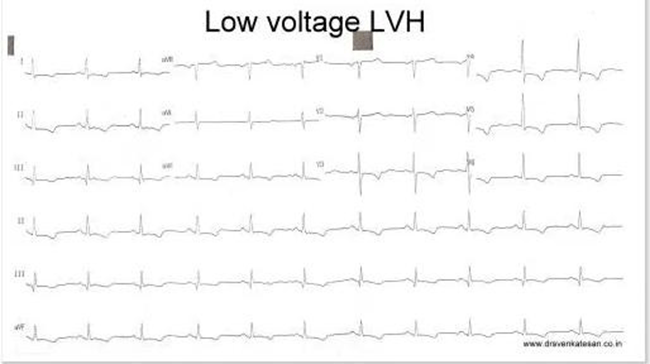
Cơ chế LVH không có điện thế cao
Đặc điểm điện sinh lý cơ bản – Sắp xếp định hướng các sợi cơ sẽ xác định điện áp. (Song song vs vuông góc, rối loạn vv)
LVH bệnh lý có quá trình xơ hóa và phì đại khoảng kẽ có thể không ghi được điện thế cao.
Sự xuất hiện của điện thế cao do LVH cho thấy phì đại khối cơ trội leenm không có phì đại khoảng kẽ hay xơ hóa
Cuối cùng, nguyên nhân kỹ thuật như thành ngực dày ở người béo phì có thể làm giảm điện thế LVH.
148. Tái cực sớm lành tính – ber
Nhiều điện tâm đồ (ECG) có hình ảnh bệnh lý, nhưng trong thực tế nó lại là biến thể của ECG bình thường, không có nghĩa bệnh nhân có bệnh
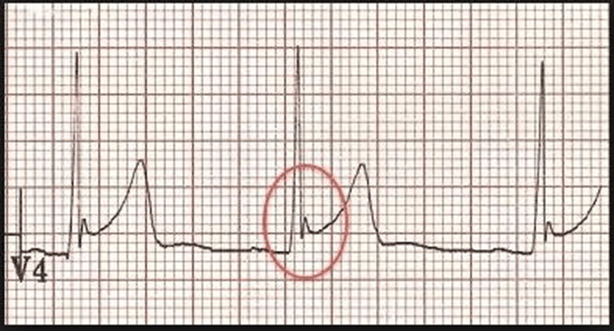
Tái cực SỚM lành tính (BENIGN EARLY REPOLARIZATION)
Đặc điểm lâm sàng
tái cực sớm lành tính (BER), còn được gọi là tái cực sớm hoặc điểm J chênh gặp trong khoảng 1-2% dân số nói chung và 13% số bệnh nhân vào cấp cứu vì đau ngực. Ở những bệnh nhân n sử dụng cocaine và hiện tại có đau ngực, BER gặp 23% đến 48% .
ECG
ST chênh lên bắt đầu ở điểm J (đường giao nhau của QRS và đoạn ST), hình dạng lõm, đặc biệt là ở phần đầu đoạn ST. Những đoạn ST chênh lên lan tỏa, thường thấy ở chuyển đạo trước tim, từ V2 đếnV6, lớn nhất ở V4.
ST chênh lên trong khoảng 0,5-5 mm, nhưng thường dưới 2 mm trong chuyển đạo trước tim và dưới 0,5 mm trong các chuyển đạo chi.
Các sóng T thường hợp với QRS và có biên độ tương đối cao và rất nhọn hay “đạt đỉnh” đối xứng. Chiều cao sóng T dao động từ 5 mm ở chuyển đạo chi đến 6,5 mm trong chuyển đạo trước tim.
sóng R cao ở chuyển đạo trái trước tim, có thể có xu hướng dịch chuyển sang phải ở vùng chuyển tiếp ở chuyển đạo trước tim .
Phải xem nhiều chuyển đạo để đo khoảng QT. Đầu tiên, xem nhiều chuyển đạo để xác định chính xác vị trí kết thúc sóng T. Thứ hai, nếu tỷ lệ này cao, có thể sóng T
chồng chéo sóng P đi sau, khó xác định thời điểm kết thúc sỏng T. Thứ ba, nếu có sóng T cũng gây khó khăn để xác định vị trí kết thúc của sóng T
sóng U
Định nghĩa. sóng U là sóng dương xuất hiện sau sóng T. Nó thường thấy khi nhịp tim chậm ở V2 và V4. Mặc dù có hay không có nó không nói lên có bệnh lý hay không, khi có bệnh sẽ làm sóng U rõ hơn.
Hình dạng. sóng U thường tròn nhẵn.
Trục. Thông thường trục sóng U về phía trước, trái, dưới làm nó thẳng đứng trong cac chuyển đạo trừ aVR, và thỉnh thoảng ở III aVF.
Biên độ. Biên độ sóng U nhỏ, thường là 5% đến 25% của sóng T đi trước
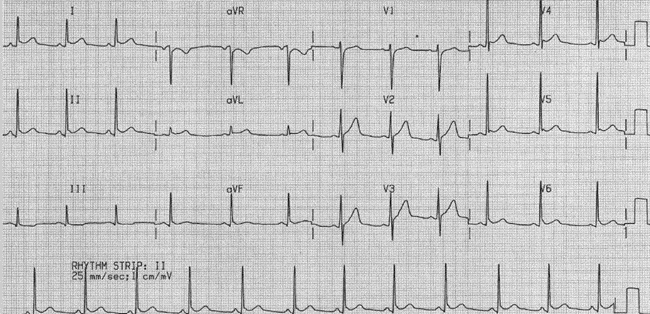
Giờ chúng ta hãy theo dõi case dưới đây. 1 trường hợp rất khó phân biệt với tắc LAD
bn nam 35 tuổi vào cấp cứu vì tỉnh dậy do đau ngực liên tục. tiền sử rối loạn lipid và tiền sử bệnh mạch vành gia đình. dấu hiệu sinh tồn bình thường, cân nặng trung bình. ECG có ST chênh lên ở I, aVL và V1–V4. troponin âm tính
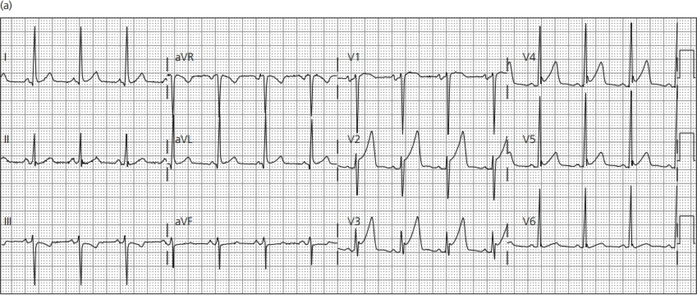
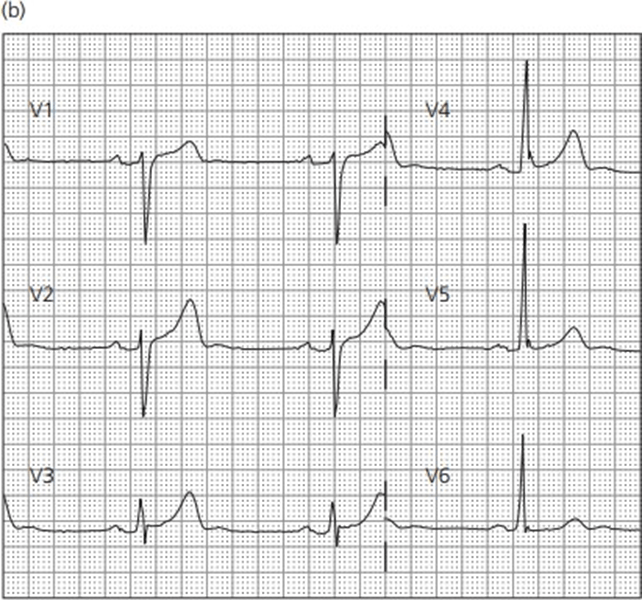
Bất thường có thể thứ phát từ QTS bất thường mà không phải do Thiếu máu cục bộ
(hình a) ECG có đặc điểm của BER: đoạn cuối QRS bìnhthường(S bình thường ở V2 and V3), đoạn ST chênh lõm. Không có STD đối xứng. dù T cao hơn R ở V2, biên độ trung bình của
R từ V2-V4 lớn (= 12 mm). R trung bình > 10 mm ít gặp trong tắc LAD. Tuy nhiên, STE ở V2-V4 >2mm ủng hộ nmct thành trước. hơnnữa phươngtrìnhhồi quy: (1.553 x mean STEJ) + (0.0546 x QTc-B) – (0.3813 x mean RA), với QTc-B 420 ms, được giá trị 22.55 (> 21), gợi ý tắc LAD. Hơn nữa, STE chuyển đạo trước, thậm chí nhịp ở chuyển đạo trước cũng chậm hơn (hình b, V1–V6).
Thông thường, STE của BER giảm khi nhịp tăng lên. Bệnh nhân này chụp vành bình thường và troponin âm tính
Biến thể bình thường hoặc BER
STE đến 3.5 mm trong một hoặc nhiều chuyển đạo trước tim có thể là một biến thể bình thường, đặc biệt là ở nam giới trẻ tuổi, gọi là tái cực sớm lành tính (BER) [6]. BER là một biến thể bình thường bắt chước STEMI. tái cực sớm lành tính hay gặp ở nam giới khỏe mạnh tuổi dưới 40, chủng tộc da đen và những người chơi thể thao [7]. Trong thực tế, STE chuyển đạo trước tim hay gặp và BER được coi đơn giản là bình thường hơn là một biến thể bình thường [6]. Chỉ 2% trường hợp có STE 5mm
sóng T trong BER nổi bật, như trong STEMI, và sóng R rõ hơn so với STEMI. Trong một nghiên cứu lớn so sánh 167 trường hợp BER và 250 tắc LAD (thành trước STEMI), nhưng phân tích chỉ 125 STEMI khó phân biệt với BER, BER có biên độ sóng T trung bình, ở V2-V4, 6,2 mm (so với 6,8 mm) và R trung bình 11,3 mm (so với 4,6 mm) [8,9]. STE trung bình tại điểm J, và ở 60 ms sau điểm J, là 1,3 mm và 1,9 mm, thấp hơn đang kể so với đàn ông có tắc LAD (2,0 mm và 2,9 mm).
QTC-B trung bình là 390 ± 27 ms so với 420 ± 28 ms [8].
o những bệnh nhân có biểu hiện các triệu chứng điển hình của ACS thường xuyên là thách thức cho các bác sĩ để phân biệt BER với AMI [10]. Một số bệnh nhân có thể bị xử trí PCI hoặc tiêu sợi huyết ngay cả khi không bị MI [5].
Các đặc điểm ECG của BER, trái ngược với STEMI
1. STE chênh lõm ở các chuyển đạo chi và V2–V6:
Giống sợi dây mắc từ đỉnh R sang đỉnh T võng xuống [11]. ST chênh lõm không loại trừ nmct thành trước do tắc LAD, thực tế hay gặp trong tắc LAD giai đoạn sớm, không có chênh lõm không loại trừ tuyệt đối BER
2. Chênh lõm từ điểm J: thường là sóng J đặc trưng ; tuy nhiên sóng J này cũng gặp trong STEMI
3. Sóng T lớn, bất đối xứng: sóng lên từ từ hơn lúc xuống
4. ổn định tạm thời: có thể có ở các ECG cũ; cũng có ngoại lệ . vị trí đặt điện cực cũng ảnh hưởng STE. Isoproterenol và thể thao cũng giảm STE
5. không có ST chênh xuống đối xứng: đặc biệt không có STD ở aVL với BER chuyển đạo dưới.
6. kết hợp T âm lành tính‖: T 2 phase đặc biệt ở V3–V5. T âm trong nmct thành trước thường gặp ở V2–V4
7. QT ngắn so với AMI: chỉ 4% tắc LAD tinh tế, 40% BER có QTc-B <380 ms (Smith SW, et al., unpublished data).
8. Xuất hiện sóng S, J ở V2, V3:
Nên không có dạng QRS kết thúc méo ―terminal QRS distortion‖ (gặp trong tắc LAD do mất sóng s).
9. Biên độ Sóng R cao: biên độ R trung bình V2 – V4 > 5 mm gặp ở 34% tắc LAD tính tế (nhạy 66%) và ở 94% BER (nhạy 94%), và ≥ 10 mm ở 10% tắc LAD với 59% BER (Smith SW, et al., unpublished data).
10. Hiếm khi xuất hiện ở chuyển đạo dưới khi không có ở chuyển đạo trước: STE chuyển đạo dưới thường < 1 mm. STE chỉ ở chuyển đạo dưới không nên giả định là do BER. Tuy nhiên, STE chuyển đạo dưới mà không có STD aVL không phải do STEMI.
Tóm lại: với STE ở V2–V4, nếu có bất kỳ yếu tố nào dưới đây, ít khi là BER mà có thể là STEMI (Smith SW et al., unpublished data):
1. STE chỉ 1 chuyển đạo > 5 mm
2. STD chuyển đạo trước hoặc dưới
3. QRS méo (mất sóng S ở V2 or V3, không có sóng J
4. ST Chỉ ở 1 chuyển đạo V2–V6 thẳng hoặc lồi (không lõm) 5.STE (V2–V4) trung bình ≥ 2 mm.
6. R trung bình (V2–V4) ≤ 5 mm
Hơn nữa nhiều tiêu chuẩn trên ECG làm ta khó phân biệt BER với tắc LAD (không chuyển đạo nào STE 5 mm, không có STD, không QRS méo, chênh lõm các chuyển đạo). nếu giá trị (1.553 mean STEJ) (0.0546 QT-cB) (0.3813 mean RA) 21, thường là BER; nếu 21 thường tắc LAD, độ nhạy, đặc hiệu và chính xác là 91%, 87%, 88%
149. Hội chứng tái cực sớm ERS độc quyền ở nam giới?
Trong phân tích sơ bộ của 50 ECG liên tiếp có dạng ERS, chỉ có 3 là nữ. Tỷ lệ thấp đáng ngạc nhiên là 6%?
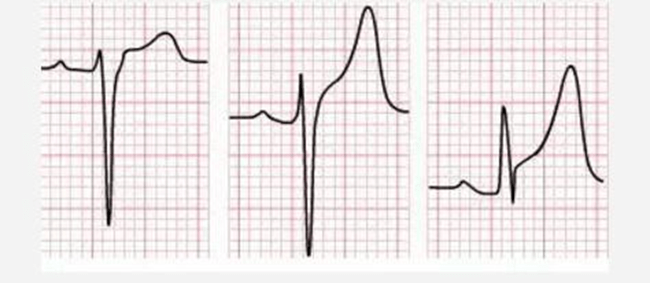
Bạn thường gặp ERS ở phụ nữ trẻ?
Phát hiện này có thể không gây bất ngờ, nếu chúng ta liên kết một thực tế khác là độ dài QT ở phụ nữ. tái cực bắt đầu khi kênh Na nhanh chóng dừng còn kênh kali bắt đầu giải phóng cation này ra ngoài từ trong tế bào. Điều này xảy ra trong phase 0 và 1. Điểm này tương ứng với sự khởi đầu của quá trình tái cực
Sự khởi phát của quá trình tái cực không hoàn toàn liên quan tới sự giải phóng K (thay vì K xác định phần lớn thời gian tái cực). Khoảng QT kéo dài ở nữ vì tái cực chậm ở nữ còn nam giới tái cực sớm, ngắn và nhanh.
Những bí ẩn xung quanh các kênh ion, đặc biệt là K + với sự đa dạng di truyền và giới tính vẫn chưa được làm sáng tỏ. Ảnh hưởng của hoóc môn giới tính ngay từ những ngày đầu của bào thai có thể là một trong những lĩnh vực nghiên cứu.
Các rối loạn ECG liên quan đến giới tính khác bao gồm:
Ở phụ nữ sóng T hiếm khi vượt quá 5 mm. Ở nam thanh niên thường có sóng T cao Sóng T đẳng điện hoặc âm ở V1-V4 thường hay gặp ở phụ nữ
Thông điệp cuối cùng
Đó là một thực tế được công nhận, tái cực nhanh ở nam giới và chậm ở nữ giới. điều này làm tăng nguy cơ xuất hiện rung thất do thiếu máu cục bộ. Rối loạn nhịp tim do EAD gây ra hay gặp ở những người có ERS.
Thống kê một lần nữa tiết lộ nam giới có nhiều khả năng có VF nguyên phát trong STEMI. (Nam giới là một yếu tố nguy cơ CAD!). Gần đây các tài liệu cho thấy ERS thực sự là một yếu tố nguy cơ cho VF nguyên phát ở thời điểm thiếu máu cục bộ

150. Sóng T dẹt
Thường thì các bác sĩ đa khoa hay nghĩ sóng ST/T dẹt là bất thường
Một phát hiện tương đối hiếm gặp là đoạn ST dẹt, được thảo luận ở đây.
Bất thường hay gặp nhất (lành tính) là sự đảo ngược sóng T và sóng ST/T cao trong tái cực sớm ở nam giới. đoạn ST dẹt là phát hiện thường gặp trong dân số nói chung.
Đoạn ST được ghi trong khoảng thời gian quan trọng nhất của chu kỳ tim. Đây là khoảng thời gian tâm thất đang hoạt động chính, tức là đẩy máu đi trong thời kỳ tâm thu. Do đó nó phải chịu áp lực cao nhất. Trong thời gian thiếu máu đoạn ST được nâng lên hoặc chênh xuống tùy vào mức độ nghiêm trọng của thiếu máu. Vì cùng một lý do, thậm chí những thay đổi tinh tế của đoạn ST này cũng làm các nhà tim mạch cau mày. Hầu hết trong số họ sẽ làm test gắng sức EST.
Thật trớ trêu, vài người bình thường có hoạt động điện gần như im lặng trong giai đoạn quan trọng này của ECG .ST thường là một đường thẳng. Đây là một ECG của một phụ nữ nghi CAD. Cô ấy không có triệu chứng. Siêu âm tim bình thường. Cô đã được yêu cầu làm EST.
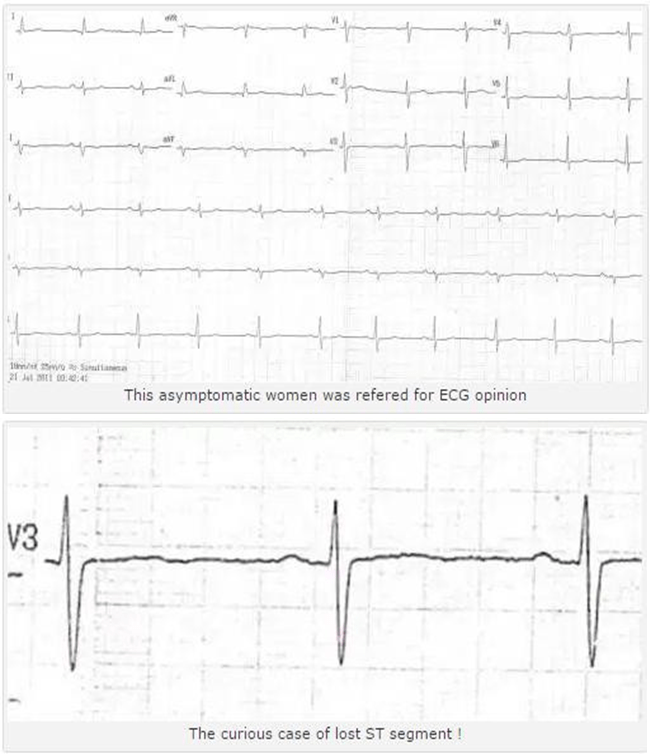
Điều đặc biệt về sóng T là, sóng T âm 10mm hay 5mm đều có thể là bình thường. vì vậy không bất ngờ khi sóng T âm hoặc sóng T dẹt là bình thường
Các trường hợp không thấy đoạn ST!
* sóng T sóng được ghi lại khi K + nhanh chóng đi ra khỏi tế bào. Hạ kali máu có thể là một nguyên nhân quan trọng gây ra T dẹt
Nó vẫn là một bí ẩn sao có sóng T cao khi K đi ra khỏi tế bào trong khi ở nữ lại làm T dẹt
151. Các thuốc phối hợp thường quy trên bệnh nhân có nmct cấp ( aha stemi guideline 2013)
1) CÁC THUỐC CHẸN BETA 1 CLASS I
1) Thuốc chẹn beta đường uống nên được dùng trong 24 giờ đầu ở những bệnh nhân STEMI không có bất kỳ các dấu hiệu dưới đây:
+Các dấu hiệu của suy tim: các bằng chứng của suy tim cung lượng thấp , tăng nguy cơ shock tim
+Hoặc các chống chỉ định khác khi dùng thuốc chẹn beta đường uống như PRI>0,24s, Block av 2,3, Hen đang hoạt động, hoặc các bệnh ở đường hô hấp đang hoạt động) (level of evidence:B)
2) Các thuốc chẹn beta nên được dùng tiếp tục trong suốt và sau khi nhập viện ở tất cả các bệnh nhân STEMI không có chống chỉ dịnh dùng thuốc chẹn beta (level of evidence:B)
3) Những bệnh nhân có chống chỉ định khi dùng chẹn beta 1 trong 24 giờ đầu sau STEMI nên được đánh giá lại để xác định việc sử dụng thích hợp sau này với thuốc chẹn beta
CLASS IIa
1) Nên dùng thuốc chẹn beta đường tĩnh mạch trong khi điều trị bệnh nhân STEMI không có chống chỉ định để điều trị tăng huyết áp hoặc thiếu máu cơ tim cục bộ (level of evidence:B)
Tác dụng và tính an toàn trong việc dùng thường quy, sớm thuốc chẹn beta truyền tĩnh mạch đã được kiểm tra ở thử nghiệm COMMIT/CCS-2.Metoprolol đường tĩnh mạch dùng sớm theo sau bởi liều cao đường uống metoprolol có một ảnh hưởng không rõ ràng đến việc kết nối các biến chứng của bệnh nhân bao gồm tử vong, tái nhồi máu cơ tim hoặc ngừng tim.Kết quả cho thấy Tỷ lệ thấp hơn bệnh nhân NMCT tái phát và rung thất ở nhóm bệnh nhân được điều trị, các bệnh nhân xuất viện có tỷ lệ cao hơn do shock tim khi điều trị với metoprolol , đặc biệt ở ngày 0 và 1. Việc tiến triển shock tim gia tăng ở nhóm phụ , bao gồm các bệnh nhân >70 tuổi, Huyết áp tâm thu <120mmHg, Tần số tim>110mmHg, hoặc tăng thời gian từ lúc khởi phát triệu chứng STEMI tới lúc điều trị.Lợi ích của thuốc chẹn beta trong việc ngăn ngừa thứ phát NMCT đã được đưa ra ở nhiều thử nghiệm liên quan đến thời kỳ trước tái tưới máu và được cho là tốt nhất ở các bệnh nhân NMCT biến chứng suy tim, giảm chức năng thất trái, hoặc loạn nhịp thất. Thời gian điều trị dài hạn thường quy của thuốc chẹn Beta 1 sau NMCT không biến chứng không kèm suy tim hoặc tăng huyết áp chưa được đề cập tới.
Các guideline phòng ngừa thứ phát của AHA/ACCF khuyến cáo thời gian điều trị 3 năm cho những bệnh nhân ở nhóm nhỏ này
2) CÁC THUỐC ỨC CHẾ MEN CHUYỂN (ACE) THUỐC CHẸN THỤ THỂ ANGIOTENSIN(ARB)
CLASS I
1) Thuốc ức chế men chuyển ACE nên được chỉ định trong 24 giờ đầu cho tất cả các bệnh nhân STEMI thành trước, suy tim, hoặc EF nhỏ hơn hoặc bằng 40%. trừ khi không có chống chỉ định (level of evidence:A)
2) Thuốc chẹn thụ thể angiotensin (ARB) nên được dùng ở những bệnh nhân STEMI không đáp ứng với ACR (level of evidence:B)
3) Thuốc kháng aldosterone nên được dùng ở những bệnh nhân STEMI không có chống chỉ định và đã được dùng ACE và chẹn beta , có EF nhỏ hơn hoặc bằng 40% và có triệu chứng suy tim toàn bộ hoặc đái tháo đường(level of evidence:B)
CLASS IIa
1) ACE được dùng cho tất cả các bệnh nhân STEMI và không có chống chỉ đinh ACE (level of evidence:B)
ACE đường uống giảm các biến chứng tim mạch trầm trọng và nhẹ ở tất cả các bệnh nhân STEMI. Các tác dụng bảo vệ của chúng đã được chứng minh không phụ thuộc vào các thuốc khác (như tiêu sợi huyết , aspirin, và chẹn beta) .Lợi ích lâm sàng của ACE hiệu quả nhất ở nhóm bệnh nhân nguy cơ cao(NMCT thành trước, EF<40%, suy tim, NMCT trước đây, và nhịp tim nhanh).Sự chứng minh lợi ích sớm (trước 24 giờ) hỗ trợ cho việc thúc đẩy dùng những thuốc này ở những bệnh nhân không có chống chỉ định trước đó (hạ huyết áp , shock, hẹp mạch thận 2 bên hoặc tiền sử có suy thận hoặc giảm chức năng thận với ACE/ARB, hoặc dị ứng thuốc). Vai trò của việc dùng ACE dài hạn thường quy ở những bệnh nhân nguy cơ thấp sau STEMI đã được tái tưới máu và điều trị với các thuốc giảm mỡ máu ít hơn.ARB được chỉ định cho những bệnh nhân không đáp ứng với ACE.Đặc biệt,valsartan đã được nghiên cứu cho thấy không thua kém captopril trong thử nghiệm VALIANT
Nghiên cứu EPHESUS cho thấy lợi ích của thuốc kháng aldosterone ,eplerenone tăng thêm tính tối ưu trong điều trị ở những bệnh nhân có lâm sàng phù hợp ( createnin<=2,3mg/dL ở nam giới và <=2mg/dL ở phụ nữ, Kali <=5mEq/L) từ 3- 14 ngày sau STEMI với EF <=40% và có triệu chứng suy tim toàn bộ hoặc đái tháo đường. Một phân tích sau thử nghiệm EPHESUS đồng thuận với tác dụng của việc điều trị phụ thuộc thời gian của eplerenone.Bắt đầu sớm thuốc (<7 ngày) giúp giảm tỷ lệ tử vong do bất kỳ nguyên nhân nào, đột tử, và tử vong do tim mạch/nhập viện do tim mạch, trong khi bắt đầu thuốc >=7 ngày không có tác dụng gì khi xuất viện.
3) THUỐC GIẢM MỠ MÁU CLASS I
1) Các thuốc statin mạnh nên được dùng hoặc tiếp tục dùng ở các bệnh nhân STEMI không có chống chỉ định (level of evidence:B)
CLASS IIa
1) Nên xét nghiệm mỡ máu ở tất cả các bệnh nhân STEMI,trong 24 giờ từ lúc nhập viện(level of evidence:C)
Điều trị với statins ở các bệnh nhân đã được điều trị ổn định sau HC vành cấp bao gồm STEMI, làm giảm nguy cơ tử vong do bệnh tim mạch vành, tái NMCT, đột quỵ, và cần tái thông mạch . Nhiều thuốc statin mạnh( so với các thuốc statin yếu hơn) giúp giảm các biến chứng không trầm trọng sau khi điều trị.Trong số các statins hiện hành, chỉ có atorvastatin liều cao (80 mg mỗi ngày) được chỉ ra làm giảm tỷ lệ tử vong và các biến chứng thiếu máu cơ tim trong các bệnh nhân HC vành cấp. Gần 1/3 bệnh nhân trong thử nghiệm PROVE-IT TIMI 22 được chẩn đoán STEMI. Tỷ lệ biến chứng tim mạch không giảm với liệu trình simvastain (40mg mỗi ngày trong 1 tháng sau đó 80mg mỗi ngày) trong thử nghiệm A-Z , và các bằng chứng gần đây cho thấy sự an toàn của simvastatin liều cao (80mg hàng ngày).Mặc dù lợi ích của statins mạnh giảm ở những bệnh nhân Statin-naive có HC vành cấp vì vai trò giảm lượng Lipoprotein tỉ trọng thấp, các tác giả khuyến cáo việc sử dụng statins ở tất cả các bệnh nhân STEMI. Sử dụng statin sau HC vành cấp có lợi dù các bệnh nhân có LDL <70mg/dL.Các thử nghiệm khi điều trị statin ở các bệnh nhân HC vành cấp và bệnh tim, thiếu máu cơ tim ổn định đã được đưa ra để so sánh tính mạnh yếu của các statins trong điều trị và tâm lý.Chúng không được đưa ra để so sánh hiệu quả xuất viện trong lâm sàng với chức năng đặc hiệu giảm LDL đã đạt được khi được điều trị.Cải thiện sự chấp thuận điều trị của bệnh nhân là một nhân tố căn bản trong việc điều chỉnh thời gian điều trị thuốc giảm mỡ máu trước khi xuất viện sau STEMI.Điều trị dài hạn mỡ máu sau STEMI bao gồm đưa ra mục tiêu Triglycerides và lipoprotein tỷ trọng không cao được đề cập trong AHA/ACC secondary prevention and risk reduction therapy ..2011 update
4) NITRAT
Mặc dù NTG có thể caỉ thiện triệu chứng và dấu hiệu của thiếu máu cơ tim bằng cách giảm tiền gánh thất trái và tăng tưới máu mạch vành, nhưng nó tổng quan không làm giảm tổn thương cơ tim liên quan đến tắc mạch vành vùng thượng tâm mạc trừ khi co mạch đóng vai trò chính trong sinh lý bệnh. NTG tĩnh mạch có thể có ích trong điều trị các bệnh nhân STEMI và tăng huyết áp hoặc suy t im. Nitrat không nên được chỉ định ở các bệnh nhân tụt huyết áp , nhất là nhịp tim chậm hoặc nhịp tim nhanh , Nhồi máu thất phải, hoặc việc dùng thuốc chẹn 5’phosphodiesterase trong 24-48 giờ trước đó. Nitrat không có vai trò gì khi sử dụng thường quy đường uống trong thời kỳ hồi phục ở những bệnh nhân STEMI
5) THUỐC CHẸN KÊNH CALCI
Một cuộc hồi cứu trên 19000 bệnh nhân chứng minh rằng sử dụng thuốc chẹn kênh calci trong tình trạng cấp hoặc giai đoạn hồi phục STEMI không có lợi trong việc hạn chế vùng nhồi máu hoặc giảm tỷ lệ tái nhồi máu. Thuốc chẹn kênh Calci có thể có ích, tuy nhiên, để giảm nhẹ thiếu máu cơ tim,hạ huyết ap, hoặc kiểm soát tần số thất trong rung nhĩ ở những bệnh nhân không đáp ứng với thuốc chẹn Beta. Chú ý thận trọng dùng ở những bệnh nhân có chức năng tâm thu thất trái giảm. Sử dụng ngay lập tức nifedipine bị chống chỉ định ở những bệnh nhân STEMI vì gây tụt huyết áp và gây kích ứng thần kinh giao cảm làm nhịp tim nhanh.
6) OXYGEN
Một vài tài liệu được đưa ra ủng hộ hoặc bác bỏ giá trị của việc dùng Oxygen thường quy trong pha cấp cứu STEMI , và nhiều nghiên cứu nữa đang được thực hiện . Phương pháp tổng hợp COchrane trong 3 thử nghiệm cho thấy nguy cơ cao gấp 3 lần tử vong ở các bệnh nhân được chẩn đoán NMCT cấp điều trị với oxygen
hơn là những bệnh nhân NMCT cấp trong phòng thông khí tốt.Biện pháp oxygen được đánh giá cao ở những bệnh nhân giảm oxy máu (SPO2<90%) và có thể có ảnh hưởng tâm lý tốt cho bệnh nhân. Cung cấp Oxy có thể, tuy nhiên tăng trở kháng trong mạch vành.Oxygen nên được chỉ định thận trọng với những bệnh nhân mắc bệnh phổi mãn tính (COPD) và giữ CO2
7) GIẢM ĐAU TRÊN BỆNH NHÂN STEMI:MORPHINE, NSTEROID VÀ NSTEROID CHẸN CHỌN LỌC COX2( AHA STEMI GUIDELINES)
Trên bệnh nhân không có tiền sử nhạy cảm với morphine, morphine sulf ate là thuốc được chọn để giảm đau trên bệnh nhân STEMI , đặc biệt những trường hợp biến chứng phù phổi cấp. Morphine có thể làm giảm hô hấp , giảm stress, và tác động tích cực đến việc đổ đầy thất . Liều morphine sulfate cần đạt được để kiểm soát cơn đau sẽ phụ thuộc vào nhiều yếu tố bao gồm: tuổi , thể tạng, huyết áp và tần số tim bệnh nhân . Naloxone có thể được dùng với liều từ 0,1-0,2mg truyền tĩnh mạch mỗi 15 phút khi có tác dụng lên tâm thần DO quá liều morphine , và atropine 0,5-1,5 mg truyền tĩnh mạch có thể được dùng để kháng lại tác dụng của morphine gây nhịp tim chậm.
Các nghiên cứu dịch tễ học và các phương pháp hồi cứu đã cho thấy NSTEROID và NSTEROID chọn lọc trên COX2 có thể liên quan đến việc tăng nguy cơ tử vong, tái nhồi máu , thủng tim, tăng huyết áp, suy thận , và suy tim. NSTEROID và NSTEROID chọn lọc trên COX2 bị chống chỉ định trên những bệnh nhân STEMI . CHúng không được dùng tiên phát trong pha cấp cứu và nên được ngưng dùng ở những bệnh nhân sử dụng chúng trước khi nhập viện
152. Nhồi máu cơ tim ở phụ nữ trẻ
Một cô gái trẻ 16 tuổi ngất khi chơi bóng rổ vào cấp cứu vì suy hô hấp nặng, tỉnh nhưng kích động, thở 40-50l/phút. Cô được làm ECG kết luận bình thường. Sau đó diễn biến nặng phải đặt ống NKQ
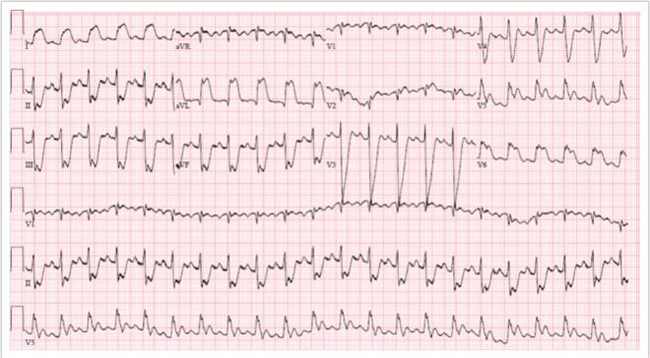
Ở đây nhịp xoang nhanh với ST chênh lên ở chuyển đạo I, aVL, V5 và V6, với ST chênh xuống ở V3 và V4, kèm theo ST chênh xuống đối xứng ở II, III. Ở đây ta có thể chẩn đoán nhồi máu thành sau bên STEMI cấp tính.
ECG đã được đọc kết quả bởi 1 bác sĩ cấp cứu không quen chẩn đoán NMCT cấp.
Sau đó bệnh nhân được chuyển đến phòng can thiệp mạch, kiểm tra có tắc nhánh bất thường của động mạch vành và kết quả thủ thuật tốt.
Bài học:
Trẻ em và thanh thiếu niên có thể có xơ vữa động mạch sớm, bệnh Kawasaki phình mạch vành và động mạch vành bất thường. Có những báo cáo nhi khoa về MI do LVH, cocaine, methamphetamine và tắc mạch do khối u, van động mạch chủ loạn sản cũng có viêm cơ tim, WPW, HOCM, dài QT, bất thường giải phẫu bẩm sinh và nhiều hơn nữa. Trong chấn thương, bệnh nhân có thể có đụng dập cơ tim.
Khi trẻ bị đau ngực, ngất, khó thở hoặc triệu chứng tim mạch khác cần ghi điện tâm đồ. Đây là phương tiện giá thành rẻ, không xâm lấn và cung cấp nhiều thông tin quan trọng.
Hơn nữa, bất cứ ai bất tỉnh khi gắng sức, ở mọi lứa tuổi cần khám và kiểm tra cẩn thận
153. Đau ngực bệnh nhân nam, 20 tuổi; ST chênh xuống: chẩn đoán tái cực sớm?
Bệnh nhân nam 20 tuổi đau ngực 2 h trước khi vào cấp cứu. cậu cảm thấy tức ngực, lan ra cánh tay phải, buồn nôn, khó thở. Không có yếu tố nguy cơ tim mạch, không sử dụng cocaine.
ECG ghi 1 giờ sau khi khởi phát cơn đau tại phòng khám tư
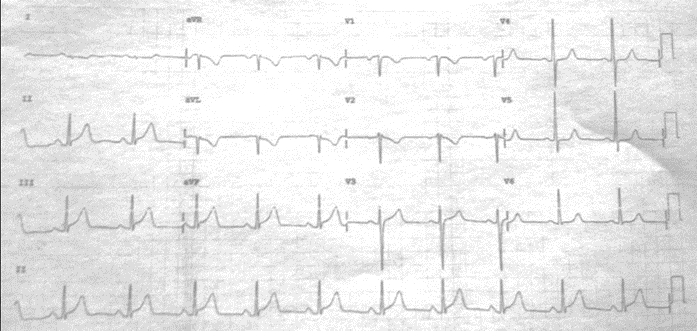
ST chênh xuống ít nhất 2mm ở aVL, ST đi ngang ở trong V4-V6 và sóng T đảo ngược ở V2.
Vậy ST chênh xuống này có thể do “tái cực sớm”?
Tại sao không? Chúng tôi thử so sánh với inferior STEMI -(66 trường hợp tái cực sớm)
1. Có ST chênh xuống ở aVL. Điều này xảy ra trong 66 trường hợp tái cực sớm và 99% bệnh nhân inferior STEMI.
2. Có quá nhiều ST chênh lên. Chỉ 1 trong 66 trường hợp tái cực sơm có 1 chuyển đạo ST chênh 2 mm
3. ST không chênh lên ở V5 và V6. Với nhóm tái cực sớm, 53 / 66 đã ST chênh lên 1 mm ở V5, và 61/66 chênh lên 0,5 mm ở V5. 64 / 66 có ST chênh 1 mm ở V6 và 58 / 66 chênh 0,5 mm ở V6.
4. Sóng T quá cao tương xứng với những người tái cực sớm
5. sóng T đảo ngược ở V2 không phù hợp với tái cực sớm, rất điển hình sau thiếu máu cục bộ.
95 phút sau, bệnh nhân đến khoa cấp cứu và đây là ECG làm lại
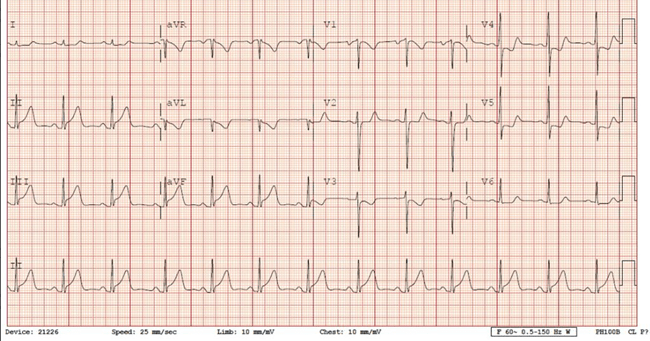
ST chênh lên 2-2,5 mm ở chuyển đạo dưới. Có ST chênh xuống ở chuyển đạo I và aVL, đảo ngược sóng T ở aVL, ST chênh xuống tương đối ở V2 (đẳng điện: ở nam thanh niên ST chênh lên ít nhất phải 1 mm), ở đây ST dẹt trong V2. Có ST chênh xuống V3- V6. Có sóng T âm ở V3, và sóng T 2 pha trong V4-V6.
Có phải là không có nghi ngờ rằng đây là STEMI. Tất cả 5 điểm trên được áp dụng, nhưng bây giờ ECG đã thay đổi và rõ ràng hơn. Ngoài ra, có ST chênh xuống ở V3-V6 có thể nghĩ đến chẩn đoán thiếu máu cục bộ.
Tuy nhiên, bệnh nhân được chẩn đoán tái cực sớm. không được tiến hành can thiệp mạch
22 phút sau, điện tâm đồ khác được làm
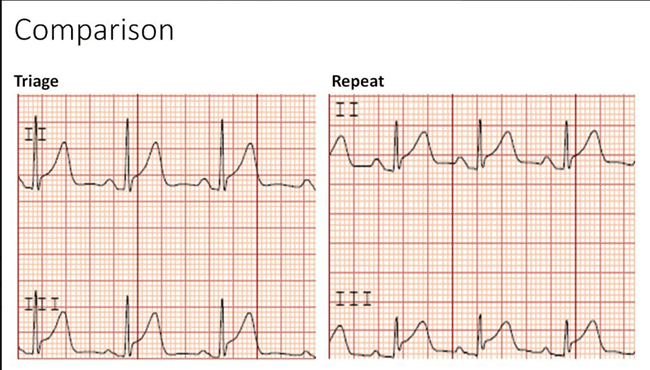
Nó có thay đổi một chút. Xem hình phóng lớn so sánh 2 chuyển đạo bên II và III ở 2 ECG đầu tiên
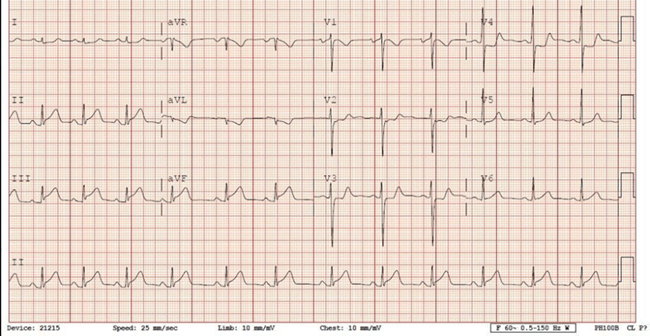
ST chênh lên hơn ở chuyển đạo sau, đặc biệt tỷ lệ thuận với sóng R. Có vẻ như có sự giảm biên độ sóng T
Troponin I : + 0,252 ng / ml.
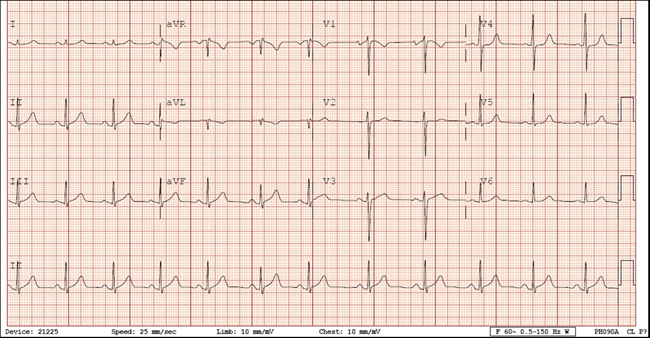
191 phút sau nhập viện
Có những dấu hiệu thiếu máu cục bộ. Không có sóng Q. Có vẻ như đã tự điều chỉnh tái tưới máu tự phát. ST chênh lên tối thiểu ở chuyển đạo dưới bây giờ phù hợp với tái cực sớm
Bắt đầu truyền Heparin nhỏ giọt.
Xét nghiệm troponin lần 2: 1,71 ng / ml -3 giờ sau đó.
6h sau nhập viện bệnh nhân được đưa đến phòng can thiệp mạch, thấy hẹp 99% ở RCA gần đoạn phân nhánh sau bên. Thấy phình động mạch vành nhưng không phân loại theo TIMI
Troponin I : 75 ng / ml. ECG 2 tuần sau đó
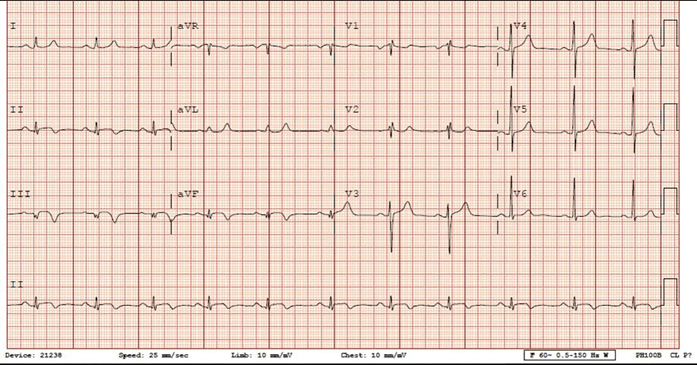
Có sóng Q sâu nhồi máu, với sóng T âm của nhồi máu cơ tim xuyên thành
Bài học:
1. Có thể gặp MI ở người trẻ
a. Một số do nguyên nhân bất thường: thường có rối loạn phình động mạch vành trái
b. Những người trẻ tuổi cũng bị xơ vữa động mạch và bong mảng bám
2. Khi đọc ECG bạn phải chẩn đoán dứt khoát. Không được để các yếu tố như tuổi trẻ hoặc triệu chứng không điển hình ảnh hưởng đến kết quả bạn đọc
3. Biết các dạng ECG tương tự như STEMI. Ở đây các bác sĩ không phân biệt được sự khác nhau giữa tái cực sơm với STEMI nên bỏ sót bệnh (xem ở trên)
4. Khi xác định STEMI cần đưa ngay bệnh nhân đến phòng can thiệp mạch ngay cả khi thấy ST không còn chênh vì nguy cơ + rủi ro rất cao
Dưới đây là hai ví dụ về tái cực sớm ở chuyển đạo dưới
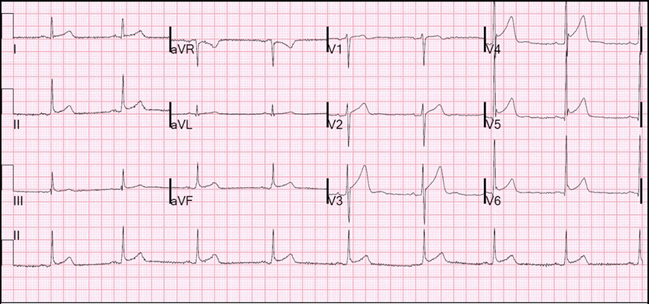
Đầu tiên:
1. ST chênh xuống mà không có ST đối xứng ở AVL. Điều này là do trục ST lệch trái, không xuống hoặc sang phải. do đó ST ở D III luôn nhỏ hơn hoặc bằng ở D II.
2. St chênh ở chuyển đạo trước và bên; ST cũng chênh ở chuyển đạo dưới là tương đối hiếm ở bệnh nhân tái cực sớm
3. trong ECG này, cũng hình thành sóng J ở V4-V6. 4. ST chênh tối đa là 1 mm ở chuyển đạo dưới
Thứ hai:
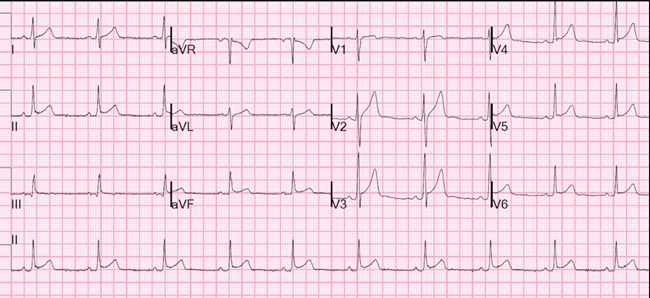
154. bệnh nhân nữ 24 tuổi: liệu STEMI? Viêm màng ngoài tim?
Bệnh nhân nữ 24 tuổi tiền sử bình thường xuất hiện đau ngực. Cơn đau ngực trái xuất hiện lúc 6:20 và lan lên cánh tay và ra sau lưng. Cô có uống rượu trước đó và trở về nhà vào lúc 1:30 hoặc 2:00. Đêm qua cô có nôn. Trươc đây chưa bao giờ cô đau ngực như này, BP là 140/100 và mạch 93. Dưới
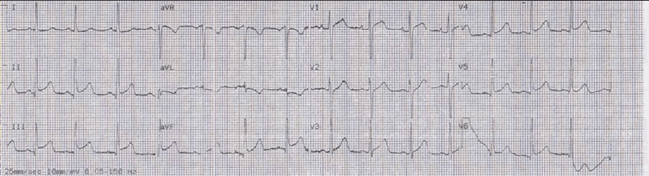 đây là ECG lúc 7h20
đây là ECG lúc 7h20Nhịp xoang. ST chênh lên ở chuyển đạo dưới và chuyển đạo bên, đối xứng với ST chênh xuống ở AVL, PR chênh xuống không có ý nghĩa
Cô được nhỏ dưới lưỡi 1 giọt NTG và thấy đỡ đau. Dưới đây là ECG lúc 7h48
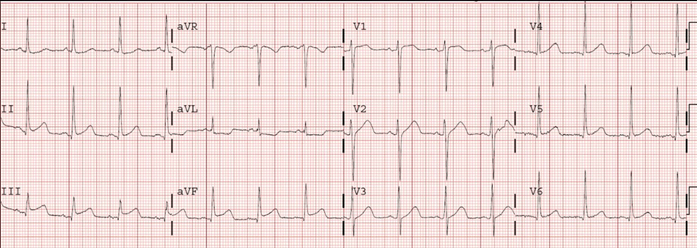
Không có nhiều thay đổi ngoại trừ ST chênh ít ở chuyển đạo bên
Chụp X-quang ngực xác định không có hội chứng Boerhaave (Boerhaave’s syndrome)
Có thể nghi ngờ viêm màng ngoài tim ở một người trẻ tuổi với ST chênh lên. Tuy nhiên, nếu bạn chẩn đoán viêm màng ngoài tim sẽ có thể làm hại bạn! Tôi tin rằng trước đây có viêm màng ngoài tim nhưng không loại trừ nhồi máu cơ tim cấp.
Hơn nữa ST chênh xuống ở chuyển đạo dưới, ST chênh xuống ở aVL gần như đã xác định nhồi máu cơ tim
Bệnh nhân được siêu âm tim tại giường ngay lập tức thấy không có tràn dịch và không có chuyển động bất thường của thành, vách tim. Bệnh nhân gần như hết đau trong thời gian này.
Trong khi chờ hội chẩn, chúng tôi ghi nhận ECG khác lúc 08h26:
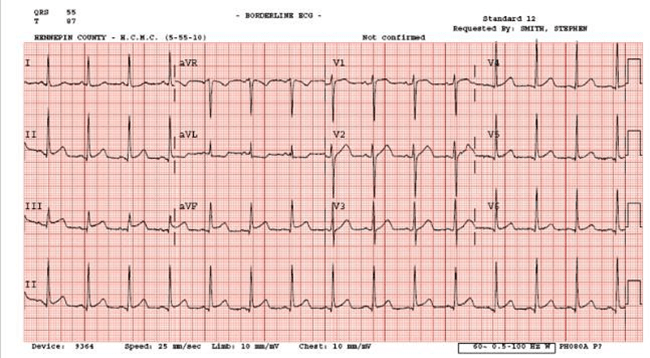
không có nhiều thay đổi. ECG lúc 08h27
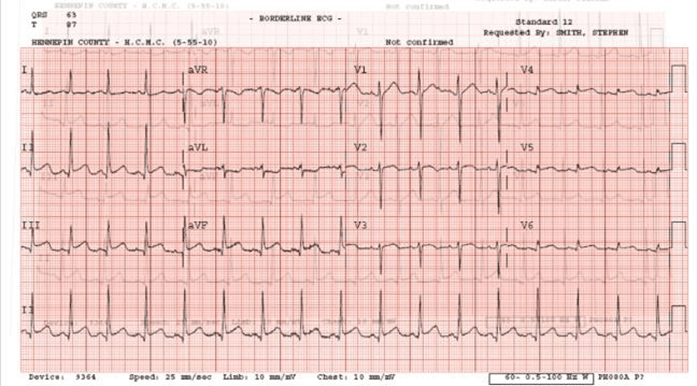
Để ý thấy ST chênh lên nghi nhồi máu thất phải
Chụp mạch phát hiện tổn thương đoạn gần LAD (TIMI3 –flows) độ 3 gây tắc LAD cấp máu thành dưới. Vì vậy, đây là nhồi máu cơ tim thành trước- dưới – bên. Bệnh nhân được đặt stent và điều trị thuốc kháng tiểu cầu và tiêu huyết khối.
Ngày hôm sau, cô ấy đã phục hồi tái tưới máu, xuất hiện sóng T ở chuyển đạo trước , cũng như chuyển đạo dưới và bên
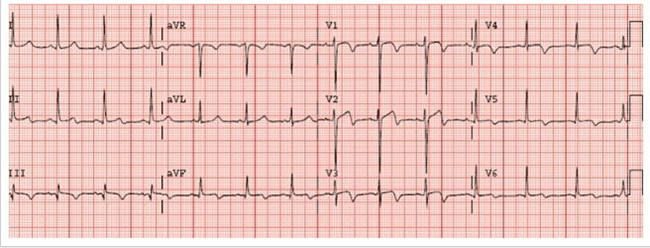
ECG nhìn tương tự hội chứng Wellens ở chuyển đạo trước.
lipid máu cô gái này: LDL 139, VLDL 10, HDL 70, cholesterol TP 219.
Bài học:
1) Đừng bao giờ nghĩ nhồi máu cơ tim không xảy ra ở người trẻ tuổi! Họ không cần phải có nhiều yếu tố nguy cơ hay đang dùng cocaine. Ở phụ nữ trẻ bị STEMI, việc chẩn đoán thường bỏ sót hoặc chậm hơn trong bất kỳ nhóm dân số khác, có lẽ vì sự thiên vị mà chúng ta luôn nghĩ trong đầu ” Không, không thể được”. nhồi máu cơ tim hiện tại phổ biến hơn nhiều ở những người trẻ, kể cả phụ nữ, so với ghi nhận trước đây. Có thể do bóc tách động mạch vành tự phát, nếu trên ECG thể hiện, hãy nghĩ đến nó, đừng tự phủ định chẩn đoán của mình bằng câu nói ” Không, không thể được”
2) Nếu bạn chẩn đoán viêm màng ngoài tim thì hãy cẩn thận
3) Không có hiện tượng vách tim chuyển động bất thường có thể làm bạn sai lầm khi phủ định nhồi máu cơ tim, đặc biệt khi bệnh nhân đã bớt đau
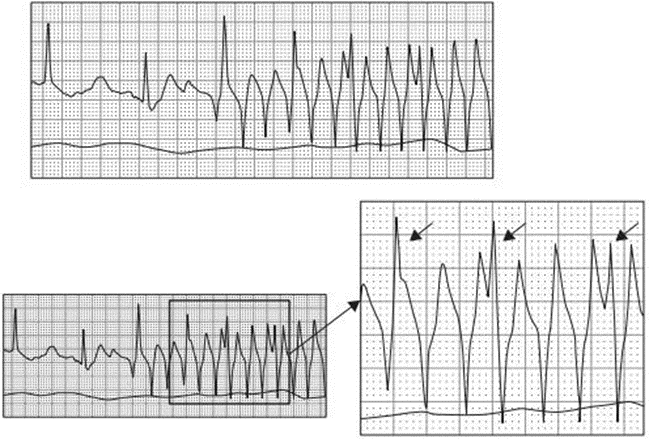
Rung nhĩ, tỷ lệ thất 96, có hỉnh ảnh giả. Nhịp ban đầu không đều không thấy rõ được hoạt động của tâm nhĩ, phù hợp với rung nhĩ. Nhịp kết thúc không đều và phức hợp QRS nhanh và thay đổi hình thái. Có thể chỗ này cân nhắc là rung nhĩ với hội chứng Wolff-Parkinson-White (WPW), xoắn đỉnh hoặc hình ảnh giả. Sự xuất hiện hình ảnh lưỡi dao ―sharp point‖ ở cả điểm cao và thấp nhất của phức hợp QRS phù hợp với hình ảnh giả. Xem hình bên dưới.
Lưu ý các mũi tên chỉ phức hợp QRS có sự thay đổi liên tục nhưng lâm sàng và tần số thất không thay đổi gợi ý đây là hình ảnh giả bệnh nhân nữ 54 tuổi mất nước do nôn nhiều vì viêm dạ dày ruột và ngất, a) ECG khi ngất b) ECG sau xử trí
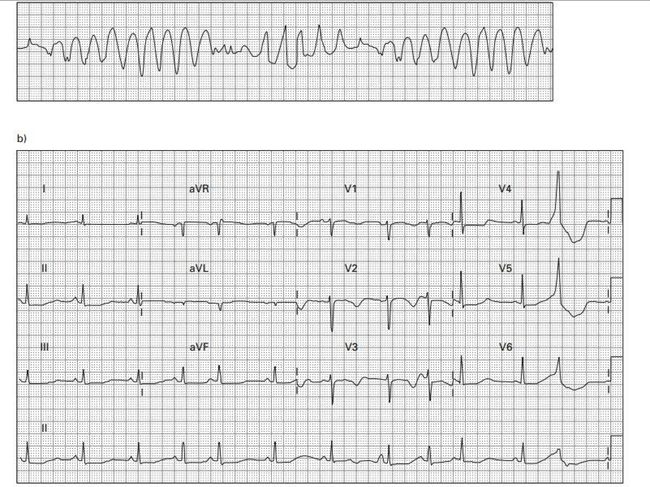
a) nhịp nhanh thất đa hình, nghi ngờ xoắn đỉnh, tần só 220. Phức hợp QRS nhanh phức tạp với liên tục thay đổi hình thái, thay đổi khoảng R-R và thay đổi trục gợi ý nhịp nhanh thất đa hình. phức hợp QRS xuất hiện xoay quanh một điểm cố định, phát triển lớn hơn, sau đó nhỏ hơn, sau đó lớn hơn và tiếp tục như vậy. Mô hình này gợi ý xoắn đỉnh. Xoắn đỉnh là một loại nhịp nhanh thất đa hình đặc trưng bởi hình ảnh này. Nó cũng được định nghĩa khi ECG có khoảng QT kéo dài.
b) nhịp xoang(SR), tần số 64, ngoại tâm th nhĩ (PAC) và ngoại tâm thu thất (PVC), thiếu máu cục bộ vách trước, kéo dài QT. Những bất thường ở đây chính là do kéo dài QT. Các khoảng QT bình thường sẽ khác nhau dựa trên tần số, vì vậy ta sẽ sử dụng công thức Bazett để tính chính xác khoảng QT:
QT (QTC) = QT / √ (RR).
RR là khoảng R-R. QTc được coi là kéo dài khi> 450 msec ở nam giới và> 460 msec ở phụ nữ và trẻ em. QTc kéo dài chỉ ra rằng bệnh nhân có nguy cơ xoắn đỉnh. Nguy cơ cao khi QTc kéo dài trên 500 msec. Trong trường hợp này, (QT = 600 ms, QTc = 620 ms). Chẩn đoán phân biệt khoảng QTkéo dài do hạ kali máu, hạ magne, hạ calci máu, thiếu máu cơ tim cấp tính, tăng áp lực nội sọ, thuốc có tác dụng trên kênh natri, hạ thân nhiệt, và hội chứng kéo dài QT bẩm sinh. Ở đây có thể QT kéo dài (cũng như các nhịp ngoại tâm thu) là do rối loạn điện giải. T âm V1-V3 nghi thiếu máu cục bộ vách trước.
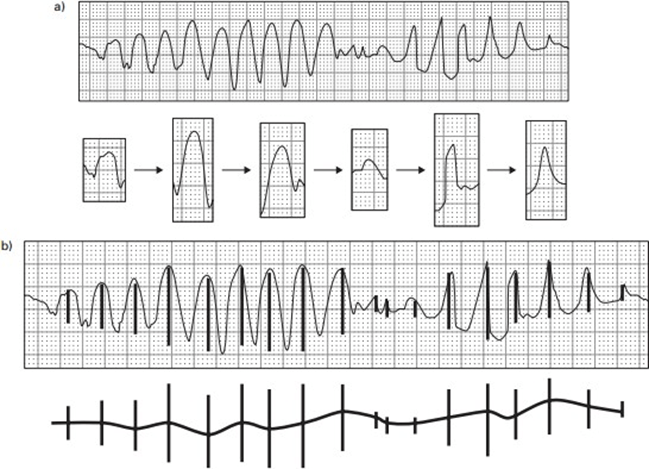
Điều quan trọng là cần lưu ý rằng việc chẩn đoán xoắn đỉnh đòi hỏi phải có tái cực bất thường
trên điện tâm đồ, cụ thể là khoảng QT kéo dài
. a) Lưu ý quan trọng là sự thay đổi beat-to-beat trong hình thái QRS
. b) Lưu ý quan trọng là sự thay đổi beat-to-beat trong biên độ QRS
80. a) bệnh nhân nữ 18 tuổi đánh trống ngực, chóng mặt và hạ huyết áp, b) trong khi điều trị
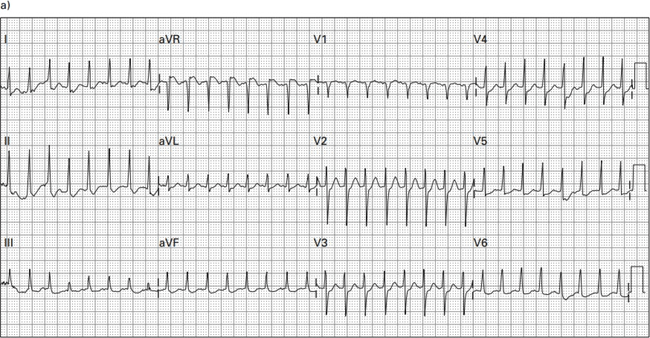
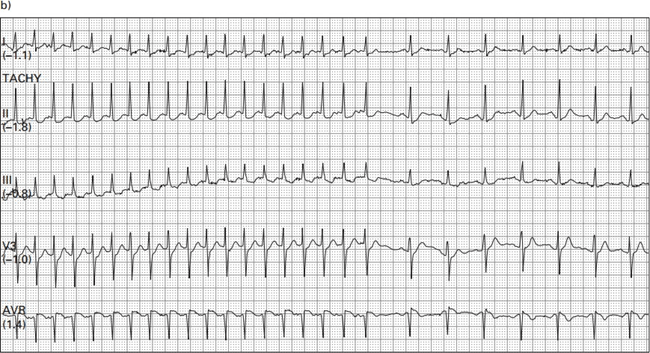
a) nhịp nhanh trên thất kịch phát, tần số 190. Chẩn đoán phân biệt nhịp nhanh có QRS hẹp
gồm nhịp nhanh xoang (ST), nhịp nhanh trên thất kịch phát (thường chỉ đơn giản gọi là nhịp nhanh trên thất, hay SVT) và cuồng nhĩ với dẫn truyền nhĩ thất 2: 1.
ST và cuồng nhĩ đặc trưng bởi hình ảnh hoạt động nhĩ rõ ràng trên ECG. SVTs, thường mất sóng P hoặc sóng P chạy sau (P xảy ra sau QRS). ECG không có sóng p hoặc sóng f nên chúng ta chẩn đoán SVT
. ST chênh xuống chuyển đạo dưới và bên thường gặp trong những trường hợp SVT và không liên quan lâm sàng miễn là ST chênh xuống mất sau khi chuyển về nhịp xoang SR
B)nhịp nhanh kịch phát trên thất, tần số 190, đã chuyển nhịp nhanh xoang, tần số 105. ECG này làm trong quá trình tiêm tĩnh mạch adenosine. Đang chuyển về nhịp xoang
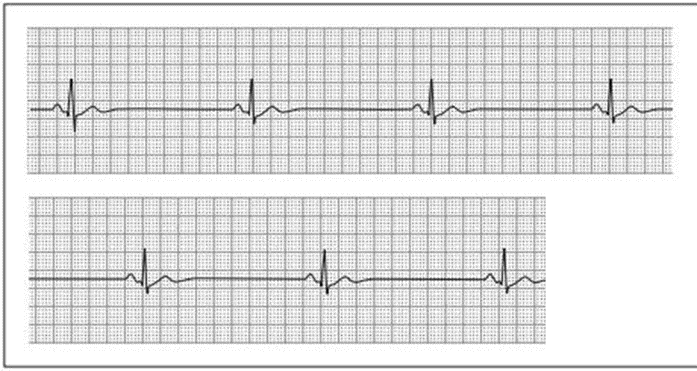
Bệnh nhân nam 68 tuổi tăng huyết áp, dùng ba loại thuốc, có biểu hiện mệt mỏi nhiều
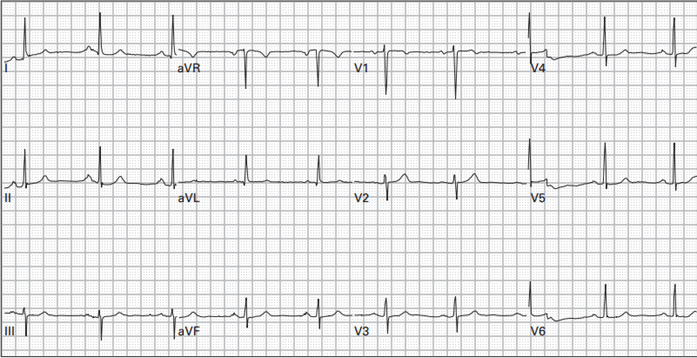
155. Phân tích case ecg
1. bệnh nhân nữ 45 tuổi đi khám sức khỏe định kì
nhịp xoang (SR), tần số 60, ECG bình thường. SR thường được xác định có tần số nhĩ 60-100 / phút và sóng P trục 15-75 độ. nhịp xoang có thể được xác định bởi sóng P thẳng đứng trong các đạo trình I, II, III, aVF; nếu sóng P âm trong bất kỳ chuyển đạo nào trong đám này gợi ý có nhịp nhĩ lạc vị. Khoảng PR > 0 · 20 giây; khoảng PR ngắn hoặc là bộ nối nhĩ thất (AV) hoặc có hội chứng tiền kích thích (ví dụ hội chứng Wolff-Parkinson-White). ECG bình thường
sẽ có T âm ở AVR và V1
2. bệnh nhân nam 25 tuổi đau ngực sau nâng tạ SR với loạn nhịp xoang, tần số 66, tái cực sớm lành tính (BER). loạn nhịp xoang được định nghĩa là nhịp xoang với thay đổi nhẹ (> 0 · 16 giây) trong các chu kỳ xoang. Điều này tạo ra bất thường nhẹ trong nhịp điệu và thường xảy ra ở tần số tim thấp (<70 lần / phút). BER là một biến thể bình thường thường gặp ở những người trẻ khỏe mạnh, đặc biệt là nam giới. Bệnh nhân thường có ST chênh lên lan tỏa trong nhiều
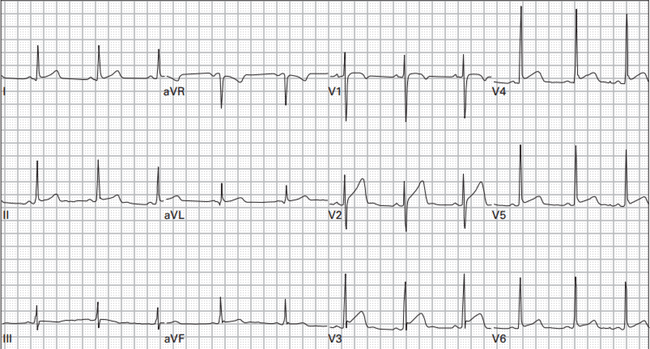
chuyển đạo, mặc dù không phải ở aVR hoặc V1. Không có sự thay đổi thuận nghịch đoạn ST giúp phân biệt với nhồi máu cơ tim cấp tính. viêm màng ngoài tim cấp tính có thể khó phân biệt với BER. Nếu có PR chênh xuống ở các chuyển đạo khác nhau sẽ ủng hộ chẩn đoán viêm màng ngoài tim cấp tính; Tuy nhiên, sự khác biệt giữa hai cái này thường phải dựa vào tiền sử và thăm khám: viêm màng ngoài tim cấp tính thường đau màng phổi rõ thay đổi theo vị trí tư thế cơ thể, và những bệnh nhân này có thể có tiếng cọ màng ngoài tim khi nghe tim
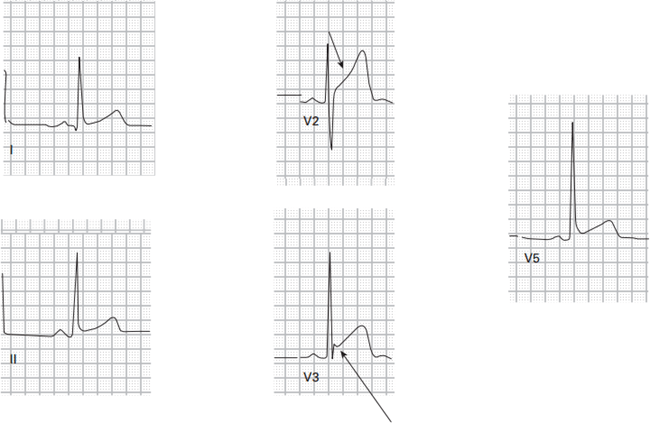
BER – lưu ý cao ST chênh lên hay gặp ở các chuyển đạo trước tim (V2, V3, V5) khi so sánh với các điện cực chi (I và II). Điểm J chênh lên kèm ST chênh giúp nâng đoạn ST và hình thái đoạn ST chênh, ST lõm (mũi tên lớn), một hình ảnh có thể giúp không nghĩ đến AMI. Điểm J thường không thấy hoặc không rõ ràng (mũi tên nhỏ)
3. bệnh nhân nam 76 tuổi khó thở
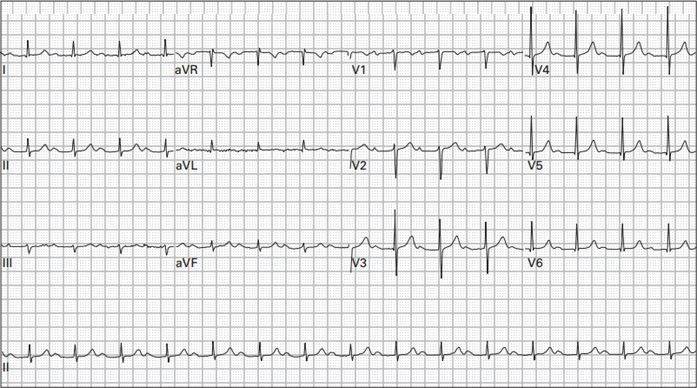
Nhịp xoang, tần số 91, block AV cấp 1. PR bình thường là 0 · 12-0 · 20 giây. Bệnh nhân này có block AV cấp 1 với 1 khoảng PR kéo dài 0 · 32 giây.
4. Bệnh nhân nam 64 tuổi không triệu chứng
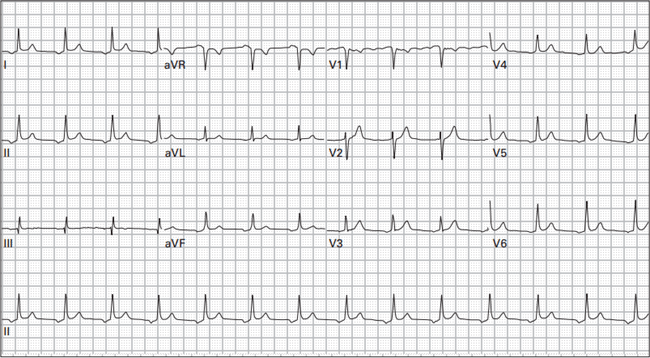
nhịp nhĩ lạc vị, tần số 82, ECG bình thường. sóng P âm trong các đạo trình I, II, aVF gợi ý
nhịp nhĩ lạc vị. PR bình thường (0 · 16 giây) khẳng định nhịp nhĩ lạc chỗ chứ không phải nhịp bộ nối AV
5. Bệnh nhân nữ 48 tuổi mới bắt đầu dùng thuốc điều trị THA, đau đầu nhẹ khi đi bộ
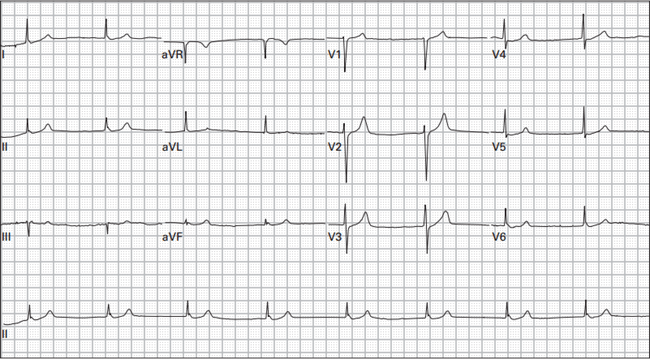
Nhịp bộ nối AV, tần số 50. Nhịp bộ nối AV thường kèm tần số 40-60l / phút và phức hợp QRS hẹp (trừ khi có một bất thường dẫn truyền, như block nhánh). Nếu nhịp bộ nối AV
Có tần số 61-100l / phút, nó được gọi là “nhịp bộ nối AV gia tốc;” nếu
Tần số > 100 / phút, nó được gọi là “nhịp nhanh bộ nối AV.” Trong nhịp bộ nối AV, sóng P có thể bị ẩn hoặc đi trước hoặc theo sau QRS. Khi những sóng P âm đi trước QRS,
Sẽ kèm theo PR ngắn (<0 · 12 giây). Bệnh nhân này gần đây đã bắt đầu dùng thuốc thuốc chẹn kênh canxi điều trị cao huyết áp. Khi ngừng thuốc, trở lại nhịp xoang và tần số thất tăng lên.
6. Bệnh nhân nam 75 tuổi sau 45 phút dùng tiêu huyết khối do nmct, hiện tại vẫn đang rất đau
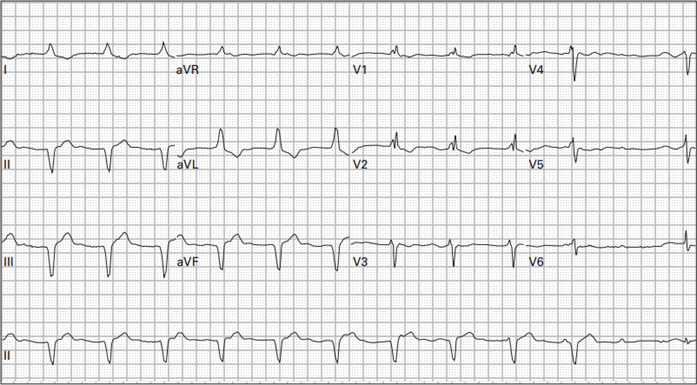
Nhịp nhanh thất tự phát gia tốc (AIVR), tần số 65. nhịp thoát tâm thất thoát thường có tần số 20-40 / phút. Khi nhịp thất là 40-110 / phút, nó được gọi là ” nhịp thất gia tốc‖ hay” nhịp nhanh thất tự phát gia tốc “. Khi tốc độ vượt quá 110 lần / phút sẽ chẩn đoán ” nhịp nhanh thất VT”. ECG của bệnh nhân này có hình ảnh phân ly AV, dễ dàng thấy ở phần sau của dải. AIVR thường gặp trong AMI, đặc biệt là sau khi dùng thuốc tiêu huyết khối. AIVR được cho là một dấu hiệu của tái tưới máu. Loạn nhịp của bệnh nhân này được giải quyết trong vài
phút mà không cần điều trị, điển hình của AIVR hậu dùng thuốc tiêu huyết khối.
7. Nam 43 tuổi không triệu chứng
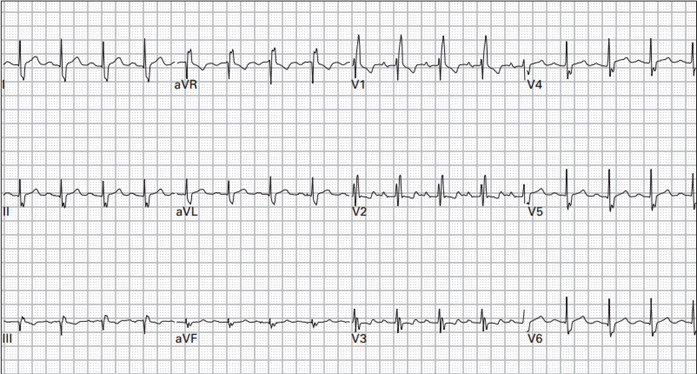
Nhịp xoang, tần số 100, RBBB. RBBB thường gắn liền với hình ảnh RSR ‘ở đạo trình phải trước tim, có thể có sóng R rộng hoặc hình ảnh QR. Sóng S rộng ở chuyển đạo bên (I, aVL, V5, V6) và QRS ≥0 · 12 giây. Nếu tất cả các tiêu chí được đáp ứng trừ QRS ≤0 · 12 giây ta sẽ chẩn đoán RBBB không hoàn toàn. V1-V3 thường có ST chênh xuống và T âm. Nếu có ST chênh lên cần theo dõi đề phòng nguy cơ AMI
8. bệnh nhân nam 82 tuổi gần đây có tăng liều beta blocker. thấy chóng mặt khi gắng sức
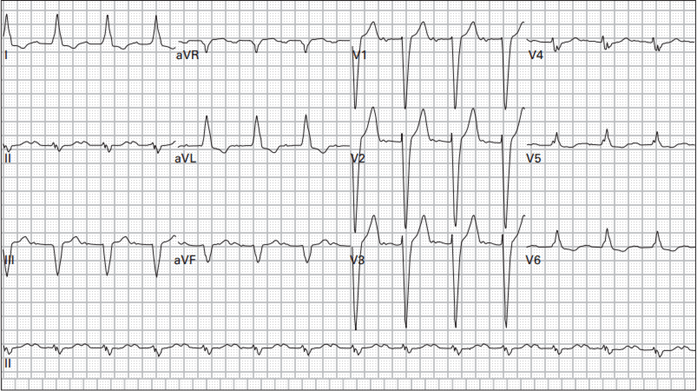
Nhịp xoang, tần số 80, block AV câp 1, LBBB. LBBB được đặc trưng bởi hình ảnh kéo dài
Thời gian QRS ≥0 · 12 giây, trục trái, sóng R 1 pha rộng trong đạo trình I và V6, và sóng S sâu ở V1 (thường không có sóng R). ST và T đi hướng ngược lại với vector QRS trong tất cả chuyển đạo .Bệnh nhân này có cả LBBB và block AV cấp 1. Việc tăng liều thuốc beta-blocker gây tăng đáng kể khoảng PR
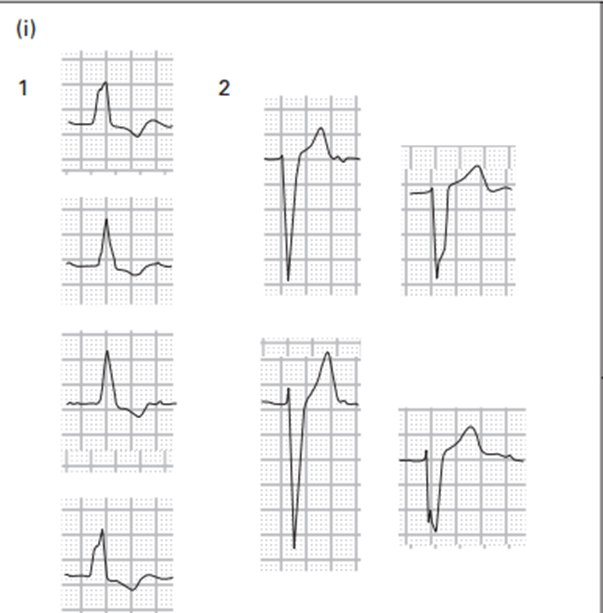
Các chuyển đạo bên (I, AVI, V5 và V6) trong LBBB; chú thích ST chênh xuống với sóng T âm.
2: chuyển đạo trước tim (V1-V4) trong LBBB; lưu ý ST chênh lên và sóng T nổi bật
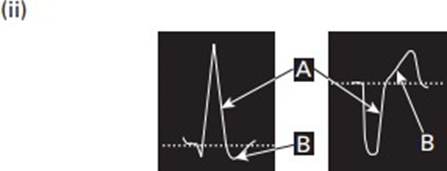
Mối liên quan QRS đến đoạn ST- sóng T trong LBBB, gọi là quy tắc
―appropriate discordance‖
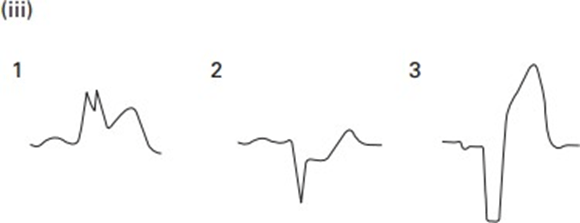
thay đổi trên điện tim kết hợp với hội chứng mạch vành cấp tính trong LBBB. 1: đoạn ST chênh lên: ST được nâng lên và cùng phía với đường cơ sở ở đoạn cuối QRS
2: ST chênh xuống : STcùng phía với đường đoạn cuối QRS 3: ST chênh quá cao năm đối diện với đoạn cuối QRS
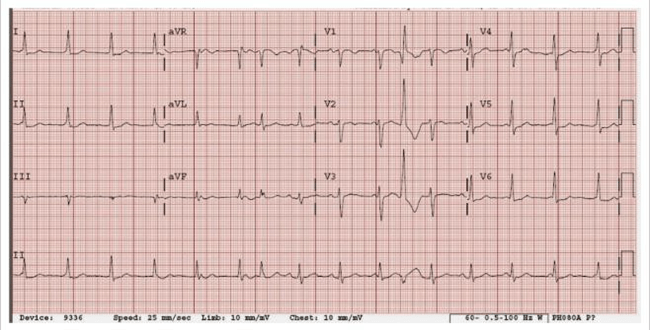
Nhịp gì và có block AV?
Nhìn ECG này dễ thấy dường như sóng P và QRS hình như không có liên quan nhau.Rất dễ để tin rằng đây là block AV hoàn toàn
Nhưng đây không phải block AV mà là nhịp bộ nối gia tốc, nhịp xoang rất gần nhịp bộ nối như hình dưới đây
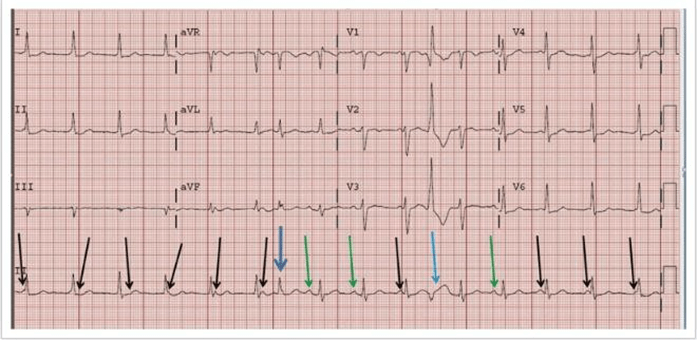
mũi tên màu đen cho thấy sóng P không được dẫn truyền hoặc do nhịp xoang ngay sau nút AV hoặc nếu các sóng Pđi trước QRS, thì nhịp nối nhanh chóng bắt đầu 1 trước khi nút xoang phát nhịp qua nút AV. Trong những nhịp này, sóng P dương thẳng vì nó là nhịp xoang. Đó là nhịp xoang do nút xoang phát nhịp trước khi dẫn truyền từ nút AV có thể ảnh hưởng đến nó. Nếu nút AV tác động đến nhĩ đầu tiên sẽ gây sóng p âm. Các mũi tên màu xanh lá cây cho thấy nhịp xoang bình thường được tiến hành trước khi nút AV có thể bắt đầu một nhịp của riêng mình. Các mũi tên màu xanh trời cho thấy ảnh trùng nhịp: trong trường hợp này, các sóng P xảy ra đủ muộn, do thời gian dẫn truyền qua nút AV, QRS không hoàn toàn ở trạng thái trơ; Tuy nhiên, trơ 1 chút nên QRS hơi bất thường (rộng hơn). Các mũi tên màu xanh trời hẹp cũng là một nhịp phản ứng tổng hợp; các sóng P được chôn trong sóng T phía trước (đó là lý do tại sao sóng T phía trước vẻ lớn hơn so với tất cả các sóng T khác. nhánh phải vẫn trơ, nhưng nhánh trái thì không, vì vậy nó có hình ảnh block nhánh phái
QRS số 8 nắm giữ đáp án case này với khoảng RR ngắn hơn và PR bình thường chỉ ra rằng dẫn truyền này từ sóng P. Như vậy, ở đây không có block AV hoàn toàn, chỉ có nhịp bộ nối AV tăng tốc với AV phân ly. Nhịp bộ nối gia tốc là 1 nhịp rất đều, QRS xảy ra với khoảng RR ngắn sẽ không phải từ bộ nối nhưng là nhịp tiến hành từ phía trên
Vì vậy, ở đây không có block AV hoàn toàn và nguy hiểm cho bệnh nhân AV phân ly không nhất thiết có nghĩa là block AV hoàn toàn
Bệnh nhân này quá liều oxcarbazepine =))
9. Bệnh nhân nữ 49 tuổi thỉnh thoảng đau ngực
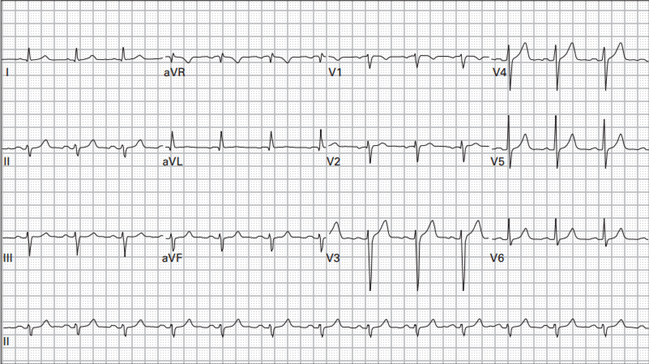
Nhịp xoang, tần số 81, LAFB. LAFB thường kèm với QRS trục trái, hình ảnh qR (Q nhỏ và R lớn) hoặc sóng R trong chuyển đạo I và aVL, rS (r nhỏ và S lớn) trong chuyển đạo DIII, và không có các nguyên nhân khác gây trục trái. Chẩn đoán phân biệt trục trái bao gồm
: LAFB, LBBB, nhồi máu cơ tim thành dưới, phì đại thất trái, nhịp thất lạc vị, nhịp máy tạo nhịp và Hội chứng WPW
hãy bắt đầu với những cái sâu và xa hơn
Bệnh nhân nam 51 tuổi đang điều trị methadone mãn tính cai nghiện vào cấp cứu vì ho và khó thở. Khám thấy thở nhanh, bão hòa oxy 88%
X-quang thấy thâm nhiễm thùy dưới bên phải. kali 3,6 mEq / L và magiê là 2,0 mEq /
L. ECG thấy loạn nhịp xoang có sóng U và QTc kéo dài (Hình 1)
Ông được tiêm tĩnh mạch moxifloxacin khi ở phòng cấp cứu. 12 giờ sau đó
ông cảm thấy lo lắng và vã mồ hôi. ECG nhịp xoang và nhiều ổ phát nhịp ngoại vi ở thất (ventricular ectopics). Ngoại tâm thu thất nhịp đôi (bigeminy) với QT kéo dài
(Hình 2). Vài phút sau, bệnh nhân mất mạch và ngưng thở kèm rung thất (Hình 3). bắt đầu ép tim và nhịp tự phát nút xoang xuất hiện. điện tâm đồ có QT kéo dài liên tục với khoảng QT (QTc) 630 ms. nguyên nhân có thể gây ngừng tim của bệnh nhân này là gì?
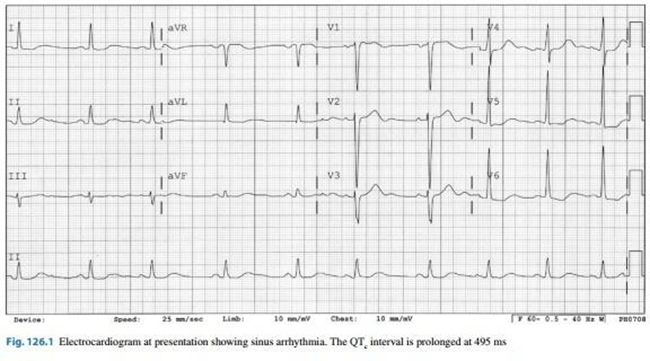
Khoảng QT, máy đo điện tim tái cực tâm thất thường bị bỏ qua hoặc hiểu sai. Sự thay đổi thời gian và cơ chế tái cực thất có thể dẫn đến nhịp nhanh thất đặc biệt là xoắn đỉnh. Các yếu tố ảnh hưởng đến khoảng QT rất phức tạp, có thể bao gồm một loạt các rối loạn các kênh, thay đổi trong phân bổ thần kinh tự động và các yếu tố như thuốc hay rối loạn điện giải. Bệnh nhân mô tả dùng methadone có tác dụng phụ làm QT kéo dài, do đó cần kiểm tra các loại thuốc phối hợp.
ông đã bắt đầu dùng kháng sinh fluoroquinolon, moxifloxacin.
Sự kết hợp của methadone và moxifloxacin ở bệnh nhân này dẫn đến QT kéo dài và xoắn đỉnh
Khi thuốc gây xoắn đỉnh (hoặc thậm chí gây kéo dài QT đáng kể mà không xoắn đỉnhcần ngay lập tức ngưng thuốc.
tạo nhịp tạm thời có thể dùng để ngăn chặn ngừng tim do nhịp nhanh trên thât. Thuốc điều nhịp như isoproterenol hoặc atropine cũng có thể dùng để tăng nhịp tim nhằm rút ngắn khoảng QT và loại bỏ rối loạn nhịp “ngắn dài ngắn”.
Tiêm tĩnh mạch magnesium sulfate, an toàn và hiệu quả, để chấm dứt xoắn đỉnh. kali nên duy trì ở mức cao (trong ngưỡng bình thường). Nếu vẫn tiếp tục
cần dùng liều thấp dopamine tĩnh mạch để hỗ trợ điều nhịp để ngăn rung thất. Moxifloxacin được ngưng cho đến khi QT về bình thường.
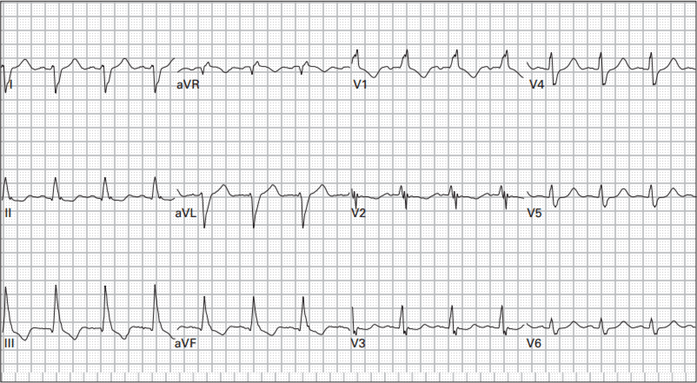
bệnh nhân nữ 65 tuổi nghiện thuốc lá, tiền sử khí phế thũng
nhịp xoang, tần số 85, RBBB, LPFB. Sự kết hợp của RBBB với block nhánh gọi là block 2 nhánh “block bifascicular.” LPFB ít gặp hơn LAFB. Nó thường xảy ra đồng thời với RBBB hơn là 1 mình nó. Sóng T âm thường thấy ở các chuyển đạo dưới ở block 2 nhánh này. LPFB thường kèm trục phải QRS, hình ảnh qR (q nhỏ và R lớn) ở DIII, và không có các nguyên nhân khác gây trục sang phải. Chẩn đoán phân biệt trục phải gồm: LPFB, nhồi máu cơ tim thành bên, phì đại thất phải, cấp tính (trong thuyên tắc phổi) và mạn tính (như khí phế thũng) bệnh phổi, nhịp thất lạc vị, tăng kali máu, quá liều thuốc chẹn kênh natri (ví dụ thuốc chống trầm cảm theo vòng). người lớn hay trẻ có tim nằm ngang cũng có trục QRS phải trên điện tâm đồ.
Bệnh nhân nữ 51 tuổi đau giữa xương ức
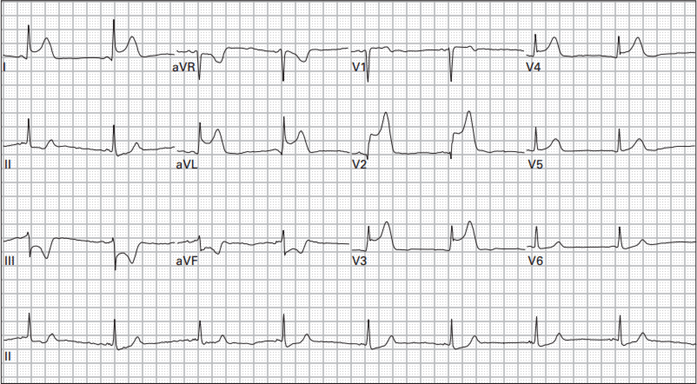
Nhịp bộ nối AV, tần số 50, NMCT thành trước bên. Có sóng P và PR ngắn (<0 · 12 giây) đặc trưng cho nhịp bộ nối AV. ST chênh lên ở chuyển đạo trước tim nên chẩn đoán NMCT thành trước. ST chênh lên ở đạo trình I và aVL gợi ý NMCT thành bên thất trái. ST chênh xuống đối xứng ở chuyển đạo dưới
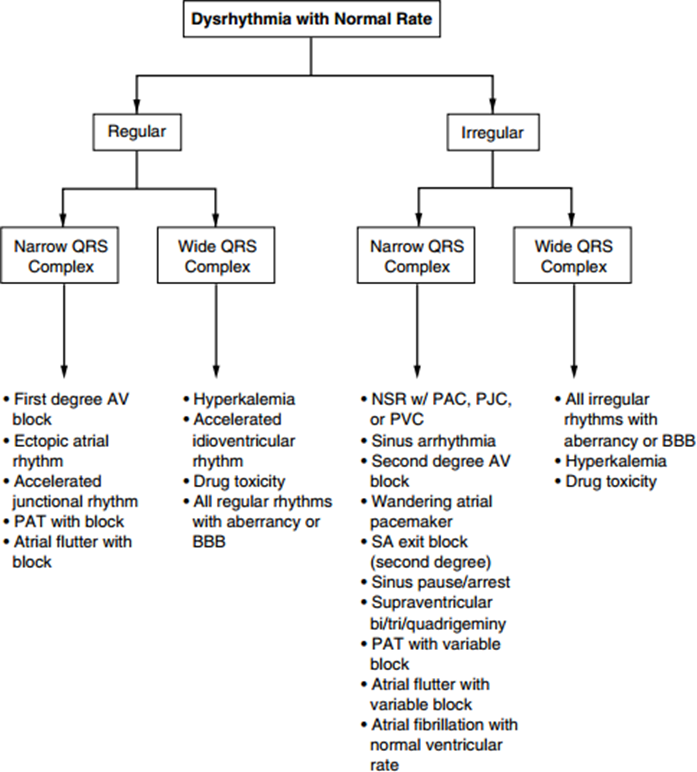
156. Nhịp nhanh QRS rộng: VT hay SVT với dẫn truyền lệch hướng
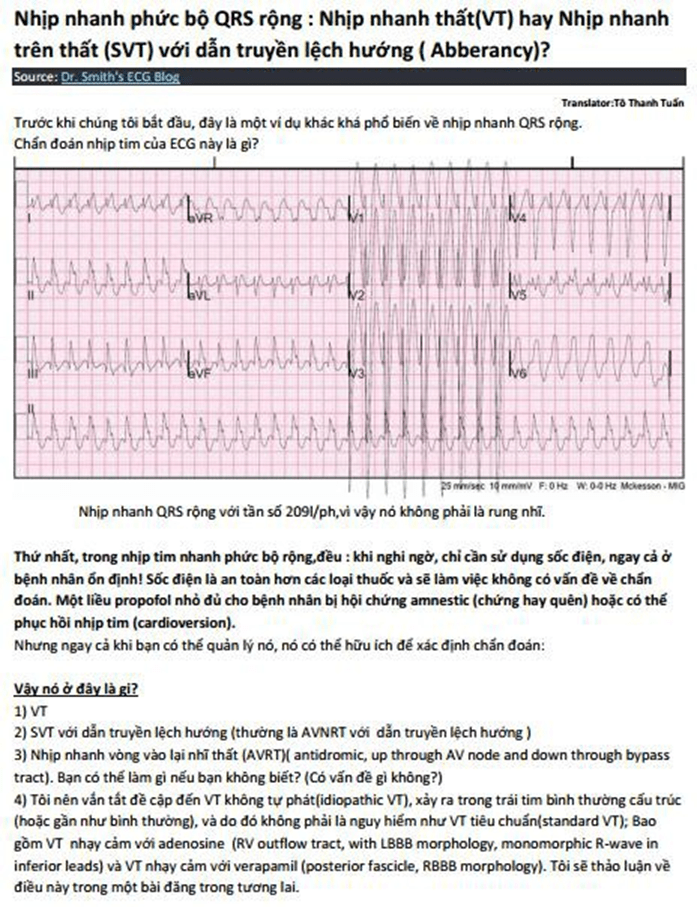

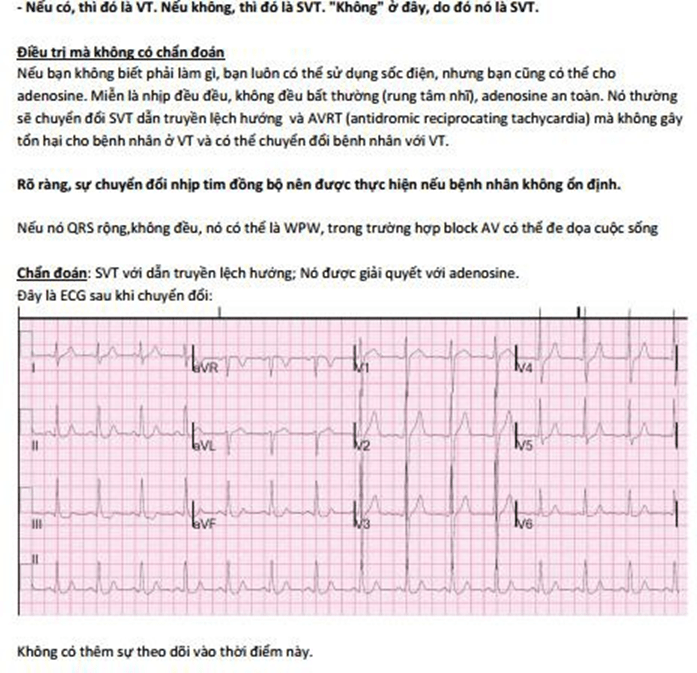
157. Khi nào streptokinase sẽ chính thức đánh bại PCI ?
STEMI là trường hợp tối cấp cứu trong y tế. nguy cơ tử vong cao nhất trong giờ đầu tiên
Đây là bệnh nhân vào cấp cứu trong vòng 30 phút đau ngực. men tim được làm và siêu âm tim thấy giảm nhiều chuyển động vùng LAD
Bạn là bác sĩ tim mạch, bạn sẽ làm gì?
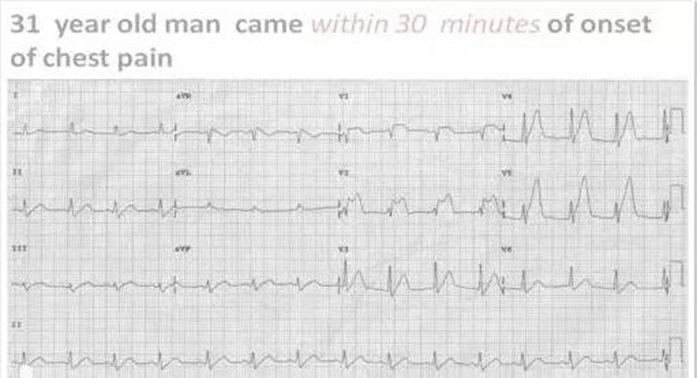
Báo cho phòng cath? Gửi bệnh nhân trực tiếp đến phòng cath?
Điều này không dễ khi chúng ta ở 1 đất nước kém phát triển và bệnh nhân nghèo Ông đã được tiêm 1 liều streptokinase giá 2.000 Rs (50 đô la) ở Ấn Độ.
Và hãy xem kết quả!
Bạn có thể tưởng tượng người đàn ông đã có nhồi máu cơ tim lớn trước đó 1h?
Bất kỳ sự can thiệp nào được thực hiện ngay lập tức đều có ảnh hưởng lớn đến kết cục. Khi bệnh nhân đến với bạn sớm trong vòng 30 phút và bị STEMI
Bạn sẽ làm gì?
Mục đích không nên để cứu vãn cơ tim, thay vì ngăn ngừa biến chứng của ACS và hủy quá trình MI!
Sao có thể như thế được ? Bạn có thể giải quyết STEMI bằng PCI mà?
Vì chúng ta phải hành động nhanh, PCI thường thất bại 9/10 trường hợp cứu STEMI
Lựa chọn tốt nhất là thực hiện can thiệp ngay lập tức, tiêu huyết khối dùng rất tốt và tiết kiệm được chi phí vô cùng lớn
Đây là điều mà bệnh nhân này được can thiệp. hãy xem kết quả, chụp mạch sau đó thấy LAD thông hoàn toàn, không có stent phải đặt. bệnh nhân được khuyên nên dùng statins, beta blocker và thuốc kháng tiểu cầu
Thông điệp cuối cùng
Đừng chế giễu bất kỳ phương thức điều trị đơn giản và rẻ tiền. Chúng có thể là phương pháp điều trị hiệu quả nhất
158. Phù chân có xuất hiện trong suy tim tâm trương?
Không thể xảy ra.
Thường gặp như trong suy tim tâm thu
Có thể xảy ra với số lượng đáng kể. Hiếm.
Đáp án: 4
3 cũng có thể đúng.
Khi suy tim được định nghĩa bởi các tiêu chuẩn Framingham từ nhiều thập kỷ trước, thực thể của suy tim tâm trương không tồn tại. Bộ ba cổ điển của suy tim tâm thu: phù chân, tăng JVP và rales đáy phổi
Cơ chế
Đối với cơ chế gây phù cần phải có giữ Na và H20. Để có thể gây phù cần 1 trong 2 điều sau: hạ protein máu và rối loạn lưu thông bạch huyết
– Tăng áp lực tĩnh mạch
– Giảm bài tiết Na và nước ở thận Cả 2 yếu tố gây xuất hiện phù cổ điển
Trong suy tim tâm trương thất trái, sự gia tăng áp suất tĩnh mạch hệ thống ít rõ rệt hơn. Do đó, phù chân ít gặp hơn. Nhưng trong bất kỳ loại suy tim nào, chỉ số tim CI có xu hướng giảm ít nhất là 1 chút. Thận là cơ quan đầu tiên cảm nhận được điều này, và các nephron bắt đầu giữ lại Na và nước như thể cơ thể sẽ đối mặt với sự khan hiếm muối và nước nặng (thực sự là một báo động giả!)
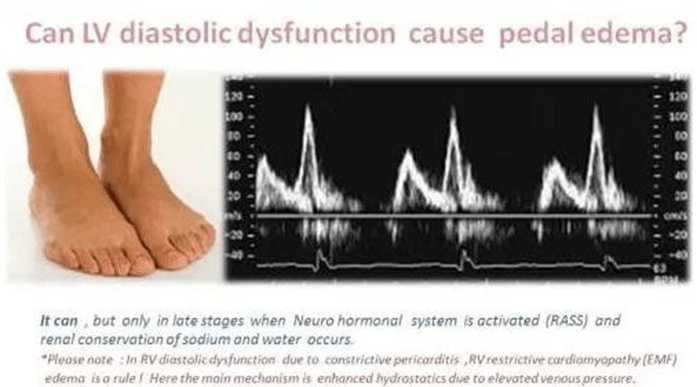
Các yếu tố quyết định khác có thể liên quan phù chân.
– Chức năng thận.
– Trạng thái thể tích lòng mạch
– Những thay đổi liên quan đến mạch máu do HT gây ra
– Nồng độ protein huyết thanh.
– Trương lực tĩnh mạch (bơm tĩnh mạch tốt ở chân giúp tránh và hạn chế phù)
– Tính toàn vẹn của lưu thông bạch huyết.
– Mật độ mỡ dưới da và kháng mô kẽ.
Tất cả có thể làm thay đổi áp suất tĩnh tại chỗ. Các yếu tố này hoạt động trong các lượng tử khác nhau và vì lý do này chỉ có một số ít bị phù đáng kể trong suy tim.
* Xin lưu ý, các thuật ngữ rối loạn chức năng tâm trương và suy tim không thể được sử dụng hoán đổi cho nhau. Rối loạn chức năng thường là tham số siêu âm trong khi suy tim là có đối chứng lâm sàng
159. chúng ta có nên dùng amiodarone thường xuyên sau rung thất nguyên phát?
Rung thất là rối loạn nhịp tim đáng sợ nhất trong STEMI. Nếu nó xuất hiện bên ngoài bệnh viện, thường vô phương cứu chữa. Nếu xảy ra trong bệnh viện, thường được cấp cứu và ít khi tử vong
Khi nó xảy ra trong những giờ đầu của STEMI nó được gọi là VF nguyên phát
Mặc dù nó là một rối loạn nhịp tim, nhưng VF nguyên phát thường là loạn nhịp tưới máu. Không có thực thể nào được gọi là VF nguyên phát tái phát
Nếu VF tái phát xuất hiện thì một số cơ chế khác sẽ được nghi ngờ (Thuốc, thiếu oxy, vết sẹo, bất thường kênh ion vv)
Cơ chế
VF nguyên phát do thiếu máu cục bộ còn VF thứ phát là do vùng bị nhồi máu gây nên. Thiếu oxy, LVF hoặc những vết sẹo cũ cũng có thể có liên quan.
Làm thế nào để chấm dứt VF nguyên phát?
Khử rung tim tức thời là lựa chọn duy nhất.
Sau khi cấp cứu chuyển nhịp thành công VF nguyên phát, chúng ta có nên dùng thuốc chống loạn nhịp thường xuyên?
Không. Không nên dùng thường xuyên
Điều gì sẽ xảy ra nếu NTTT và VT không dai dẳng tiếp tục xuất hiện trong những giờ tiếp theo của 1 đợt VF nguyên phát?
Lúc này thích hợp dùng Amiodarone hoặc lignocaine. Sau khi thường không cần uống Amiodarone nếu chức năng LV được bảo tồn tốt
Lợi thế và bất lợi của Amiodarone
Tác dụng làm giảm hoạt động cơ tim của Amiodarone là 1 yếu tố ngăn cản việc dùng thường xuyên của nó.
Amiodarone gây ra nhịp chậm (nếu nó không phải là block AV) có thể là một lợi thế như MVO2 có thể sẽ giảm.
Nhân tiện, Lignocaine tác dụng thế nào so với Amiodarone?
Nó cũng là một loại thuốc tốt với tác dụng phụ ít hơn. Nhưng nghiên cứu ALIVE đã gây ra cái chết cho loại thuốc kỳ lạ này. Nhiều người (ít nhất là tôi!) Vẫn tin rằng Lignocaine là loại thuốc rất tốt và dùng rất hiệu quả trong tim mạch
Vậy thông điệp cuối cùng là gì?
Dù nhiều ý kiến không cần thiết phải dùng chống loạn nhịp sau khi đảo ngược thành công VF nguyên phát, nên thận trọng cân nhắc những rủi ro. Chúng ta không thể sử dụng nó như một thói quen.
Tuy nhiên, nên dùng nó nếu khôn ngoan hơn để ngăn chặn các giai đoạn tiếp theo của VF (mặc dù hiếm).
Nếu bạn ở CCU, có thể không cần dùng tiếp amiodarone
Nếu bạn không tin tưởng đồng nghiệp hoặc lăn tăn bạn có thể cho dùng tiếp loại thuốc này
Xin lưu ý
** Không bao giờ nghĩ tới đặt ICD ở bệnh nhân VF nguyên phát vì nó là một chống chỉ định tuyệt đối.
*** VT / VF tái phát trong trường hợp STEMI thường được gọi là cơn bão điện. Đó là trường hợp hiếm hoi cần phải CABG / PCI ngay lập tức và cắt cơn VT. Một lần nữa ICDs chống chỉ định ở đây vì pin sẽ cạn kiệt nhanh chóng. Thêm nữa ICD không trị được VT, trong khi đốt ablation RF có thể cắt cơn VT và ngăn ngừa nó, chữa tận gốc. Tuy nhiên cần nhớ chỉ 20% VT phù hợp với cắt bằng đốt RF. Vì vậy cần kết hợp đốt RF và ICD
160. Cơ chế chống THA của beta blocker
1. giảm tần số tim
2. giảm cung lượng tim
3. giảm co cơ âm
4. giảm nhạy cảm của mạch máu với catecholamine
5. giảm bài tiết renin và trương lực mạch máu Đáp án:5 (có thể là 4)
Sự hiểu biết của chúng ta về hoạt động của chất ức chế beta trong THA đã thay đổi đáng kể qua nhiều năm. Tác động lên co cơ âm của cơ tim làm giảm huyết áp không được coi là điều quan trọng nữa. Bây giờ chúng ta đã biết, chất chẹn beta có thể làm giảm đáng kể kháng trở mạch máu ngoại vi (có 1 ngày, chúng ta sẽ cho rằng điều ngược lại là đúng, tức là khi thuốc chẹn beta bị chặn, hoạt động alpha sẽ vượt qua để gây ra kháng trở mạch máu quá mức!) . Khái niệm này không bao giờ được chứng minh một cách thuyết phục ngay cả trong cơn đau thắt ngực Prinzmetal * chống chỉ định dùng chẹn beta vì sợ làm tăng tình trạng co thắt mạch
* Lưu ý: với những người có hiện tượng Raynaud đặc biệt có bệnh mạch máu ngoại biên
Các yếu tố khác ảnh hưởng đến thuốc chẹn beta trong THA
Thuốc chẹn beta làm giảm áp lực tới trung tâm adrenergic, tác động tới trung tâm vận mạch ở não
Vai trò của thuốc chẹn beta trong tăng huyết áp tâm thu ở người cao tuổi là làm giảm dp
/ dt cơ tim (tức là co bóp)
Các chất chẹn beta có giãn mạch mới như Nebivolol, (qua trung gian Nitric Oxide Và Carvidilol có thể có thêm lợi thế trong việc kiểm soát huyết áp
thuốc chẹn beta kết hợp tốt với thuốc lợi tiểu như hydrochlorthaizide. Điều này giúp kiểm soát các dạng THA đặc biệt nghiêm trọng ở người già và trẻ
Thông điệp cuối cùng
Sự thay đổi phản ứng mạch máu với catecholamine là cơ chế quan trọng nhất để giảm huyết áp.
Đây có thể là hậu quả trực tiếp của việc
1. Ngăn chặn các thụ thể adrenergic của mạch.
2. gián tiếp thông qua sự ức chế tiết Rennin.
161. Thời gian cửa sổ tối đa tiến hành PCI trong STEMI
Chúng ta biết PCI là 1 cuộc chạy đua với thời gian cho cả bệnh nhân và bác sĩ
Giới hạn trên nào cho thời gian PCI trong STEMI?
6 giờ
12 giờ
24 giờ
36 giờ
54 giờ
Thời gian không quan trọng. Bạn có thể làm PCI càng sớm càng tốt nếu bệnh nhân có đủ điều kiện và bạn có chuyên môn
Trả lời: 2
Xin lưu ý rằng chỉ có một ngoại lệ. Sốc tim có thể kéo dài thời gian cửa sổ (Có thể đến 54 giờ). PCI có thể làm nếu sốc khởi phát trong vòng 36h bị STEMI và làm trong vòng 18h sau khi khởi phát
Mặc dù chúng ta cấm PCI thực hiện sau 12h, các bs tim mạch có thể tiến hành sau đó với tên PCI trì hoãn hoặc PCI giải cứu. đây là sự nhạo báng khái niệm về thời gian cửa sổ trong can thiệp cho STEMI
162. Khi STEMI không có hình ảnh cổ điển ST chênh lên (STE)
“STEMI là nmct cấp “, và “nmct cấp là STEMI”! Đây là cách chúng ta đã được dạy qua nhiều năm.
Nhưng STEMI có thể xuất hiện bởi 1 hay nhiều hình thức dưới đây
1. Nhồi máu cơ tim có ST chênh xuống ở V1 đến V3 (Nhiều trường hợp nhầm với đau thắt ngực không ổn định, và bỏ qua không được can thiệp tái tưới máu)
2. Chỉ với sóng T cao (TEMI)
3. blck nhánh trái
4. xuất hiện như nhịp nhanh thất VT.
5. Khi STEMI kèm block AV hoàn toàn có thể không thấy ST chênh lên
6. ECG không điển hình, có thay đổi tinh tế đặc biệt ở người cao tuổi, bệnh tiểu đường và ở những bệnh nhân bị LVH.
7. Cuối cùng, MI mà ECG bình thường tới 10% bệnh nhân.
Hiện tại, chỉ có số 1 và 3 được chấp thuận cho việc dùng thuốc tiêu huyết khối hay PCI. Những người không may mắn rơi vào các số khác sẽ mất cơ hội được tái tưới máu và không có các guideline dành cho những trường hợp này
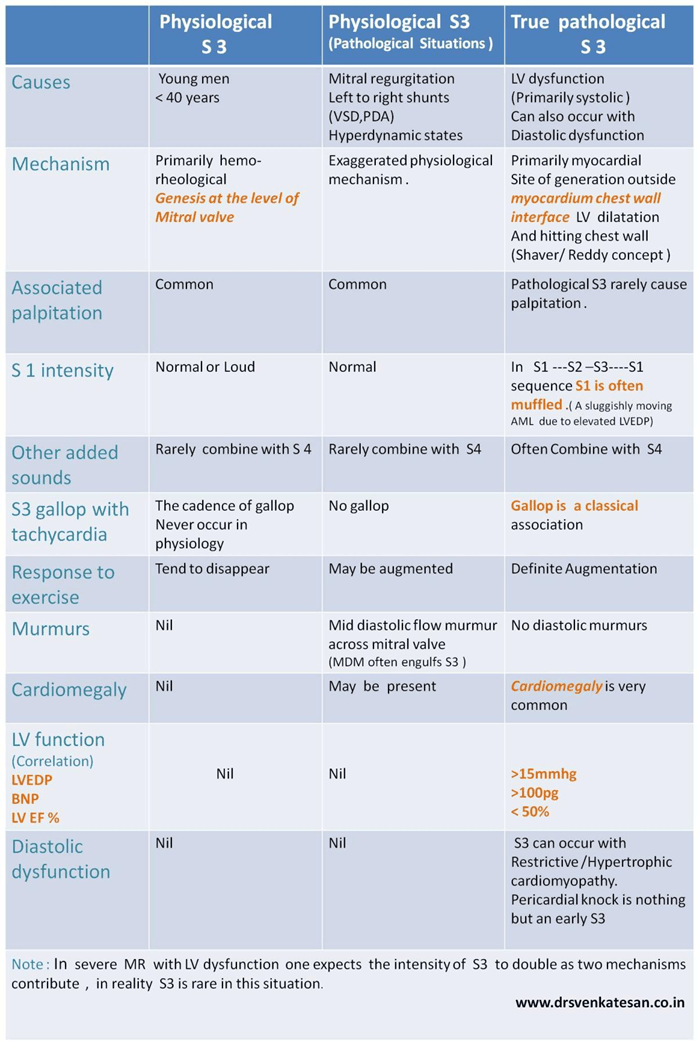
163. Khi rung nhĩ xuất hiện nhịp chậm, hãy nghĩ đến bệnh lý “nút xoang và AV”
Rung nhĩ là một trong những rối loạn nhịp hay gặp trong tim mạch lâm sàng. Tần số nhĩ có thể lên đến 600l trạng này mặc dù nhịp/p mặc dù chỉ 1 phần nhỏ của nó dẫn truyền xuống tâm thất. nhờ vào nút AV, nó hoạt động như trạm giảm dẫn truyền, do đó trong hầu hết giai đoạn của AF, tần số thất chỉ dao động từ 150-220. Chúng ta cũng biết, có sự dẫn truyền qua đường phụ nối tâm nhĩ với tâm thất có nguy cơ dẫn truyền 1:1 dẫn tới rung thất và tử vong (đột tử trong hội chứng WPW)
Một trường hợp lâm sàng
Ngày nọ, có bs gọi cho tôi thông báo về 1 trường hợp bệnh nhân bị rung nhĩ và tụt huyết áp
Tôi nói với anh ta, kiểm soát nhịp tim với Amiodarone và tôi sẽ đến trong thời gian nhanh nhất.
Anh ta trả lời, ECG có nhịp chậm. đây là 1 case ECG thú vị
Đây là một người đàn ông 73 tuổi vào viện vì ngất
Rung nhĩ tâm với nhịp chậm thất
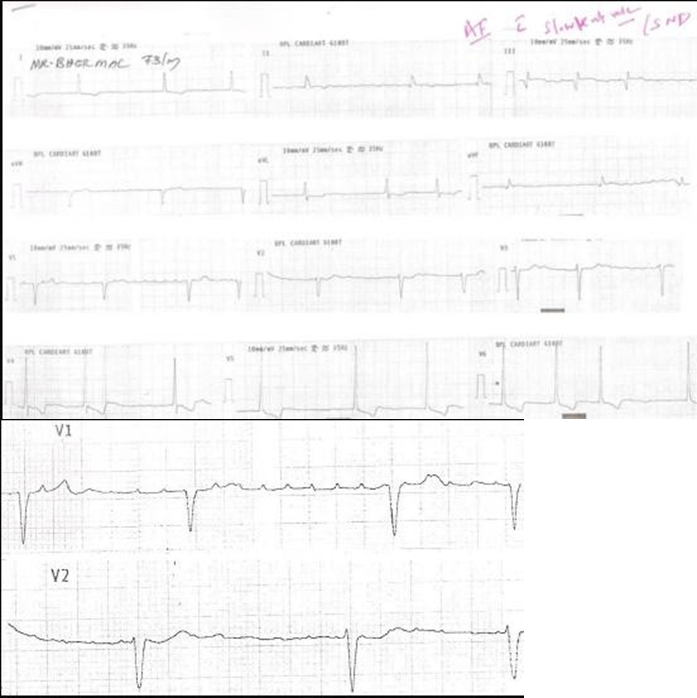
Góc phóng to của V 1 và V 2. Lưu ý tần số thất 40 / mt ngay cả khi sóng f ghi được> 300 mt. cấu trúc tim bệnh nhân bình thường, bệnh nhân được khuyên đặt máy tạo nhịp VVI
Trong khi rung nhĩ chủ yếu là nhịp nhanh, thỉnh thoảng cũng giống như bệnh nhân ở trên, xuất hiện nhịp chậm!
Điều này xảy ra như thế nào?
Như đã đề cập trước khi nút AV hoạt động như một trạm điều chỉnh dẫn truyền.
Làm thế nào nút AV có thể điều chỉnh? Đây là thuộc tính sinh lý chính của nút AV. Khi chức năng này hoạt động quá nhiều chúng ta sẽ gọi đó là đáp ứng của nút AV. 1 số người tin rằng đó là block AV độ cao, 1 số cho rằng đơn giản chỉ là tình trạng cường phó giao cảm
Một khả năng là nó là cách thoát khỏi block AV hoàn toàn và những gì bạn chứng kiến không có gì ngoài nhịp thoát bộ nối (nhưng ở đây RR sẽ khá đều )
Các thuốc có thể gây block AV quá mức (Digoxin / Verapamil) có thể bắt chước hình ảnh giống nhau.
Mối quan hệ giữa rối loạn chức năng nút xoang (SND) và rung nhĩ là gì?
AF với đáp ứng chậm hay gặp ở người cao tuổi có rối loạn chức năng nút xoang
AF có thể được kết hợp với SND theo hai cách
Bệnh tâm nhĩ và rối loạn chức năng nút xoang hay xảy ra cùng nhau. Điều này không quá ngạc nhiên. Nút xoang được bao quanh bởi các mô nhĩ trái theo chiều dài và chiều rộng của nó. Khi bệnh thoái hóa và thâm nhập của tâm nhĩ xảy ra nó có thể gây ra SND, cũng như rung nhĩ
Trong khi khả năng khác là AF là phản ứng điện mặc định đối với SND. Có một số bằng chứng cho thấy tâm nhĩ có thể giải phóng một nhịp thoátlạc vị để thhoais hóa thành AF hoặc khỏi lạc lối, có thể thoái hóa thành AF
Tần số thất được kiểm soát và đáp ứng thất chậm trong AF là gì?
Khía cạnh này không được xác định rõ ràng trong y văn Đáp ứng bình thường trung bình HR 70-90 / mt
Đáp ứng thất chậm là <60 / mt
Nhịp chậm bệnh lý khi HR<50 hoặc khi nhịp chậm kèm theo có biểu hiện triệu chứng Holter có thể giúp theo dõi trong những trường hợp này.
Tỉ lệ mắc bệnh nút AV trong rối loạn chức năng nút xoang SND là gì?
Bệnh lý nút AV gặp trong 30% SND.
Có lợi thế về lâm sàng khi có bệnh lí nút AV trong AF?
Có vẻ như vậy, miễn là bệnh nút nhĩ thất AV không dẫn đến block AV hoàn toàn CHB. Dẫn truyền chậm là phản ứng mong muốn ở bệnh nhân bị đau thắt ngực và bệnh cơ tim (đặc biệt là trong nhịp tim nhanh).
Rung nhĩ là chủ yếu là rối loạn nhịp nhanh, thỉnh thoảng xuất hiện nhịp chậm, trong trường hợp này phải nghi ngờ có rối loạn chức năng nút xoang (còn gọi hội chứng tachy brady). Điều quan trọng phải nhận ra nó vì nhiều khi dẫn truyền chậm xuất hiện chỉ với 1 liều duy nhất amiodarone hoặc DC shock
164. hạ kali có gây liệt cơ tim?
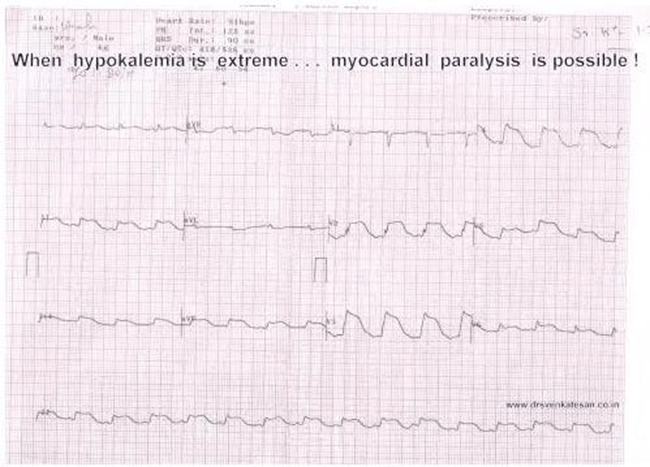
Bn nữ vào viện vì khó thở. ECG nghi STEMI, bn chuẩn bị được dùng tPA thì kết quả kali 2,3. Dừng tPA, bù kali, ECG về bình thường
165. cơ chế sóng T cao trong nmct cấp
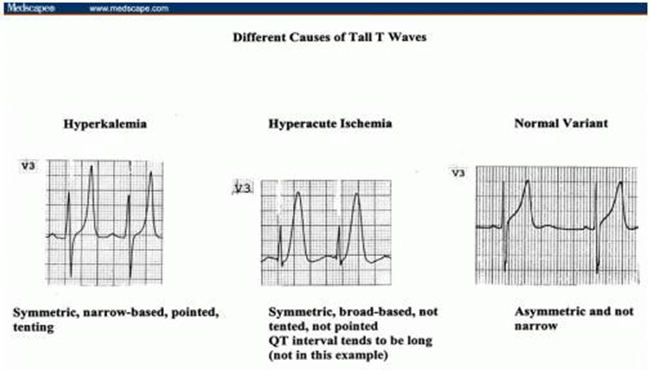
Một vài suy nghĩ
sóng T cao thấy trong giai đoạn rất sớm của STEMI (trong vòng 30 phút) Cơ chế là gì? Do sự thay đổi của ST chậm hơn độ tăng của sóng T (có thể chồng chéo lên nhau) có thể không liên quan đến tổn thương hiện tại.Đó là sự thay đổi cố hữu trong sự hình thành của sóng T. Sóng được ghi lại cực nhanh trong phase 3 khi 3K+ đi ra ngoài
Tác dụng của thiếu máu cục bộ trên kênh K + là gì?
Không có câu trả lời thống nhất (block, kích thích, 2 pha, thay đổi…)
Có 6 kênh K quan trọng trong mỗi tế bào cơ tim làm cơ chế thêm phức tạp.
Các tế bào thiếu máu sẽ gây rò rỉ kali hay giữ lại nó?
Mặc dù gồm cả 2 nhưng chủ yếu sẽ gây rò rỉ kali ra ngoài làm tăng kali ngoại bào khu vực đó làm xuất hiện sóng T cao
Ảnh hưởng của khoảng QT trên hình thái sóng T là gì?
QT dài trong hạ kali sẽ kéo sóng T xuống hoặc thậm chí đảo ngược nó . QT ngắn có xu hướng đẩy nó lên như trong ERS. Ảnh hưởng của thiếu máu trên khoảng QT lại một lần nữa không thể đoán trước được.
Ảnh hưởng của tái tưới máu lên sóng T?
T cao thường có xu hướng thoái triển khi kali bị đẩy trở lại tế bào hoặc đi xa khỏi khu vực thiếu máu cục bộ
Nói một cách đơn giản tôi tin rằng cơ chế của sóng T cao thiếu máu gần như là do tăng kali máu. Đáy sóng T hẹp và nhọn như trong CKD vì ST hẹp và lều như trong CKD bởi vì ST chênh lên luôn có xu hướng mở rộng đáy sóng T, hơn nữa khoảng QT kéo dài trong tăng kali do thận có xu hướng chiếm phần đáy của sóng T ở bên trái làm sóng T trở nên hẹp
166. Đừng sợ hãi khi thấy rung nhĩ trong STEMI
Rung nhĩ là rối loạn nhịp hay gặp nhất trong tim mạch lâm sàng. Hiếm khi xảy ra trong ACS và hiếm khi kết hợp UA/ STEMI .
Tỷ lệ AF trong STEMI dưới 5%. Tất nhiên, AF kết hợp với nmct thành sau dưới và RVMI là một nguyên nhân quan trọng kích hoạt AF. LCX thường liên quan đến AF vì nó có nhánh nuôi nhĩ trái
Tác động lên huyết động học
AF có thể làm giảm huyết áp.
Sự thiếu máu cục bộ sẽ nặng hơn do tăng MVO2 Có thể gây bất ổn ở nhồi máu RV
AF trong STEMI – Có phải là trường hợp tối cấp cứu?
Nó sẽ là như vậy, tuy nhiên nếu huyết động ổn định không cần thiết phải hoảng sợ. cần giải quyết tình trạng thiếu oxy và tối ưu hóa liều beta blocker là đủ
Vai trò của DC Shock, Các biện pháp phòng ngừa trước khi gây sốc, các vấn đề sau khi sốc điện ?
Chỉ sốc điện nếu có bất ổn định về huyết động học hoặc thiếu máu cục bộ tiến triển (Rất khó để loại trừ trường hợp sau)
Cục máu đông có thể hình thành thậm chí trong vòng 24h và có thể gây đột quỵ do chấn động trong sốc điện có thể gây ra
Do đó bắt buộc phải làm siêu âm tim trước khi sốc điện Thuốc lựa chọn
Betablocker
nhóm 1c-Flecanide.
nhóm 3 -Amiodarone./Ibutilide/ Vai trò của Digoxin
Có nhiều lo lắng khi sử dụng digoxin trong ACS vì nó là thuốc chống loạn nhịp nhưng vẫn có vai trò trong xử trí rung nhĩ. Không có loại thuốc loạn nhịp nào có sẵn để kiểm soát nhịp tim mà không làm giảm chức năng LV
Kiểm soát tần số so với kiểm soát nhịp
Luôn luôn kiểm soát nhịp trong trường hợp ACS. Kiểm soát tần số không đặt ra trong trường hợp cấp dù amiodarone có thể giải quyết cả 2
Rung nhĩ QRS rộng
Như chúng ta biết, AF trong STEMI có thể gây dẫn truyền bất thường, và chúng ta được dạy là nhịp nhanh đều QRS rộng là VT trong trường hợp nmct nên khiến số liệu thống kê bị sai lệch
Nói cho cùng, cả hai rối loạn này đều không thấy sóng
P. tần số cao khó xác định khoảng RR không đều, tuy nhiên khi gây sốc điện thì AF hay VT đều đáp ứng, kết quả đều tốt
Tóm lại
AF trong STEMI là một rối loạn nhịp tim nguy hiểm và cần can thiệp khẩn cấp, nhưng không cần phải báo động. chỉ AF kèm STEMI có rối loạn huyết động mới cần sốc điện. nhiều khi nó chỉ thoáng qua
167. Kiểm soát tần số hay nhịp trong rung nhĩ?
Chúng ta có hai lựa chọn để xử trí AF. Tần số hoặc nhịp. 1 thập kỷ này đều chọn kiểm soát nhịp. chúng ta biết rằng, y học thường không tôn trọng logic‖. Bây giờ, chúng ta có dữ liệu rõ ràng và thống nhất rằng kiểm soát tần số là chiến lược tốt trong hầu hết tình huống của AF (nghiên cứu AFFIRM, RACE 1 và 2). Mục đích điều trị AF như sau.
Cải thiện triệu chứng tim đập nhanh Cải thiện huyết động
Giảm MVO2 và do đó tránh thiếu máu cục bộ Phòng ngừa lâu dài nhịp nhanh
Tránh đột quỵ
Có 3 lí do tại sao không nên chuyển nhịp
1. Chỉ 35% bệnh nhân về được nhịp xoang. Các cơn AF thoáng qua có thể xuất hiện bất cứ lúc nào
2. Các thuốc dùng chuyển nhịp rất độc
3. Kiểm soát tần số và dùng chống đông có thể giảm đột quỵ tốt hơn ở nhóm chuyển nhịp do nguy cơ đột quỵ do thiếu máu cục bộ vẫn tiếp tục phát sinh ở nhiều nơi như động mạch chủ và động mạch cảnh. Do đó, ở người có đột quỵ do AF trước đó, thường dùng chống đông ngăn đột quỵ chứ không phải kiểm soát nhịp. những bệnh nhân kiểm soát nhịp cần tiếp tục dùng chống đông và có thể mất đi lợi thế trị liệu hợp lý
168. Bao nhiêu trường hợp nhịp nhanh thất không đều?
Chúng ta biết, nhịp nhanh QRS rộng thường chúng ta sẽ chẩn đoán VT dù thận trọng khi áp dụng quy tắc này nếu nhịp nhanh QRS có RR không đều
Tất cả các VTs cổ điển nhịp thường đều. VT có thay đổi độ dài nhỏ trong chu kỳ ở VT nhưng chúng ta không thấy được nó trên ECG bề mặt
Không có quy tắc thực tiễn. RR không đều đặt ra câu hỏi nghiêm túc về chẩn đoán VT cổ điển. hầu hết các cơn nhịp nhanh không đều QRS rộng đều bị chẩn đoán thành rung nhĩ
Tuy nhiên, có thể xảy ra không đều trong suốt thời kỳ VT (có thể dưới 10%)
Khi nào VT có thể không đều bất thường?
Không đều xảy ra ngay khi Vt khởi phát vòng vào lại và cố gắng giảm tần số.
AV phân ly có thể làm VT không đều nhưng thay đổi tinh tế (sẽ không gây không đều nếu quá trình dẫn truyền ngược VA còn nguyên vẹn)
VT với nhiều điểm khởi phát và tổn thương thượng tâm mạc
Thuốc điều trị VT.Amiodarone có thể làm VT không đều vì nó làm kéo dài vòng vào lại và gây block AV cũng như dẫn đến phân ly AV
VT đa ổ
Thông điệp cuối cùng
Theo thống kê, cũng như thực tế, nguyên nhân hay gặp nhất gây nhịp nhanh không đều QRS rộng là rung nhĩ, cho dù QRS rộng hay hẹp